cho lưu huỳnh vào muôi sắt đốt cháy và đưa nhanh vào bình đậy nắp chặt lại. Khi lưu huỳnh cháy hết, để nguội thì khối lượng bình thay đổi thế nào

Những câu hỏi liên quan
Đốt nóng thìa sắt nhỏ có chứa lưu huỳnh bột trên ngọn lửa đèn cồn, lưu huỳnh nóng chảy, sau đó cháy trong không khí cho ngọn lửa xanh mờ. Đưa lưu huỳnh đang cháy vào bình đựng khí oxi, lưu huỳnh tiếp tục cháy cho ngọn lửa A. sáng hơn và sinh ra lưu huỳnh đioxit B. mờ hơn và sinh ra lưu huỳnh đioxit C. sáng hơn và sinh ra lưu huỳnh trioxit D. mờ hơn và sinh ra lưu huỳnh trioxi
Đọc tiếp
Đốt nóng thìa sắt nhỏ có chứa lưu huỳnh bột trên ngọn lửa đèn cồn, lưu huỳnh nóng chảy, sau đó cháy trong không khí cho ngọn lửa xanh mờ. Đưa lưu huỳnh đang cháy vào bình đựng khí oxi, lưu huỳnh tiếp tục cháy cho ngọn lửa
A. sáng hơn và sinh ra lưu huỳnh đioxit
B. mờ hơn và sinh ra lưu huỳnh đioxit
C. sáng hơn và sinh ra lưu huỳnh trioxit
D. mờ hơn và sinh ra lưu huỳnh trioxi
A
Đưa lưu huỳnh đang cháy ngoài không khí vào bình đựng khí O 2 thì lưu huỳnh cháy sáng hơn, cho sản phẩm là S O 2 (lưu huỳnh đioxit).
![]()
Đúng 1
Bình luận (0)
đốt cháy lưu huỳnh trong bình đựng không khí thì lưu huỳnh và oxi phản ứng vừa hết .Tính khối lượng của 16,8 lít hỗn hợp khí sau khi đốt cháy lưu huỳnh nếu lưu huỳnh cháy hết oxi còn dư .Tính phần trăm các khí sau phản ứng biết 1 mol hỗn hợp khí sau phản ứng nặng 33,6 gam
\(n_{hhkhí}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
Gọi \(n_{SO_2}=a\left(mol\right)\left(0< a< 0,75\right)\)
\(\rightarrow n_{O_2\left(dư\right)}=0,75-b\left(mol\right)\)
Ta có: \(\dfrac{64a+32\left(0,75-a\right)}{0,75}=\dfrac{33,6}{1}=33,6\left(\dfrac{g}{mol}\right)\)
\(\rightarrow a=0,0375\left(mol\right)\)
\(\rightarrow\left\{{}\begin{matrix}\%V_{SO_2}=\dfrac{0,0375}{0,75}=5\%\\\%V_{O_2\left(dư\right)}=100\%-5\%=95\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
đốt cháy lưu huỳnh trong bình đựng không khí thì lưu huỳnh và oxi vừa hết .Tính khối lượng của 16,8 lít hỗn hợp khí sau khi đốt cháy lưu huỳnh nếu lưu huỳnh cháy hết oxi còn dư .Tính % các khí sau phản ứng biết 1 mol hỗn hợp khí sau phản ứng nặng 33,6 gam
Đốt nóng thìa sắt nhỏ có chứ lưu huỳnh bột trên ngọn lửa đèn cồn, lưu huỳnh nóng chảy, sau đó chảy trong không khí cho ngọn lửa xanh nhạt. Đưa lưu huỳnh đang cháy vào bình đựng khí oxi, lưu huỳnh tiếp tục cháy cho ngọn lửa A. sáng hơn và sinh ra lưu huỳnh đioxit. B. mờ hơn và sinh ra lưu huỳnh đioxit. C. sáng hơn và sinh ra lưu huỳnh đioxit. D. mờ hơn và sinh ra lưu huỳnh đioxit.
Đọc tiếp
Đốt nóng thìa sắt nhỏ có chứ lưu huỳnh bột trên ngọn lửa đèn cồn, lưu huỳnh nóng chảy, sau đó chảy trong không khí cho ngọn lửa xanh nhạt. Đưa lưu huỳnh đang cháy vào bình đựng khí oxi, lưu huỳnh tiếp tục cháy cho ngọn lửa
A. sáng hơn và sinh ra lưu huỳnh đioxit.
B. mờ hơn và sinh ra lưu huỳnh đioxit.
C. sáng hơn và sinh ra lưu huỳnh đioxit.
D. mờ hơn và sinh ra lưu huỳnh đioxit.
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng oxi dư, thu được hỗn hợp ba khí (CO2, SO2, O2). Sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ thay đổi như thế nào? A. Tăng. B. Giảm. C. Có thể tăng hoặc giảm phụ thuộc vào lượng S và C. D. Không đổi.
Đọc tiếp
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng oxi dư, thu được hỗn hợp ba khí (CO2, SO2, O2). Sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ thay đổi như thế nào?
A. Tăng.
B. Giảm.
C. Có thể tăng hoặc giảm phụ thuộc vào lượng S và C.
D. Không đổi.
Đáp án D
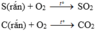
Từ 2 phương trình trên ta thấy số mol khí của chất tham gia phản ứng và sau phản ứng bằng nhau và không phụ thuộc vào lượng C, S => do vậy áp suất của bình sẽ không thay đổi khi ta đưa về nhiệt độ ban đầu
Đúng 0
Bình luận (0)
Trong 1 bình kín chứa 11,2l O2 (đktc) cho vào bình 12,8g lưu huỳnh rồi đốt cháy. Sau phản ứng xảy ra cho tiếp vào bình 3,1g phôtpho rồi đốt đốt đến khi kết thúc phản ứng. Hỏi a) P có cháy hết ko?tại sao? b) tính khối lượng oxit thu được sau phản ứng Mk đang cần gấp. Cảm ơn
\(n_{O_2}=0,5\left(mol\right);n_S=0,4\left(mol\right);n_P=0,1\left(mol\right)\)
a) \(S+O_2-^{t^o}\rightarrow SO_2\) (1)
Lập tỉ lệ : \(\dfrac{0,4}{1}< \dfrac{0,5}{1}\) => Sau phản ứng O2 dư
\(4P+5O_2-^{t^o}\rightarrow2P_2O_5\) (2)
\(n_{O_2\left(dưsaupu1\right)}=0,5-0,4=0,1\left(mol\right)\)
Lập tỉ lệ ở pứ (2) \(\dfrac{0,1}{4}< \dfrac{0,1}{5}\)=> P dư, O2 phản ứng hết
=> P không cháy hết
b) \(m_{oxit}=m_{SO_2}+m_{P_2O_5}=0,4.64+\dfrac{0,1.2}{5}.142=31,28\left(g\right)\)
Đúng 1
Bình luận (0)
Lưu huỳnh cháy theo sơ đồ phản ứng sau: Lưu huỳnh + khí oxi → Lưu huỳnh đioxit Nếu đốt cháy 48 gam lưu huỳnh và thu được 96 gam lưu huỳnh đioxit thì khối lượng oxi đã tham gia vào phản ứng là bao nhiêu?
Theo ĐLBT KL, có: mS + mO2 = mSO2
⇒ mO2 = mSO2 - mS = 96 - 48 = 48 (g)
Đúng 0
Bình luận (0)
Lưu huỳnh cháy theo sơ đồ phản ứng sau: Lưu huỳnh + khí oxi → Lưu huỳnh đioxit Nếu đốt cháy 48 gam lưu huỳnh và thu được 96 gam lưu huỳnh đioxit thì khối lượng oxi đã tham gia vào phản ứng là bao nhiêu?
Bài 14: Một bình kín có dung tích 1,4l đầy không khí (đktc). Nếu đốt cháy 2,5g photpho P trong bình, thì photpho có cháy hết không?Bài 15: Đốt cháy 100g hỗn hợp bột lưu huỳnh S và sắt Fe dùng hết 33,6l khí oxi (đktc). Tính khối lượng mỗi chất trong hỗn hợp. Biết rằng đốt Fe tạo ra Fe3O4Bài 16: Dẫn 11,2 lít khí H2 (đktc) qua ống nghiệm chứa 16 gam CuO. Sau khi phản ứng kết thúc, hãy tính: khối lượng kim loại thu được. Sau phản ứng có chất nào còn dư, dư bao nhiêu?
Đọc tiếp
Bài 14: Một bình kín có dung tích 1,4l đầy không khí (đktc). Nếu đốt cháy 2,5g photpho P trong bình, thì photpho có cháy hết không?
Bài 15: Đốt cháy 100g hỗn hợp bột lưu huỳnh S và sắt Fe dùng hết 33,6l khí oxi (đktc). Tính khối lượng mỗi chất trong hỗn hợp. Biết rằng đốt Fe tạo ra Fe3O4
Bài 16: Dẫn 11,2 lít khí H2 (đktc) qua ống nghiệm chứa 16 gam CuO. Sau khi phản ứng kết thúc, hãy tính: khối lượng kim loại thu được. Sau phản ứng có chất nào còn dư, dư bao nhiêu?
Bài 14
\(n_{O_2}=\dfrac{1.4}{22,4}=0,0625\left(mol\right)\)
\(n_P=\dfrac{2.5}{31}=0,0806451\left(mol\right)\)
4P + 5O2 ----to--->2P2O5
Xét tỉ lệ : \(\dfrac{0.0625}{5}< \dfrac{0.0806451}{4}\)
=> P ko cháy hết
Đúng 2
Bình luận (0)
bài 15
\(n_{O_2}=\dfrac{3.36}{22,4}=0,15\left(mol\right)\)
Gọi nFe = a ( mol ) và nS = b (mol )
PTHH :
S + O2 ---to---> SO2
3Fe + 2O2 ----to----> Fe3O4
Ta có 32b + 56a= 100
Theo PT : nS = nO2 = b (mol)
Theo PT : nO2 = 2/3 nFe = 2/3a ( mol)
=> 2/3a + b = 1,5
Từ những điều trên \(\left[{}\begin{matrix}56a+32b=100\\\dfrac{2}{3}a+b=1,5\end{matrix}\right.\Leftrightarrow\left[{}\begin{matrix}a=1,5\left(mol\right)\\b=0,5\left(mol\right)\end{matrix}\right.\)
\(m_{Fe}=1,5.56=84\left(g\right)\)
\(m_S=0,5.32=16\left(g\right)\)
Đúng 2
Bình luận (0)
Bài 16 :
\(n_{H_2}=\dfrac{11.2}{22,4}=0,5\left(mol\right)\)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
Ta thấy : 0,5 > 0,2 => H2 dư , CuO đủ
PTHH : CuO + H2 -> Cu + H2O
0,2 0,2 0,2
\(m_{Cu}=0,2.64=12,8\left(g\right)\)
\(m_{H_2\left(dư\right)}=\left(0,5-0,2\right).2=0,6\left(g\right)\)
Đúng 2
Bình luận (0)
















