Đốt cháy 5,6l CH4 trong oxi
a/ Viết PTHH
b/ Tính khối lượng H2O thu được?
c/ Tính thể tích khí sinh ra?
d/ Tính khối lượng nước cần dùng để điều chế lượng oxi trên? Biết khối lượng nước dùng dư 20%
đốt cháy 5,4 gam al trong bình chứa oxi
a,viết pthh
b, tính thể tích oxi cần dùng đo ở đktc
c, tính khối lượng KMnO4 cần dùng để điều chế lượng oxi trên
a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: \(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
0,2--->0,15
b) \(V_{O_2}=0,15.22,4=3,36\left(l\right)\)
c) PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
0,3<-----------------------------------0,15
\(\Rightarrow m_{KMnO_4}=0,3.158=47,4\left(g\right)\)
Đốt cháy hoàn toàn11,2 lít khí metan (CH4 ):
a) Tính thể tích khí oxi cần dùng để đốt cháy hết lượng metan ở trên?
b) Tính khối lượng CO2 và H2O sinh ra sau phản ứng?
c) Dẫn toàn bộ sản phẩm sinh ra ở trên vào dung dịch nước vôi trong lấy dư thu được m(g) kết tủa. Tính m?
Thể tích các khí đo ở đktc
Đáp án:
VO2=22,4 (l); VCO2=11,2 (l)��2=22,4 (�); ���2=11,2 (�)
Giải thích các bước giải:
Ta có:
đốt cháy hoàn toàn 2,24 lít etilen a). viết pthh b). tính thể tích oxi bằng 20% thể tích không khí c). tính khối lượng CO2 sinh ra d). không khí cần dùng , biết thể tin dẫn toàn bộ khí CO2 trên thu đc dd nước vôi trong dư , tính khối lượng kết tủa
a, nC2H4 = 2,24/22,4 = 0,1 (mol)
PTHH: C2H4 + 3O2 -to-> 2CO2 + 2H2O
Mol: 0,1 ---> 0,3 ---> 0,2
b, VO2 = 0,3 . 22,4 = 6,72 (l)
c, mCO2 = 0,2 . 44 = 8,8 (g)
d, Vkk = 6,72 . 5 = 33,6 (l)
PTHH: Ca(OH)2 + CO2 -> CaCO3 + H2O
Mol: 0,2 <--- 0,2 ---> 0,2
mCaCO3 = 0,2 . 100 = 20 (g)
Đốt cháy 11,2 lít khí Hiđro trong bình chứa 10,08 lít khí Oxi
a) Sau phản ứng, chất nào còn dư? Dư bao nhiêu gam?
b) Tính khối lượng sản phảm thu được
c) Tính khối lượng Kali pemanganat cần dùng để điều chế được lượng oxi dùng cho phản ứng trên
a) \(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{O_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{0,5}{2}< \dfrac{0,45}{1}\) => H2 hết, O2 dư
PTHH: 2H2 + O2 --to--> 2H2O
0,5-->0,25----->0,5
=> \(m_{O_2\left(dư\right)}=\left(0,45-0,25\right).32=6,4\left(g\right)\)
b) \(m_{H_2O}=0,5.18=9\left(g\right)\)
c)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,5<-----------------------------------0,25
=> \(m_{KMnO_4}=0,5.158=79\left(g\right)\)
Đốt cháy hoàn toàn 16,8 gam sắt trong không khí
a) Tính khối lượng sản phẩm thu được
b) Tính thể tích khí oxi, và thể tích không khí cần dùng ở điều kiện tiêu chuẩn ( biết oxi chiếm 20% thể tích không khí)
c) Tính khối lượng KMnO4 cần dùng để điều chế đủ oxi cho phản ứng trên? Biết rằng lượng oxi thu được hao hụt 20%
a) nFe = 16,8/56 = 0,3 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
Mol: 0,3 ---> 0,2 ---> 0,1
mFe3O4 = 0,1 . 232 = 23,2 (g)
b) VO2 = 0,2 . 22,4 = 4,48 (l)
Vkk = 4,48 . 5 = 22,4 (l)
c) H = 100% - 20% = 80%
nO2 (LT) = 0,2 : 80% = 0,25 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,25 . 2 = 0,5 (mol)
mKMnO4 = 0,5 . 158 = 79 (g)
bột nhôm cháy trong oxi tạo ra nhôm oxit (al2o3)
a) viết pthh
b) tính thể tích oxi (ở đktc) cần dùng để đốt cháy hoàn toàn 0.54 gam bột nhôm
c) tính khối lượng kmno4 cần dùng để điều chế lượng oxi dùng cho phản ứng trên
Câu 3: Đốt cháy hoàn toàn 16,8 gam Sắt (Fe) trong không khí
a) Tính khối lượng sản phẩm thu được?
b) Tính thể tích khí oxi, và thể tích không.khí cần dùng ở đktc? (biết rằng oxi chiếm 20% thể tích không khí)
c) Tính khối lượng KMnO4 cần dùng để điều chế đủ oxi cho phản ứng trên? Biết rằng lượng oxi thu được hao hụt 20%
Cho biết: Fe = 56, O = 16, K = 39, Mn = 55
a.b.
\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe_3O_4}=0,1.232=23,2g\)
\(V_{O_2}=0,2.22,4=4,48l\)
\(V_{kk}=4,48.5=22,4l\)
c.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{\left(100-20\right)\%}=79g\)
a/ Số mol Fe là : nFe = 16,8: 56 = 0,3 mol
PTPƯ:
3Fe + 2O2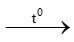 Fe3O4 (1)
Fe3O4 (1)
0,3 mol → 0,2mol → 0,1 mol
Từ (1) ta có số mol Fe3O4 = 0,1mol
→ m Fe3O4 = n.M = 0,1.232 = 23,2gam
b/ Từ (1) ta có số mol O2 đã dùng nO2 = 0,2 mol
Thể tích khí oxi đã dùng ở đktc: VO2 = n.22,4 = 0,2.22,4 = 4,48 lít
Thể tích không khí đã dùng: Vkk = 5. VO2= 5.4,48 = 22,4 lít.
c/ PTPƯ
2 KMnO4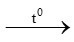 K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
0,4444mol ← 0,222mol
Vì lượng Oxi thu được hao hụt 10% nên số mol O2 cần có là:
nO2 = 0,2mol.100/90 = 0.222 mol
Từ (2) ta có số mol KMnO4 = 0,444mol
Khối lượng KMnO4 bị nhiệt phân
mKMnO4 = n.M = 0,444.158 = 70.152 gam
giúp em mấy câu này với ạ, em đang cần gấp. Em cảm ơn.
Câu 2:Đốt cháy hoàn toàn 18,6g photpho trong oxi
a/ tính thể tích oxi cần dùng(đktc)
b/Tính khối lượng sản phẩm?
c/Tính khối lượng KCLO3 cần dùng để điều chế được oxi nói trên?
nP = 18,6/31 = 0,6 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
Mol: 0,6 ---> 0,75 ---> 0,3
VO2 = 0,75 . 22,4 = 16,8 (l)
mP2O5 = 0,3 . 142 = 42,6 (g)
PTHH: 2KClO3 -> (t°, MnO2) 2KCl + 3O2
nKClO3 = 0,75 : 3 . 2 = 0,5 (mol)
mKClO3 = 122,5 . 0,5 = 61,25 (g)
Đốt cháy 16,8 gam Iron thu được Iron (II,III) oxide
a)viết PTHH
b)tính thể tích của oxi cần dùng
c) tính khối lượng của Iron (II,III) oxide tạo thành
d) tính khối lượng thuốc tím cần dùng để điều khí oxyen cho phản ứng trên
a,
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b, \(nFe=\dfrac{16,8}{56}=0,3\left(mol\right)\)
\(\Rightarrow nO_2=0,3.\dfrac{2}{3}=0,2\left(mol\right)\)
\(VO_2=0,2.24,79=4,958\left(l\right)\)
c, \(nFe_3O_4=0,1\left(mol\right)\)
\(mFe_3O_4=0,1.232=23,2\left(gam\right)\)