Giúp câu này hộ!!!
Hòa tan hỗn hợp sắt và kiểm cần dùng 500 ml dung dịch HCl 1M. Sau phản ứng thu được dung dịch X, cô cạn dung dịch X thu được 33,55 gam muối khan. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp
hòa tan hoàn toàn 14,6g hỗn hợp gồm Zn và ZnO bằng dung dịch HCl 7,3%. cô cạn dung dịch sau phản ứng thu được 27,2g muối khan
a. tính phần trăm khối lượng mỗi chất ban đầu
b. tính khối lượng dung dịch cần dùng
a) Gọi n Zn = a(mol) ; n ZnO = b(mol)
=> 65a + 81b = 14,6(1)
$Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
n ZnCl2 = a + b = 27,2/136 = 0,2(2)
Từ (1)(2) suy ra : a = b = 0,1
%m Zn = 0,1.65/14,6 .100% = 44,52%
%m ZnO = 100% -44,52% = 55,45%
b)
n HCl = 2n Zn + 2n ZnO = 0,4(mol)
m dd HCl = 0,4.36,5/7,3% = 200(gam)
Một hỗn hợp X gồm ba muối NaF, NaCl, NaBr nặng 4,82 gam. Hòa tan hoàn toàn X trong nước được dung dịch A. Sục khí clo dư vào dung dịch A rồi cô cạn hoàn toàn dung dịch sau phản ứng thu được 3,93 gam muối khan. Lấy một nửa lượng muối khan này hòa tan vào nước rồi cho phản ứng với dung dịch AgNO3 dư thì thu được 4,305 gam kết tủa Z. Tính phần trăm khối lượng mỗi muối trong hỗn hợp ban đầu.
A. 14,29% NaF, 57,14% NaCl, 28,57% NaB
B. 57,14% NaF, 14,29% NaCl, 28,57% NaBr
C. 8,71% NaF, 48,55% NaCl, 42,74% NaBr
D. 48,55% NaF, 42,74% NaCl, 8,71% NaBr
Hòa tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,28M thu được dung dịch X và 8,736 lít khí H2 (ở đktc). Cô cạn dung dịch X thu được lượng muối khan là
A. 38,93 gam
B. 103,85 gam
C. 25,95 gam
D. 77,86 gam
a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (1)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\) (2)
b) Dựa vào đề, ta thấy chắc chắn HCl dư
Ta có: \(\Sigma n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Gọi số mol của Fe là \(a\) \(\Rightarrow n_{H_2\left(1\right)}=a\)
Gọi số mol của Mg là \(b\) \(\Rightarrow n_{H_2\left(2\right)}=b\)
Ta lập được hệ phương trình:
\(\left\{{}\begin{matrix}56a+24b=8\\a+b=0,2\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=56\cdot0,1=5,6\left(g\right)\\m_{Mg}=24\cdot0,1=2,4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{8}\cdot100\%=70\%\\\%m_{Mg}=30\%\end{matrix}\right.\)
c) Theo các PTHH: \(n_{FeCl_2}=n_{MgCl_2}=n_{Fe}=n_{Mg}=0,1mol\)
\(\Rightarrow\left\{{}\begin{matrix}m_{FeCl_2}=0,1\cdot127=12,7\left(g\right)\\m_{MgCl_2}=0,1\cdot95=9,5\left(g\right)\end{matrix}\right.\) \(\Rightarrow m_{muối}=22,2\left(g\right)\)
d) Ta có: \(\Sigma n_{HCl}=\dfrac{500\cdot16\%}{36,5}=\dfrac{160}{73}\left(mol\right)\)
\(\Rightarrow n_{HCl\left(dư\right)}=\dfrac{654}{365}\left(mol\right)\) \(\Rightarrow m_{HCl\left(dư\right)}=\dfrac{654}{365}\cdot36,5=65,4\left(g\right)\)
Mặt khác: \(m_{dd}=m_{hh}+m_{ddHCl}-m_{H_2}=507,6\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{12,7}{507,6}\cdot100\%\approx2,5\%\\C\%_{MgCl_2}=\dfrac{9,5}{507,6}\cdot100\%\approx1,87\%\\C\%_{HCl\left(dư\right)}=\dfrac{65,4}{507,6}\cdot100\%\approx12,88\%\end{matrix}\right.\)
Bài 8: Hòa tan hoàn toàn 2,055 gam hỗn hợp 2 kim loại Al, Mg cần 205 ml dung dịch HCl 1M
(vừa đủ). Sau khi phản ứng kết thúc, cô cạn dung dịch thu được m gam muối khan. Tính m.
PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
a_____3a_______a______\(\dfrac{3}{2}\)a (mol)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
b_____2b_______b_____b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}27a+24b=2,055\\3a+2b=0,205\cdot1\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,045\\b=0,035\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{AlCl_3}=0,045\cdot133,5=6,0075\left(g\right)\\m_{MgCl_2}=0,035\cdot95=3,325\left(g\right)\end{matrix}\right.\)
Hòa tan hoàn toàn m gam hỗn hợp Na, K, Ba, Al vào nước được dung dịch X và 8,512 lít H2 (đktc). Cho X phản ứng với 200 ml dung dịch H2SO4 1,25M và HCl 1M thu được 24,86 gam kết tủa và dung dịch Y chỉ chứa các muối clorua và sunfat trung hòa. Cô cạn Y được 30,08 gam chất rắn khan. Phần trăm khối lượng của Ba có trong hỗn hợp ban đầu là:
A. 44,16%
B. 60,04%
C. 35,25%
D. 48,15%
Hòa tan hoàn toàn m gam hỗn hợp Na, K, Ba, Al vào nước được dung dịch X và 8,512 lít H2 (đktc). Cho X phản ứng với 200 ml dung dịch H2SO4 1,25M và HCl 1M thu được 24,86 gam kết tủa và dung dịch Y chỉ chứa các muối clorua và sunfat trung hòa. Cô cạn Y được 30,08 gam chất rắn khan. Phần trăm khối lượng của Ba có trong hỗn hợp ban đầu là:
A. 44,16%
B. 60,04%
C. 35,25%
D. 48,15%
Đáp án B
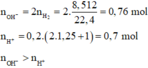
=> Kết tủa chứa BaSO4 và Al(OH)3.
• Có 24 , 86 + 30 , 08 = m KL + m OH - trong Al ( OH ) 3 + m SO 4 2 - + m Cl -
=> m + 17(0,76 - 0,7) + 96.0,25 + 35,5.0,2 = 54,94 g
=> m = 22,82 g
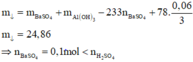
=> Chứng tỏ Ba2+ tạo kết tủa hoàn toàn: n Ba = 0 , 1 mol
![]()
Đề chưa nói rõ là : tác dụng với dung dịch axit nào nên có lẽ là HCl hoặc H2SO4 , thứ hai là câu c không đủ dữ kiện đề bài để giải nhé.
\(Đặt:n_{Mg}=x\left(mol\right),n_{Fe}=y\left(mol\right)\)
\(m_{hh}=24x+56y=8\left(g\right)\left(1\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{H_2}=x+y=0.2\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):x=y=0.1\)
\(\%Mg=\dfrac{0.1\cdot24}{8}\cdot100\%=30\%\\ \%Fe=70\%\)
\(m_M=m_{MgCl_2}+m_{FeCl_2}=0.1\cdot95+0.1\cdot127=22.2\left(g\right)\)
Hòa tan hoàn toàn 43,0 gam hỗn hợp X gồm Al, Zn, FeO, Cu(NO3)2 cần dùng hết 860 ml dung dịch H2SO4 1M thu được hỗn hợp khí Y (đktc) gồm 0,12 mol NO và 0,26 mol H2, đồng thời thu được dung dịch Z chỉ chứa các muối sunfat trung hòa. Cô cạn dung dịch Z thu được 113,8 gam muối khan. Thành phần phần trăm khối lượng của Al trong hỗn hợp X có giá trị gần nhất là
A. 25,5%.
B. 8,5%.
C. 20,5%.
D. 22,5%.