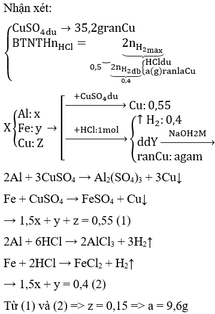
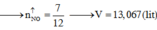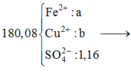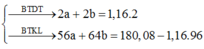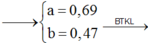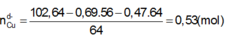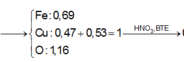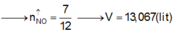Cho 10 gam hỗn hợp X gồm CuO và Cu vào dung dịch axit sunfuric đặc
dư. Đun nóng để phản ứng xảy ra hoàn toàn thu được 2,24 lít khí Y (đktc).
a.
Viết các phương trình phản ứng đã
xảy ra. Xác định khí Y.
b.
Tính thành phần % theo khối lượng mỗi chất trong
hỗn hợp X
Hóa học8