Cho 1,6g một oxit sắt tác dụng hết với 30ml dung dịch H2SO4 1M. Oxit sắt đó là

Những câu hỏi liên quan
Cho 1,6 gam một oxit sắt tác dụng vừa đủ với 60 ml dung dịch HCl 1M. Xác định công thức oxit sắt.
Gọi CTHH của oxit là $Fe_xO_y$
$n_{HCl} = 0,06(mol)$
$Fe_xO_y + 2yHCl \to xFeCl_{2y/x} + yH_2O$
$n_{oxit} = \dfrac{1}{2y}n_{HCl} = \dfrac{0,03}{y}(mol)$
$\Rightarrow \dfrac{0,03}{y}.(56x + 16y) = 1,6$
$\Rightarrow \dfrac{x}{y} = \dfrac{2}{3}$
Vậy oxit là $Fe_2O_3$
Đúng 3
Bình luận (0)
X là một oxit sắt. Biết 1,6g X tác dụng vừa hết với 300ml dung dịch HCl 2M. Xác định công thức của oxit sắt
Hình như đề sai rồi bạn /_\ mình sửa 1,6g thành 16g nha
------------------------------------
\(n_{HCl}=0,3.2=0,6\left(mol\right)\)
Gọi n là hóa trị của Fe
cthc: \(Fe_2O_n\)
Pt: \(Fe_2O_n+2nHCl\rightarrow2FeCl_n+nH_2O\)
112 + 16n 2n
16 (g) 0,6mol
\(\Rightarrow\dfrac{112+16n}{16}=\dfrac{2n}{0,6}\)
\(\Rightarrow n=3\)
Vậy cthc: Fe2O3
Đúng 0
Bình luận (1)
Cho hỗn hợp A gồm Al và và một oxit sắt. Chia hỗn hợp A thành 2 phần bằng nhau. Phần 1: cho tác dụng với dung dịch H2SO4 loãng thu được 0,672 lít khí (đktc). Phần 2: Phản ứng nhiệt nhôm hoàn toàn, thu được hỗn hợp B, cho B tác dụng với dung dịch NaOH dư thu được 134,4 ml khí (đktc) sau đó cho tiếp dung dịch H2SO4 loãng, dư được 0,4032 lít H2(đktc). Oxit sắt là: A. Fe2O3 B. FeO C. Fe3O4 D. Không xác định
Đọc tiếp
Cho hỗn hợp A gồm Al và và một oxit sắt. Chia hỗn hợp A thành 2 phần bằng nhau.
Phần 1: cho tác dụng với dung dịch H2SO4 loãng thu được 0,672 lít khí (đktc).
Phần 2: Phản ứng nhiệt nhôm hoàn toàn, thu được hỗn hợp B, cho B tác dụng với dung dịch NaOH dư thu được 134,4 ml khí (đktc) sau đó cho tiếp dung dịch H2SO4 loãng, dư được 0,4032 lít H2(đktc). Oxit sắt là:
A. Fe2O3
B. FeO
C. Fe3O4
D. Không xác định
Đáp án C
Phần 1: Tác dụng vói dung dịch H2SO4 loãng gồm Al và FexOy nên n H 2 = 3 2 n Al ⇒ n Al = 0 , 02
Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn và hỗn hợp B tác dụng với dung dịch NaOH dư có H2 nên B có Fe, A12O3 và Al dư. Có n Al du = 2 3 n H 2 ( NaOH ) = 0 , 004 .
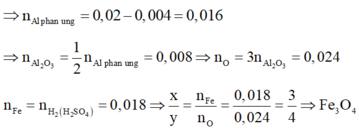
Đúng 0
Bình luận (0)
Cho 7,2 gam một oxit sắt tác dụng với dung dịch axit HCl có dư. Sau phản ứng thu được 12,7 gam một muối khan. Tim công thức oxit sắt đó.
Fe x O y + 2yHCl → x FeCl 2 y / x + y H 2 O
Theo phương trình : (56x + 16y) gam cho (56x + 71y) gam muối
Theo đề bài: 7,2 gam cho 12,7 gam
Giải ra, ta có : x/y = 1/1 . Công thức oxit săt là FeO.
Đúng 0
Bình luận (1)
Bài 1: Cho kim loại sắt vào dung dịch axit H2SO4 loãng. Sau một thời gian, sắt tan hết thu được 6,72 lit khí hiđrô (đktc).
a) Tính khối lượng sắt ban đầu?
b) Để có lượng sắt tham gia phản ứng trên, phải cho bao nhiêu gam sắt(III) oxit tác dụng với khí hiđrô?
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3
a)\(m_{Fe}=0,3\cdot56=16,8g\)
b)\(Fe_2O_3+3H_2\rightarrow3Fe+3H_2O\)
0,1 0,3 0,3
\(m_{Fe_2O_3}=0,1\cdot160=16g\)
Đúng 4
Bình luận (0)
a)nH2 =6,72:22,4=0,3(mol)
PTHH Fe+H2SO4--->FeSO4+H2
theo pt , nFe = nH2 = 0,3 (mol)
=> mFe =n.M=0,3.56=16,8(g)
b) Ta có nH2=nFe=0,3(MOL)
Pthh: Fe2O3 + 3H2 ---> 2Fe + 3H2O
theo pt , nFe2O3=1/3 nH2=0,1(mol)
=> mFe2O3= n.M=0,1.(56.2+16.3)=16(g)
Vậy để có lượng sắt tham gia phản ứng trên phải có 16g Fe2O3 để tác dụng với H2
Đúng 1
Bình luận (0)
Cho hỗn hợp A gồm Al và một oxit sắt. Chia hỗn hợp A thành 2 phần bằng nhau.Phần 1: Cho tác dụng với dung dịch
H
2
SO
4
loãng thu được 13,44 lít khí (đktc).Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được hỗn hợp B. Cho B tác dụng với dung dịch NaOH dư thu được 3,36 lít khí (đktc) và chất rắn C. Cho chất rắn C vào dung dịch
H
2
SO
4
loãng, dư được...
Đọc tiếp
Cho hỗn hợp A gồm Al và một oxit sắt. Chia hỗn hợp A thành 2 phần bằng nhau.
Phần 1: Cho tác dụng với dung dịch H 2 SO 4 loãng thu được 13,44 lít khí (đktc).
Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được hỗn hợp B. Cho B tác dụng với dung dịch NaOH dư thu được 3,36 lít khí (đktc) và chất rắn C. Cho chất rắn C vào dung dịch H 2 SO 4 loãng, dư được 6,72 lít H 2 (đktc). Công thức của oxit sắt là
A. FeO
B. Fe 2 O 3
C. Fe 3 O 4
D. không xác định được
Cho hỗn hợp A gồm Al và một oxit sắt. Chia hỗn hợp A thành 2 phần bằng nhau.Phần 1: Cho tác dụng với dung dịch
H
2
SO
4
loãng thu được 6,72 lít khí (đktc).Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được hỗn hợp B. Cho B tác dụng với dung dịch NaOH dư thu được 1,344 lít khí (đktc) và chất rắn C. Cho chất rắn C vào dung dịch
H
2
SO
4
loãng, dư được...
Đọc tiếp
Cho hỗn hợp A gồm Al và một oxit sắt. Chia hỗn hợp A thành 2 phần bằng nhau.
Phần 1: Cho tác dụng với dung dịch H 2 SO 4 loãng thu được 6,72 lít khí (đktc).
Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được hỗn hợp B. Cho B tác dụng với dung dịch NaOH dư thu được 1,344 lít khí (đktc) và chất rắn C. Cho chất rắn C vào dung dịch H 2 SO 4 loãng, dư được 4,032 lít H 2 (đktc). Công thức của oxit sắt là
A. FeO
B. Fe 2 O 3
C. Fe 3 O 4
D. không xác định được
Chuyển hoá hoàn toàn 1,68 gam sắt thành một oxit sắt, sau đó hoà tan hết oxit sắt bằng dung dịch axit H2SO4 loãng 0,2M thu được dung dịch chứa 16,56 gam muối.
a) Xác định công thức phân tử của oxit sắt.
b) Tính thể tích dd H2SO4 đã dùng. Biết rằng lượng axit đem dùng dư 20% so với lượng cần thiết.
Câu 1 : Cho 2,32g hh gồm FeO , Fe2O3 , Fe3O4 ( trong đó số mol FeO bằng số mol Fe2O3 ) tác dụng vừ đủ với V lit dd HCl 1M . Giá trị của V ?
Câu 2 : Khử hoàn toàn 11,6g oxit sắt bằng CO ở nhiệt độ cao . Sản phẩm khí dẫn vào dd Ca(OH)2 dư , tạo ra 20g kết tủa . Công thứ của oxit sắt là ?
Câu 3 : X là 1 oxit sắt . Biết 1,6g X tác dụng vừa hết với 30ml dd HCl 2M . X là oxit nào của sắt ?
Đọc tiếp
Câu 1 : Cho 2,32g hh gồm FeO , Fe2O3 , Fe3O4 ( trong đó số mol FeO bằng số mol Fe2O3 ) tác dụng vừ đủ với V lit dd HCl 1M . Giá trị của V ?
Câu 2 : Khử hoàn toàn 11,6g oxit sắt bằng CO ở nhiệt độ cao . Sản phẩm khí dẫn vào dd Ca(OH)2 dư , tạo ra 20g kết tủa . Công thứ của oxit sắt là ?
Câu 3 : X là 1 oxit sắt . Biết 1,6g X tác dụng vừa hết với 30ml dd HCl 2M . X là oxit nào của sắt ?
Gọi CTTQ của ox sắt là FexOy
PTHH ; \(Fe_xO_y+yCO\underrightarrow{t^o}xFe+yCO_2\) (1)
\(56x+16y\left(g\right)\)________________ymol
__11,6g____________________0,2mol
Vì Ca(OH)2 dư nên xảy ra pư tạo muối TH
\(CO_2\left(0,2\right)+Ca\left(OH\right)_2\rightarrow CaCO_3\left(0,2\right)+H_2O\)
\(n_{CaCO_3}=0,2mol\)
(1) => 11,2x + 3,2y = 11,6y
=> 11,2x = 8,4y
=> \(\dfrac{x}{y}=\dfrac{3}{4}\)
=> CTHH là Fe3O4
Câu 1 có thiếu đề ko bạn?
Đúng 0
Bình luận (0)
Gọi CTTQ của ox sắt là FexOy
\(PTHH:\left(\dfrac{0,03}{y}\right)Fe_xO_y+2yHCl\left(0,06\right)\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2O\)
\(n_X=\dfrac{1,6}{56x+16y}\left(mol\right)\)
\(\Rightarrow\dfrac{0,03}{y}=\dfrac{1,6}{56x+16y}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTTh của X là Fe2O3
Đúng 0
Bình luận (0)
Xem thêm câu trả lời

















