Câu 1: Dẫn 2,8 lít hỗn hợp ch4 và C3H6 đi qua bình đựng dung dịch nước Brom đã làm mất màu hoàn toàn dung dịch có chứa 4g Brom.
a, Tính thể tích mỗi khí có trong hỗn hợp.
b, Tính thể tích Oxi cần dùng để đốt cháy hoàn toàn hỗn hợp khí ban đầu.
c, Khí sinh ra cho đi qua bình đựng 300 ml dung dịch sau phản ứng.
Câu 2: 3,36 lít hỗn hợp khí CH4 và C2H4 có khối lượng 3g
a, Tính thành phần phần trăm các chất có trong hỗn hợp theo khối lượng và thể tích.
b, Nếu dẫn 1,68 lít khí trên (đktc) đi qua bình đựng dung dịch nước Brom thấy dung dịch Brom bị nhạt màu. Viết phương trình phản ứng. Khối lượng bình đựng dung dịch nước Brom tăng thêm bao nhiêu?
( LÀM ƠN GIÚP EM VỚI... EM CẦN GẤP Ạ =(((( )

Những câu hỏi liên quan
Dẫn 22,4 lít hỗn hợp khí Metan và Etylen đi qua bình đựng dung dịch nước brom, đã làm mất màu hoàn toàn một dung dịch brom chứa 8 g brom.
a. Viết PTHH.
b. Tính phần trăm thể tích mỗi khí có trong hỗn hợp.
c. Tính thể tích khí oxi cần để đốt cháy hoàn toàn hỗn khí nói trên. Biết các thể tích khí đều đo ở đktc
C2H4+Br2->C2H4Br2
0,05---0,05
n Br2=\(\dfrac{8}{160}\)=0,05 mol
V%C2H4=\(\dfrac{0,5.22,4}{22,4}\).100=5%
=>%CH4=95%
Đúng 4
Bình luận (0)
Dẫn 5,6 lít (đktc) khí metan và etilen đi qua bình đựng dung dịch nước brom, đã làm mất màu hoàn toàn dung dịch có chứa 4 gam brom. Tính thành phần phần trăm theo thể tích mỗi chất khí có trong hỗn hợp?
\(n_{hh\left(CH_4,C_2H_4\right)}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ n_{Br_2}=\dfrac{4}{160}=0,025\left(mol\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ n_{C_2H_4}=n_{Br_2}=0,025\left(mol\right)\)
Vì số mol tỉ lệ thuận với thể tích, nên ta có:
\(\%n_{C_2H_4}=\dfrac{0,025}{0,25}.100\%=10\%\\ \Rightarrow\%V_{C_2H_4}=10\%;\%V_{CH_4}=100\%-10\%=90\%\)
Đúng 0
Bình luận (0)
Dẫn 5,6 lít (đktc) khí metan và etilen đi qua bình đựng dung dịch nước brom, đã làm mất màu hoàn toàn dung dịch có chứa 4 gam brom. Thể tích khí metan (đktc) trong hỗn hợp là
A. 0,56 lít.
B. 5,04 lít.
C. 0,28 lít.
D. 3,36 lít
Dẫn 2 khí qua dung dịch nước brom chỉ có C 2 H 4 phản ứng
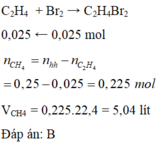
Đúng 0
Bình luận (0)
Dẫn 6,72 lít khí ở điều kiện tiêu chuẩn gồm metan và etilen đi qua bình dung dịch nước brom đã làm mất màu hoàn toàn dung dịch chứa 6gam brom . Tính thành phần , phần trăm về thể tích mỗi chất có trong hỗn hợp
Ta có: \(n_{Br_2}=\dfrac{6}{160}=0,0375\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,0375\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,0375.22,4}{6,72}.100\%=12,5\%\\\%V_{CH_4}=87,5\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hỗn hợp A gồm các khí metan, etilen và axetiien. Dẫn từ từ 2,8 lít hồn hợp, A (đktc) qua bình chứa dung dịch brom, thấy bình brom bị nhạt màu và có 20 gam brom tham gia phản ứng. Mặt khác, đốt cháy hoàn toàn 5,6 lít A (đktc) rồi cho toàn bộ sản phẩm cháy qua bình đựng 180 gam dung dịch NaOH 20% sau thí nghiệm thu được dung dịch chứa NaOH với nồng độ 2,75%. Tính thành phần % theo thể tích của mỗi khí trong hỗn hợp A
Đọc tiếp
Hỗn hợp A gồm các khí metan, etilen và axetiien. Dẫn từ từ 2,8 lít hồn hợp, A (đktc) qua bình chứa dung dịch brom, thấy bình brom bị nhạt màu và có 20 gam brom tham gia phản ứng. Mặt khác, đốt cháy hoàn toàn 5,6 lít A (đktc) rồi cho toàn bộ sản phẩm cháy qua bình đựng 180 gam dung dịch NaOH 20% sau thí nghiệm thu được dung dịch chứa NaOH với nồng độ 2,75%. Tính thành phần % theo thể tích của mỗi khí trong hỗn hợp A
nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
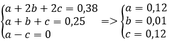
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%
Đúng 0
Bình luận (0)
Hỗn hợp khí A gồm CH4 và C2H4. Dẫn hỗn hợp A qua bình đựng dung dịch brom dư, sau phản ứng khối lượng bình brom tăng 9,8 (g). Mặt khác nếu đốt cháy hoàn toàn hỗn hợp khí A cần dùng 34,72 lít khí oxi ( ở đktc). Tính % về thể tích của CH4 và C2H4 trong hỗn hợp A . Giải giúp em với ạ :< em đang cần gấp
Hỗn hợp khí A gồm CH4 và C2H4. Dẫn hỗn hợp A qua bình đựng dung dịch brom dư, sau phản ứng khối lượng bình brom tăng 9,8 (g). Mặt khác nếu đốt cháy hoàn toàn hỗn hợp khí A cần dùng 34,72 lít khí oxi ( ở đktc). Tính % về thể tích của CH4 và C2H4 trong hỗn hợp A .
Ở điều kiện tiêu chuẩn 3,36 lít hỗn hợp khí gồm CH4 và C2H4 có khối lượng 3 gam A Tính phần trăm theo thể tích và theo khối lượng mỗi khí trong hỗn hợp B Dẫn 3,36 lít hỗn hợp khí trên qua bình chứa dung dịch brom dư thấy dung dịch Brom bị nhạt màu và khối lượng tăng thêm M gam. Tính m
a, Ta có: \(n_{CH_4}+n_{C_2H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\left(1\right)\)
\(16n_{CH_4}+28n_{C_2H_4}=3\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,1\left(mol\right)\\n_{C_2H_4}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,1.16}{3}.100\%\approx53,33\%\\\%m_{C_2H_4}\approx46,67\%\end{matrix}\right.\)
- Ở cùng điều kiện nhiệt độ và áp suất, % số mol cũng là %V.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,15}.100\%\approx66,67\%\\\%V_{C_2H_4}\approx33,33\%\end{matrix}\right.\)
b, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Có: m tăng = mC2H4 = 0,05.28 = 1,4 (g)
Đúng 1
Bình luận (0)
a) \(n_{hh}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a+b=0,15\\16a+28b=3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,05\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,15}.100\%=66,67\%\\\%V_{C_2H_4}=100\%-66,67\%=33,33\%\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,1.16}{3}.100\%=53,33\%\\\%m_{C_2H_4}=100\%-53,33\%=46,67\%\end{matrix}\right.\)
b) \(m=m_{C_2H_4}=0,05.28=1,4\left(g\right)\)
Đúng 2
Bình luận (0)
Dẫn hỗn hợp 11,2 lít gồm hai khí metan và etylen vào bình đựng 250 ml dung dịch có chứa 64 gam brom màu da cam, sau một thời gian nhận thấy dung dịch brom mất màu da cam. Tính thể tích và phần trăm thể tích mỗi khí trong hỗn hợp. Tính nồng độ mol dung dịch brom phản ứng
\(n_{Br_2}=\dfrac{64}{160}=0,4\left(mol\right)\\ n_{hh2khi}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ ChỉcóC_2H_4tácdụngvớiBr_2\\ PTHH:C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ n_{C_2H_4}=n_{Br_2}=0,4\left(mol\right)\\ \Rightarrow n_{CH_4}=0,5-0,4=0,1\left(mol\right)\\ \%Vcũnglà\%n\\ \Rightarrow\%V_{CH_4}=\dfrac{0,1}{0,5}.100=20\%;\%V_{C_2H_4}=100-20=80\%\\ CM_{Br_2}=\dfrac{0,4}{0,25}=1,6M\)
Đúng 2
Bình luận (0)
Dẫn hỗn hợp 11,2 lít gồm hai khí metan và etylen vào bình đựng 250 ml dung dịch có chứa 64 gam brom màu da cam, sau một thời gian nhận thấy dung dịch brom mất màu da cam. Tính thể tích và phần trăm thể tích mỗi khí trong hỗn hợp. Tính nồng độ mol dung dịch brom phản ứng
\(n_{Br_2}=\dfrac{64}{160}=0,4\left(mol\right)\)
\(n_{hh}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,4<----0,4
\(\rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,4}{0,5}.100\%=80\%\\\%V_{CH_4}=100\%-80\%=20\%\end{matrix}\right.\)
\(C_{M\left(Br_2\right)}=\dfrac{0,4}{0,25}=1,6M\)
Đúng 4
Bình luận (0)

















