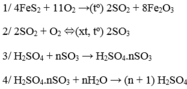Trong công nghiệp, người ta sản xuất H2SO4 theo sơ đồ sau: S -> SO2 -> SO3 -> H2SO4
a. V

Những câu hỏi liên quan
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2
→
SO2
→
SO3
→
H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là: A. 40% B. 60% C. 80% D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là:
A. 40%
B. 60%
C. 80%
D. 62,5%
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4. Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là: A. 40%. B. 60%. C. 80%. D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau:
FeS2 → SO2 → SO3 → H2SO4.
Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là:
A. 40%.
B. 60%.
C. 80%.
D. 62,5%
Đáp án C.
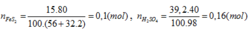
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%
Đúng 0
Bình luận (0)
II-Tự luậnAxit sunfuric là hóa chất hàng đầu được dùng trong nhiều ngành công nghiệp. Hàng năm, các nước trên thế giới sản xuất ra khoảng 160 triệu tấn. Viết PTHH sản xuất
H
2
S
O
4
từ
F
e
S
2
theo sơ đồ:
F
e
S
2
→
S
O
2
→
S
O
3...
Đọc tiếp
II-Tự luận
Axit sunfuric là hóa chất hàng đầu được dùng trong nhiều ngành công nghiệp. Hàng năm, các nước trên thế giới sản xuất ra khoảng 160 triệu tấn. Viết PTHH sản xuất H 2 S O 4 từ F e S 2 theo sơ đồ: F e S 2 → S O 2 → S O 3 → o l e u m → H 2 S O 4 .
trong công nghiệp người ta điều chế H2SO4 từ quặng pirit sắt có thành phần chính là FeS2 theo sơ đồ sau
FeS2->SO2->SO3->H2SO4
a) hoàn thành sơ đồ trên bằng các phương trình hóa học (ghi rõ điều kiện)
b) tính khối lượng H2SO4 98% điều chế được từ 1 tấn quặng chứa 60% FeS2 .Biết hiệu của cả quá trình là 80%
Xem chi tiết
a)
\(4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 4SO_2\\ 2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3\\ SO_3 + H_2O \to H_2SO_4\)
b)
\(m_{FeS_2} = 1000.60\% = 600(kg)\\ n_{FeS_2} = \dfrac{600}{120} = 5(kmol)\\ \Rightarrow n_{FeS_2\ pư} = 5.80\% = 4(kmol)\)
Bảo toàn nguyên tố với S : \(n_{H_2SO_4} = 2n_{FeS_2} = 4.2 = 8(kmol)\)
Suy ra :
\(m_{H_2SO_4} = 8.98 = 784(kg)\\ \Rightarrow m_{dd\ H_2SO_4} = \dfrac{784}{98\%} =800(kg)\)
Đúng 1
Bình luận (0)
trong công nghiệp người ta điều chế H2SO4 từ quặng pirit sắt có thành phần chính là FeS2 theo sơ đồ sau FeS2->SO2->SO3->H2SO4.tính khối lượng H2SO4 98% điều chế được từ 1 tấn quặng chứa 60% FeS2 .Biết hiệu của cả quá trình là 80%
\(m_{FeS_2}=\dfrac{1.60}{100}=0,6\left(tấn\right)\)
=> \(m_{FeS_2\left(pư\right)}=\dfrac{0,6.80}{100}=0,48\left(tấn\right)\)
Cứ 1 mol FeS2 điều chế được 2 mol H2SO4
=> 120g FeS2 điều chế được 196g H2SO4
=> 0,48 tấn FeS2 điều chế được 0,784 tấn H2SO4
=> \(m_{ddH_2SO_4}=\dfrac{0,784.100}{98}=0,8\left(tấn\right)\)
Đúng 1
Bình luận (2)
\(m_{FeS_2}=0.6\left(tấn\right)=0.6\cdot10^3\left(kg\right)\)
\(n_{FeS_2}=\dfrac{0.6\cdot10^3}{120}=\dfrac{10^3}{200}\left(kmol\right)\)
Dựa vào sơ đồ phản ứng :
\(n_{H_2SO_4}=2n_{FeS_2}=2\cdot\dfrac{10^3}{200}=\dfrac{10^3}{100}=10\left(kmol\right)\)
\(m_{H_2SO_4\left(tt\right)}=10\cdot\dfrac{98}{80\%}=1225\left(kg\right)\)
\(m_{dd_{H_2SO_4}}=\dfrac{1225}{98\%}=1250\left(kg\right)=12.5\left(tấn\right)\)
Đúng 1
Bình luận (0)
Trong công nghiệp, người ta điều chế axit sunfuric từ lưu huỳnh theo sơ đồ sau
S –> SO2 –> SO3 –> H2SO4
Tính khối lượng nguyên liệu lưu huỳnh có lẫn 5% tạp chất cần dùng để điều chế 0,1 tần dung dịch H2SO4 98%? Giả thiết tỉ lệ hao hụt cả quá trình sản xuất là 17%.
Axit sunfuric H2SO4 là một trong những hóa chất có ứng dụng hàng đầu trong đời sống như: sản xuất phân bón, thuốc trừ sâu, chất giặt rửa tổng hợp, tơ sợi hóa học, chất dẻo, sơn, dược phẩm. Trên thế giới mỗi năm người ta sản xuất khoảng 160 triệu tấn H2SO4 từ lưu huỳnh hoặc quặng pirit FeS2 theo sơ đồ sau: a. Hoàn thành sơ đồ chuyển hóa trên (ghi rõ điều kiện phản ứng nếu có) b. Trong thực tế sản xuất, để an toàn người ta không hấp thụ trực tiếp SO3 vào nước mà hấp thụ SO2 vào H2SO4 đặc để tạot...
Đọc tiếp
Axit sunfuric H2SO4 là một trong những hóa chất có ứng dụng hàng đầu trong đời sống như: sản xuất phân bón, thuốc trừ sâu, chất giặt rửa tổng hợp, tơ sợi hóa học, chất dẻo, sơn, dược phẩm. Trên thế giới mỗi năm người ta sản xuất khoảng 160 triệu tấn H2SO4 từ lưu huỳnh hoặc quặng pirit FeS2 theo sơ đồ sau:
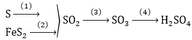
a. Hoàn thành sơ đồ chuyển hóa trên (ghi rõ điều kiện phản ứng nếu có)
b. Trong thực tế sản xuất, để an toàn người ta không hấp thụ trực tiếp SO3 vào nước mà hấp thụ SO2 vào H2SO4 đặc để tạothành Oleum (H2SO4.nSO3). Tùy theo mục đích sử dụng người ta hòa tan Oleum vào nước để thu được dung dịch H2SO4 có nồng độ theo yêu cầu. Hòa tan hoàn toàn 16,9 gam Oleum vào nước thu được 25 gam dung dịch H2SO4 78,4%. Xác định công thức của Oleum.
trong công nghiệp điều chế H2SO4 từ FeS2 theo sơ đồ sau
FeS2-->SO2-->SO3-->H2SO4
4FeS2 + 11O2\(\underrightarrow{t^o}\) 2Fe2O3 + 8SO2
2SO2 + O2 \(\xrightarrow[V_2O_5]{t^o}\) 2SO3
SO3 + H2O \(\rightarrow\) H2SO4
Đúng 0
Bình luận (0)
4FeS2 + 11O2 ---------> 2Fe2O3+ 8SO2(Đk: to)
2SO2 +O2---------->2SO3(Đk: xúc tác V2O5, >450oC)
SO3+ H2O ------->H2SO4
Đúng 0
Bình luận (0)
Sản xuất H2SO4 trong công nghiệp, người ta cho khí SO3, hấp thụ vào
A. H2O
B. dung dịch H2SO4 loãng
C. H2SO4 đặc để tạo oleum
D. HCl