CACO3->CAC+CO2
chất tham gia phản ứng là chất nào
Những câu hỏi liên quan
khi nung hợp chất CaCO3 bị phân hủy theo phản ứng sau:
CaCO3 ---> CaO +CO2.
Người ta nung 100g đá vôi chứa 90% CaCO3 còn lại là chất trơ. sau 1 thời gian, thu được 64,8 g chất rắn.
1> tính thể tích khí CO2 thoát ra<đktc>
2> tính m CaCO3 tham gia phản ứng.
3> tính khối lượng mỗi chất có trong chất rắn sau khi nung.
1) \(m_{CO_2}=m_{rắn\left(trcpư\right)}-m_{rắn\left(saupư\right)}=100-64,8=35,2\left(g\right)\)
=> \(n_{CO_2}=\dfrac{35,2}{44}=0,8\left(mol\right)\)
=> \(V_{CO_2}=0,8.22,4=17,92\left(l\right)\)
2)
PTHH: CaCO3 --to--> CaO + CO2
0,8<---------0,8<---0,8
=> \(m_{CaCO_3\left(pư\right)}=0,8.100=80\left(g\right)\)
3)
\(m_{CaCO_3\left(bd\right)}=\dfrac{100.90}{100}=90\left(g\right)\)
=> Rắn sau pư chứa CaCO3, CaO, tạp chất
\(m_{tạp.chất}=100-90=10\left(g\right)\)
\(m_{CaCO_3\left(saupư\right)}=90-80=10\left(g\right)\)
\(m_{CaO}=0,8.56=44,8\left(g\right)\)
Đúng 1
Bình luận (0)
\(1,n_{CaCO_3}=\dfrac{90\%.100}{100}=0,9\left(mol\right)\\ PTHH:CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\\ Đặt:n_{CaCO_3\left(p.ứ\right)}=a\left(mol\right)\left(a>0\right)\\ Ta.có:m_{rắn}=64,8\left(g\right)\\ \Leftrightarrow10+\left(90-100a\right)+56a=64,8\\ \Leftrightarrow a=0,8\left(mol\right)\\ n_{CO_2}=n_{CaO}=n_{CaCO_3\left(p.ứ\right)}=0,8\left(mol\right)\\ V_{CO_2\left(đktc\right)}=0,8.22,4=17,92\left(l\right)\\ 2,m_{CaCO_3\left(p.ứ\right)}=0,8.100=80\left(g\right)\\ 3,Rắn.sau.nung:m_{tạp.chất}=10\%.100=10\left(g\right)\\ m_{CaO}=0,8.56=44,8\left(g\right)\\ m_{CaCO_3\left(dư\right)}=\left(0,9-0,8\right).100=10\left(g\right)\)
Đúng 0
Bình luận (0)
khi nung hợp chất CaCO3 bị phân hủy theo phản ứng sau:
CaCO3 ---> CaO +CO2.
Người ta nung 100g đá vôi chứa 90% CaCO3 còn lại là chất trơ. sau 1 thời gian, thu được 64,8 g chất rắn.
1> tính thể tích khí CO2 thoát ra<đktc>
2> tính m CaCO3 tham gia phản ứng.
3> tính khối lượng mỗi chất có trong chất rắn sau khi nung.
1) Trong 100 g đá vôi có 90 g CaCO3 (0,9 mol).
Gọi x là số mol CO2, theo pt ta có: 64,8 = 56x + 90 - 100x hay x = 0,572 mol.
V = 0,572.22,4 = 12,829 lít.
2) m = 100x = 57,2 g.
3) mCaCO3 = 90 - 100x = 32,8 g; mCaO = 64,8 - 32,8 = 32g.
Đúng 0
Bình luận (0)
Có phương trình hóa học sau: CaCO3 → CaO + CO2. a) Cần dùng bao nhiêu mol CaCO3 để điều chế được 11,2g CaO? b) Muốn điều chế được 7g CaO cần dùng bao nhiêu gam CaCO3? c) Nếu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít CO2 (đktc). d) Nếu thu được 13,44 lít khí CO2 ở đktc thì có bao nhiêu gam chất rắn tham gia và tạo thành sau phản ứng.
Đọc tiếp
Có phương trình hóa học sau:
CaCO3 → CaO + CO2.
a) Cần dùng bao nhiêu mol CaCO3 để điều chế được 11,2g CaO?
b) Muốn điều chế được 7g CaO cần dùng bao nhiêu gam CaCO3?
c) Nếu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít CO2 (đktc).
d) Nếu thu được 13,44 lít khí CO2 ở đktc thì có bao nhiêu gam chất rắn tham gia và tạo thành sau phản ứng.
Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 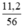 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 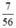 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 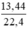 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)
Đúng 0
Bình luận (0)
Cho các chất sau: CH3-CH3 ; CH2=CH2; CH3-CH=CH2. Chất nào tham gia: a) Chất nào có liên kết đôi?
b) Chất nào tham gia phản ứng cháy?
c) Chất nào tham gia phản ứng cộng?
d) Chất nào tham gia phản ứng trùng hợp?
e) Chất nào chỉ tham gia phản ứng thế?
Biết rằng: Ethanol cháy trong không khí tạo ra khí carbon dioxide và hơi nước các chất tham gia phản ứng là cac chất nào?
Chất tham gia: ethanol \((C_2H_5OH)\) và \(O_2\)
Đúng 0
Bình luận (0)
Có phương trình hóa học sau:
CaCO3 → CaO + CO2.
a) Cần dùng bao nhiêu mol CaCO3 để điều chế được 11,2g CaO?
b) Muốn điều chế được 7g CaO cần dùng bao nhiêu gam CaCO3?
c) Nếu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít CO2 (đktc).
d) Nếu thu được 13,44 lít khí CO2 ở đktc thì có bao nhiêu gam chất rắn tham gia và tạo thành sau phản ứng.
Phương trình hóa học CaCO\(_3\) → CaO + CO\(_2\).
a) nCaO = \(\frac{11,2}{56}\) = 0,2 mol.
Theo PTHH thì nCaCO\(_3\) = nCaO = 0,2 (mol)
b) nCaO = \(\frac{7}{56}\) = 0,125 (mol)
Theo PTHH thì nCaCO\(_3\) = nCaO = 0,125 (mol)
mCaCO\(_3\) = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO\(_2\) = nCaCO\(_3\) = 3,5 (mol)
VCO\(_2\) = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO\(_2\) = \(\frac{13,44}{22,4}\) = 0,6 (mol)
Theo PTHH nCaO = nCaCO\(_3\) = nCO\(_2\) = 0,6 (mol)
mCaCO\(_3\) = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)
#shin
PTHH : CaCO3 --> Cao + CO2
a, nCaO = \(\frac{11,2}{56}=0,2\left(mol\right)\)
Theo PTHH : nCaO = nCaCO3 = 0,2 mol
Vậy : Cần dùng 0,2 mol CaCO3 để điều chế đc 11,2 g CaO
b, Mấy câu sau dễ tự làm
Xét các phản ứng sau:
1
)
C
a
C
O
3
→
C
a
O
+
C
O
2
△
H
0
2
)
2
S
O
2
(
k
)
+
O
2
(
k
)
⇌
2
S
O
3
(
k
)
;
△
H...
Đọc tiếp
Xét các phản ứng sau:
1 ) C a C O 3 → C a O + C O 2 △ H > 0 2 ) 2 S O 2 ( k ) + O 2 ( k ) ⇌ 2 S O 3 ( k ) ; △ H < 0 3 ) N 2 ( k ) + 3 H 2 ( k ) ⇋ 2 N H 3 ( k ) △ H < 0 4 ) H 2 ( k ) + I 2 ( k ) ⇋ 2 H I ( k ) ; △ H < 0
Các giải pháp hạ nhiệt độ, tăng áp suất, tăng nồng độ chất tham gia phản ứng và giảm nồng độ chất sản phẩm đều có thể làm cân bằng chuyển dịch theo chiều thuận đối với phản ứng nào?
A. 2, 3, 4
B. 2, 3
C. 4
D. 1, 4
Cho sơ đồ các phản ứng sau
a,Al+CuCl2- AlCl3+Cu
b, NaOH+H2SO4-Na2SO4+H2O
c, Cao+HCl-CaCl2+H2O
d, Ca(OH) +CO2- CaCO3+H2O
Lập các PTPƯ và cho biết số nguyên tử , số phân tử của các chất tham gia trong mỗi phản ứng
\(a.2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\)
Tỉ lệ = \(2:3:2:3\)
\(b.2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
Tỉ lệ = \(2:1:1:2\)
\(c.CaO+2HCl\rightarrow CaCl_2+H_2O\)
Tỉ lệ = \(1:2:1:1\)
\(d.Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
Tỉ lệ = \(1:1:1:1\)
Đúng 1
Bình luận (1)
a.2Al+3CuCl2→2AlCl3+3Cua.2Al+3CuCl2→2AlCl3+3Cu
b.2NaOH+H2SO4→Na2SO4+2H2Ob.2NaOH+H2SO4→Na2SO4+2H2O
c.CaO+2HCl→CaCl2+H2Oc.CaO+2HCl→CaCl2+H2O
d.Ca(OH)2+CO2→CaCO3+H2Od.Ca(OH)2+CO2→CaCO3+H2O
Đúng 1
Bình luận (0)
Nồng độ các chất tham gia phản ứng có ảnh hưởng như thế nào đến tốc độ phản ứng khi các chất sau đây tác dụng với nhau ? CaC O 3 + HCl →
CaC O 3 + 2HCl → Ca Cl 2 + H 2 O + CO 2
Khi dung dịch HCL có nồng độ càng lớn thì tốc độ phản ứng càng lớn.
Đúng 0
Bình luận (0)




















