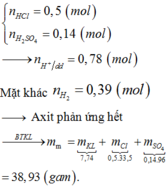Hòa tan hết 7,74 gam hỗn hợp 2 kim loại Mg và Al bằng 500ml dung dịch chứa hỗn hợp HCl 1M và H2SO4 0,28M, thu được dung dịch A và 8,736 lít khí H2. Tính tổng khối lượng muối tạo thành sau phản ứng.

Những câu hỏi liên quan
Hòa tan hết 7,74 gam hỗn hợp Mg, Al bằng 500ml dung dịch HCl 1M và H2SO4 loãng 0,28M thu được dung dịch X và 8,736 lít khí H2. Cô cạn X thu được khối lượng muối là A. 103,85 gam B. 25,95 gam C. 77,86 gam D. 38,93 gam
Đọc tiếp
Hòa tan hết 7,74 gam hỗn hợp Mg, Al bằng 500ml dung dịch HCl 1M và H2SO4 loãng 0,28M thu được dung dịch X và 8,736 lít khí H2. Cô cạn X thu được khối lượng muối là
A. 103,85 gam
B. 25,95 gam
C. 77,86 gam
D. 38,93 gam
Giải thích: Đáp án D
nH2 = 0,39 mol
nH+ = 0,5.1 + 0,28.2.0,5 = 0,78 = 2nH2
→ phản ứng vừa đủ
BTKL mmuối = mKL + maxit – mH2 = 7,74 + 0,5.1.36.5 + 0,28.0,5.98 – 0,39.2 =38,93
Đúng 1
Bình luận (0)
Bài 1: Hòa tan hết 7,74 g hỗn hợp 2 kim loại magie và nhôm bằng 500ml dung dịch chứa hai axit HCl 1M và H2SO4 0,28M thu được dung dịch A và 8,736 lít khí H2 (đktc). Viết PTHH và tính khối lượng muối khan thu được khi cô cạn dung dịch A.
\(n_{HCl}=0.5\cdot1=0.5\left(mol\right)\)
\(n_{H_2SO_4}=0.5\cdot0.28=0.14\left(mol\right)\)
\(\Rightarrow n_{H^+}=0.5+0.14\cdot2=0.75\left(mol\right)\)
\(n_{H_2}=\dfrac{8.736}{22.4}=0.39\left(mol\right)\)
\(Mg+2H^+\rightarrow Mg^{2+}+H_2\)
\(2Al+6H^+\rightarrow2Al^{3+}+3H_2\)
\(n_{H_2}>2n_{H^+}\)
=> Đề sai
Đúng 1
Bình luận (0)
Hòa tan hết 7,74 gam hỗn hợp hai kim loại magie và nhôm bằng 500ml dd chứa hai axit HCl 1M và H2SO4 0,28M thu được dung dịch A và 8,736 lít khí hiđro đo ở điều kiện tiêu chuẩn.
1/ Tính khối lượng muối khan thu được.
2/ Cho dd A phản ứng với V lít dd NaOH 2M. Tính thể tích dung dịch NaOH cần dùng để thu được kết tủa lớn nhất. Tính khối lượng kết tủa đó.
1/ nH2 = 0,39 mol; nHCl = 0,5 mol; nH2SO4 = 0,14 mol
nH+= 0,5 + 0,14.2 = 0,78 = 2nH2
=> axit phản ứng vừa đủ
Bảo toàn khối lượng: mkim loại + mHCl + mH2SO4 = mmuối khan + mH2
=> mmuối khan = 7,74 + 0,5.36,5 + 0,14.98 – 0,39.2 = 38,93 gam
2/ Đặt x, y là số mol Mg, Al
\(\left\{{}\begin{matrix}24x+27y=7,74\\x+\dfrac{3}{2}y=0,39\end{matrix}\right.\)
=> x=0,12 ; y=0,18
Để thu được kết tủa lớn nhất thì Al(OH)3 không bị tan trong NaOH
Dung dịch A : Mg2+ (0,12 mol) , Al3+ (0,18 mol)
\(Mg^{2+}+2OH^-\rightarrow Mg\left(OH\right)_2\)
\(Al^{3+}+3OH^-\rightarrow Al\left(OH\right)_3\)
=> \(n_{OH^-}=n_{NaOH}=0,12.2+0,18.3=0,78\left(mol\right)\)
=> \(V_{NaOH}=\dfrac{0,78}{2}=0,39\left(lít\right)\)
Đúng 2
Bình luận (1)
hòa tan hết 7,74 gam hỗn hợp hai lim loại magie và nhôm bằng 500ml dung dịch chứa hai axit HCl 1M và H2SO4 0,28M thu được dung A và 8,736 lít khí hidro đo ở điều kiện tiêu chuẩn.a) Tính khối lượng muối khan thu được. b) cho dung dịch A phản ứng với V lít dung dịch NaOH 2M. Tính thể tích dung dịch NaOH cần dùng để thu được kết tủa lớn nhất. Tính khối lượng của kết tủa đó.
Đọc tiếp
hòa tan hết 7,74 gam hỗn hợp hai lim loại magie và nhôm bằng 500ml dung dịch chứa hai axit HCl 1M và H2SO4 0,28M thu được dung A và 8,736 lít khí hidro đo ở điều kiện tiêu chuẩn.
a) Tính khối lượng muối khan thu được.
b) cho dung dịch A phản ứng với V lít dung dịch NaOH 2M. Tính thể tích dung dịch NaOH cần dùng để thu được kết tủa lớn nhất. Tính khối lượng của kết tủa đó.
a) \(\left\{{}\begin{matrix}n_{HCl}=0,5.1=0,5\left(mol\right)\\n_{H_2SO_4}=0,5.0,28=0,14\left(mol\right)\end{matrix}\right.\)
=> \(n_H=0,5+0,14.2=0,78\left(mol\right)\)
\(n_{H_2}=\dfrac{8,736}{22,4}=0,39\left(mol\right)\)
Do \(n_{H_2}=2.n_H\)
=> Lượng axit pư hết
BTKL: \(m_{KL}+m_{HCl}+m_{H_2SO_4}=m_{muối}+m_{H_2}\)
=> mmuối = 7,74 + 0,5.36,5 + 0,14.98 - 0,39.2
= 38,93 (g)
b)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
=> 24a + 27b = 7,74 (1)
PTHH: Mg + 2HCl --> MgCl2 + H2
Mg + H2SO4 --> MgSO4 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
=> \(n_{H_2}=n_{Mg}+1,5.n_{Al}\)
=> a + 1,5b = 0,39 (2)
(1)(2) => a = 0,12 (mol); b = 0,18 (mol)
Kết tủa lớn nhất khi Mg2+, Al3+ bị kết tủa hoàn toàn và không có sự hòa tan kết tủa
\(\left\{{}\begin{matrix}n_{Mg\left(OH\right)_2}=0,12\left(mol\right)\\n_{Al\left(OH\right)_3}=0,18\left(mol\right)\end{matrix}\right.\)
=> mkt = 0,12.58 + 0,18.78 = 21 (g)
Bảo toàn (OH): nNaOH = 0,12.2 + 0,18.3 = 0,78 (mol)
=> \(V_{dd.NaOH}=\dfrac{0,78}{2}=0,39\left(l\right)\)
Đúng 1
Bình luận (0)
Hòa tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,28M thu được dung dịch X và 8,736 lít khí H2 (ở đktc). Cô cạn dung dịch X thu được lượng muối khan là A. 38,93 gam B. 103,85 gam C. 25,95 gam D. 77,86 gam
Đọc tiếp
Hòa tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,28M thu được dung dịch X và 8,736 lít khí H2 (ở đktc). Cô cạn dung dịch X thu được lượng muối khan là
A. 38,93 gam
B. 103,85 gam
C. 25,95 gam
D. 77,86 gam
Hoà tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,28M thu được dung dịch X và 8,736 lít khí H2 (ở đktc). Cô cạn dung dịch X thu được lượng muối khan là: A. 38,93 gam. B. 103,85 gam. C. 25,95 gam. D. 77,86 gam.
Đọc tiếp
Hoà tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,28M thu được dung dịch X và 8,736 lít khí H2 (ở đktc). Cô cạn dung dịch X thu được lượng muối khan là:
A. 38,93 gam.
B. 103,85 gam.
C. 25,95 gam.
D. 77,86 gam.
Đáp án A.
Số mol của Hiđro bằng: n H 2 = 8 , 736 22 , 4 = 0 , 39 ( m o l )
Lại có n H C l = 500 1000 . 1 = 0 , 5 ( m o l ) ; n H 2 S O 4 = 500 1000 . 0 , 28 = 0 , 14 ( m o l )
Khối lượng muối tạo thành bằng: 7,74 + 0,5.36,5 + 0,14.98 – 0,39.2 = 38,93 (gam).
Đúng 0
Bình luận (0)
Hoà tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và
H
2
S
O
4
0,28M thu được dung dịch X và 8,736 lít khí
H
2
(đktc). Cô cạn dung dịch X thu được lượng muối khan là A. 38,93 gam B. 103,85 gam C. 25,95 gam D. 77,86 gam
Đọc tiếp
Hoà tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H 2 S O 4 0,28M thu được dung dịch X và 8,736 lít khí H 2 (đktc). Cô cạn dung dịch X thu được lượng muối khan là
A. 38,93 gam
B. 103,85 gam
C. 25,95 gam
D. 77,86 gam
hòa tan hết 7,74 hỗn hợp kim loại magie,nhôm bằng 500ml dung dịch chứa 2 loại axit hcl 1M và h2so4 0,28M thu được dung dich A và 8,736 lít khí hidro đo ở dktc.cho dd A phản ứng với v lít dung dịch nạoh 2M. tính thể tích naoh cần dùng để thu được kết tủa lớn nhất.tính kl kết tủa đó
\(\left\{{}\begin{matrix}n_{H_2SO_4}=0,14\left(mol\right)\\n_{HCl}=0,5\left(mol\right)\end{matrix}\right.\)
Gọi công thức chung của 2 axit là HX
=> nHX = 0,14.2 + 0,5 = 0,78 (mol)
Gọi số mol Mg, Al là a, b (mol)
\(n_{H_2}=\dfrac{8,736}{22,4}=0,39\left(mol\right)\)
PTHH: Mg + 2HX --> MgX2 + H2
a---->2a------>a---->a
2Al + 6HX --> 2AlX3 + 3H2
b--->3b------>b----->1,5b
=> \(\left\{{}\begin{matrix}24a+27b=7,74\\a+1,5b=0,39\end{matrix}\right.\)
=> a = 0,12 (mol); b = 0,18 (mol)
=> dd A chứa \(\left\{{}\begin{matrix}MgX_2:0,12\left(mol\right)\\AlX_3:0,18\left(mol\right)\end{matrix}\right.\)
PTHH: MgX2 + 2NaOH --> 2NaX + Mg(OH)2
0,12--->0,24--------------->0,12
AlX3 + 3NaOH --> 3NaX + Al(OH)3
0,18--->0,54--------------->0,18
=> \(V=\dfrac{0,24+0,54}{2}=0,39\left(l\right)\)
mkt = 0,12.58 + 0,18.78 = 21 (g)
Đúng 3
Bình luận (0)
Hòa tan hết 7,74 gam hỗn hợp 2 kim loại Mg và Al bằng 500ml dung dịch chứa hỗn hợp HCl 1M và H2SO4 0,28M, thu được dung dịch A và 8,736 lít khí H2. Tính tổng khối lượng muối tạo thành sau phản ứng.
Giúp mình nhé!
Mình cần gấp
Cảm ơn trước!
Theo bài: (PTHH bn tự viết nha....Có thể viết hoặc ko nhưng nên viết nhá:))
nHCl=0,5×1=0,5 mol
nH2SO4=0,5×0,28=0,14 mol
⇒∑nH+=0,5+0,14×2=0,78 mol
Đối với HCl và H2SO4 (loãng), H+ đóng vai trò oxi hóa.
⇒2H+ + 2e−→H2
0,78→0,39mol
⇒ H+ hết.
m muối = m kim loại + m gốc axit = 7,78 + 0,5 × 35,5 + 0,14 × 96 = 38,93 (gam)
Đúng 0
Bình luận (0)