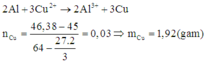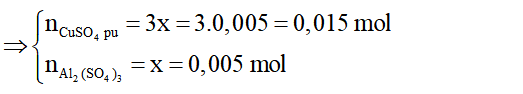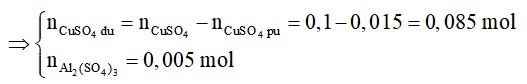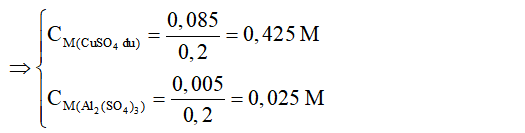Để một miếng Nhôm nặng 27 gam ngoài không khí một thời gian sau đó cân lại thấy nặng 35 gam Hãy giải thích hiện tượng trên ?

Những câu hỏi liên quan
Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch
C
u
S
O
4
0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của
C
u
S
O
4
và
A
l
2
S
O
4
trong dung dịch sau phản ứng lần lượt là...
Đọc tiếp
Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch C u S O 4 0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của C u S O 4 và A l 2 S O 4 trong dung dịch sau phản ứng lần lượt là
A. 0,425M và 0,2M
B. 0,425M và 0,3M
C. 0,4M và 0,2M
D. 0,425M và 0,025M.
n C u S O 4 = 0,5.0,2 = 0,1 mol
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
2x……3x……..x……3x (Mol)
Theo bài ta có:
m C u b á m v à o - m A l tan = m A l t ă n g
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
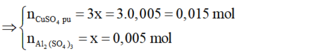

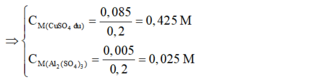
⇒ Chọn D.
Đúng 0
Bình luận (0)
Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch CuSO4 0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Tính nồng độ mol của các chất có trong dung dịch sau phản ứng.
Al: 25 gam + 0,1 mol CuSO4 → thanh nhôm nặng 25,69 gam.
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Sau phản ứng mtăng = 25,69 - 25 = 0,69 gam
=> \(n_{Al} = 2. \dfrac{0,69}{3 .64 - 2 . 27} = 0,01 mol\)
=> nAl2(SO4)3 = 0,005 mol; nCuSO4dư = 0,1 - 0,015 = 0,085 mol
=> CM Al2(SO4)3= 0,025 M; CM CuSO4 = 0,425 M
Đúng 2
Bình luận (0)
Nhúng một thanh nhôm nặng 45 gam vào 400 ml dung dịch C u S O 4 0,5M. Sau một thời gian lấy thanh nhôm ra cân lại thấy nặng 46,38 gam. Khối lượng Cu thoát ra là
A. 0,64 gam.
B. 1,28 gam.
C. 1,92 gam.
D. 2,56 gam.
Đáp án B
Bảo toàn ne=> 3nAl = 2nH2=> nAl = 0,1 => %mAl = 0,1.27.100%/5 = 54%
Đúng 0
Bình luận (0)
Nhúng một thanh nhôm nặng 45 gam vào 400 ml dung dịch CuSO4 0,5M. Sau một thời gian lấy thanh nhôm ra cân lại thấy nặng 46,38 gam. Khối lượng Cu thoát ra là
A. 0,64 gam
B. 1,28 gam
C. 1,92 gam
D. 2,56 gam
Đáp án : C
2Al + 3Cu2+ -> 2Al3+ + 3Cu
, x -> 1,5x -> 1,5x
=> msau - mtrước = 64.1,5x – 27x = 46,38 – 45
=> x = 0,02 mol => mCu pứ = 1,5.0,02.64 = 1,92g
Đúng 0
Bình luận (0)
Nhúng một thanh nhôm nặng 45 gam vào 400 ml dung dịch CuSO4 0,5M. Sau một thời gian lấy thanh nhôm ra cân lại thấy nặng 46,38 gam. Khối lượng Cu thoát ra là A. 0,64 gam B. 1,28 gam C. 1,92 gam D. 2,56 gam
Đọc tiếp
Nhúng một thanh nhôm nặng 45 gam vào 400 ml dung dịch CuSO4 0,5M. Sau một thời gian lấy thanh nhôm ra cân lại thấy nặng 46,38 gam. Khối lượng Cu thoát ra là
A. 0,64 gam
B. 1,28 gam
C. 1,92 gam
D. 2,56 gam
Chọn C
2Al + 3Cu2+ → 2Al3+ + 3Cu
x → 1,5x
Ta có ∆m = mCu – mAl ⇒ 46,38 – 45 = 64.1,5x – 27x ⇒ x = 0,02
⇒ mCu = 64.1,5.0,02 = 1,92g
Đúng 0
Bình luận (0)
Nhúng 1 thanh nhôm nặng 45 gam vào 400ml dung dịch CuSO4 0,5M. Sau một thời gian lấy thanh nhôm ra cân lại thấy nặng 46,38 gam. Khối lượng Cu thoát ra là: A. 0,64 gam. B. 1,28 gam. C. 1,92 gam. D. 2,56 gam.
Đọc tiếp
Nhúng 1 thanh nhôm nặng 45 gam vào 400ml dung dịch CuSO4 0,5M. Sau một thời gian lấy thanh nhôm ra cân lại thấy nặng 46,38 gam. Khối lượng Cu thoát ra là:
A. 0,64 gam.
B. 1,28 gam.
C. 1,92 gam.
D. 2,56 gam.
Bài 2: Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch CuSO4 0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của CuSO4 và Al2 (SO4)3 trong dung dịch sau phản ứng lần lượt là?
\(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\\ Đặt:n_{Al\left(pứ\right)}=x\left(mol\right)\\ m_{tăng}=m_{Cu\left(sinhra\right)}-m_{Al\left(pứ\right)}=\dfrac{3}{2}x.64-x.27=25,69-25\\ \Rightarrow x=0,01\left(mol\right)\\ \Rightarrow n_{CuSO_4\left(dư\right)}=0,2.0,5-0,01.\dfrac{3}{2}=0,085\left(mol\right)\\ n_{Al_2\left(SO_4\right)_3}=0,01\left(mol\right)\\ CM_{Al_2\left(SO_4\right)_3}=\dfrac{0,01}{0,2}=0,05\left(M\right)\\ CM_{CuSO_4\left(dư\right)}=\dfrac{0,085}{0,2}=0,475M\)
Đúng 3
Bình luận (0)
nCuSO4= 0,5.0,2 = 0,1 mol
2Al+3CuSO4→Al2(SO4)3+3Cu
2x……3x……..x……3x (Mol)
Theo bài ta có:
mCu bámvào−mAl tan=mAl tăng
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
*Tham khảo
Đúng 4
Bình luận (2)
Để 3,24 gam kim loại Al ở ngoài không khí , sau một thời gian cân nặng 5,16 gam . Tính thành phần phần trăm khối lượng kim loại R đã bị oxi hóa
Áp dụng ĐLBTKL: \(m_{O_2}=5,16-3,24=1,92\left(g\right)\)
\(\Rightarrow n_{O_2}=\dfrac{1,92}{32}=0,06\left(mol\right)\)
PTHH: \(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
0,08<--0,06
\(\Rightarrow\%m_{Al\left(\text{bị oxi hóa}\right)}=\dfrac{0,08.27}{3,24}.100\%=66,67\%\)
Đúng 1
Bình luận (0)
một á sắt (iron) nặng 28g để ngoài không khí , xay ra với khí oxygen tạo ra gỉ sắt. sau một thời gian cân lại lá sắt thấy khối lượng thu được là 31,2g
viết phương trình chữ và phương trình bảo toàn khối lượng của các chất trong phản ứng trên
hãy tính khối lượng và thể tích ( 25% và 1 bar) khí oxygen đã phản ứng
Sắt + oxygen \(\rightarrow\) Gỉ sắt
Phương trình bảo toàn khối lượng :
msắt + moxygen = mgỉ sắt
=> moxygen = 31.2 - 28 = 3.2(g)
\(V_{O_2}=\dfrac{3.2}{32}\cdot24.79=2.479\left(l\right)\)
Đúng 1
Bình luận (0)