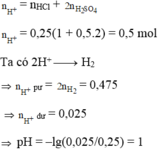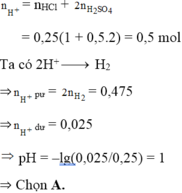cho 3 87 gam hỗn hợp gồm mg và al tác dụng với 250ml dung dịch hcl 1m và h2so4 0 5m thu được 4,368l H2 ( dktc) tính khối lượng muối tạo thành(gọi công thức chung của axit là HX)

Những câu hỏi liên quan
Cho 26,25g hỗn hợp gồm Mg và Al tác dụng vừa đủ với dung dịch HCl 10% thu được 30,8 lít H2 (đktc).
a) Tìm % khối lượng của Mg và Al có trong hỗn hợp ban đầu.
b) Tính khối lượng dung dịch HCl cần dùng.
c) Tính C% của mỗi muối tạo thành sau phản ứng.
a)
Gọi số mol Mg, Al là a, b (mol)
=> 24a + 27b = 26,25 (1)
\(n_{H_2}=\dfrac{30,8}{22,4}=1,375\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
a-->2a--------->a------>a
2Al + 6HCl --> 2AlCl3 + 3H2
b---->3b------->b------>1,5b
=> a + 1,5b = 1,375 (2)
(1)(2) => a = 0,25 (mol); b = 0,75 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,25.24}{26,25}.100\%=22,857\%\\\%m_{Al}=\dfrac{0,75.27}{26,25}.100\%=77,143\%\end{matrix}\right.\)
b)
nHCl = 2a + 3b = 2,75 (mol)
=> mHCl = 2,75.36,5 = 100,375 (g)
=> \(m_{dd.HCl}=\dfrac{100,375.100}{10}=1003,75\left(g\right)\)
c)
mdd sau pư = 1003,75 + 26,25 - 1,375.2 = 1027,25 (g)
\(\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,25.95}{1027,25}.100\%=2,312\%\\C\%_{AlCl_3}=\dfrac{0,75.133,5}{1027,25}.100\%=9,747\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Chở 3,78g hỗn hợp gồm Mg,Al vào 250ml dung dịch HCL 1M,,,H2SO4 0,5M thu đc dung dịch B và 4,368l H2 . Trung hòa dung dịch B bằng hỗn hợp NaOH 0,02M và Ba(OH)2 0,01M.cô cạn dung dịch sau phản ứng thu đc mấy g muối khan???
nH+ = 0,25 + 0,25.0,5.2 =0,5mol => 2nH2 = 0,195.2 =0,39mol
-->H+ dư =0,11 mol
Mg + 2H+ ---> Mg2+ + H2
Al + 3H+ ---> Al3+ + 3/2H2
Đặt x,y là số mol Mg ,Al --> { 24x+ 27y =3,87 ; x+3/2y =0,195}
--> x=0,06,y=0,09 --> %
b) CMH+ dư : 0,11/0,25 =0,44 M --> pH = -logH+ = 0,356
c) Mg2+ + 2OH- ---> Mg(OH)2
Al3+ + 3OH- ---> Al(OH)3
Al(OH)3 + OH- --->AlO2- + 2H2O
Ba2+ +SO42- --> BaSO4
Tổng nOH- = 0,02V + 0,01.2V =0,04V ,nOH-pu = 0,06.2 + 0,09.3 + 0,09 = 0,48mol
--> V = 0,48/0,04 =12l ,
Kết tủa : BaSO4 , Mg(OH)2
mkết tủa = 0,06.58+0,12.233=31,44g
Anh làm hơi vội nên trình bày không đẹp lắm.Thông cảm nha!!1
Đúng 0
Bình luận (0)
Cho hỗn hợp Mg, Al tác dụng vừa đủ với dung dịch HCl 1M thu được dung dịch X chứa 38,1 gam muối clorua và 9,408 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu?
cho 11g một hỗn hợp gồm Fe và Al tác dụng vừa đủ với 200ml dung dịch axit H2SO4 2(M), thì thu được V lit khí H2 (dktc)
a) xác định thành phần % về khối lượng của mỗi kim loại trong hỗn hợp đầu
b) tìm V
c) tính nồng độ các muối trong dung dịch sau phản ứng
\(n_{H_2SO_4}=0,2.2=0,4\left(mol\right)\)
Fe + H2SO4 → FeSO4 + H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Gọi x,y lần lượt là số mol Fe, Al
\(\left\{{}\begin{matrix}56x+27y=11\\x+\dfrac{3}{2}y=0,4\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=>\(\%m_{Fe}=\dfrac{0,1.56}{11}.100=50,91\%\)
=> %m Al = 100 - 50,91 =49,09 %
b)Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,4\left(mol\right)\)
=> \(V_{H_2}=0,4.22,4=8,96\left(l\right)\)
c) \(CM_{FeSO_4}=\dfrac{0,1}{0,2}=0,5M\)
\(CM_{Al_2\left(SO_4\right)_3}=\dfrac{\dfrac{0,2}{2}}{0,2}=0,5M\)
Đúng 3
Bình luận (0)
Để xác định thành phần phần trăm theo khối lượng của hỗn hợp A gồm Al và Fe người ta thực hiện 2 thí nghiệm sauTN1: Cho 10 gam hỗn hợp A tác dụng hết với dung dịch H2SO4 loạn dư thu được 8,96 lít khí H2 ở(Dktc)TN2: Cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư thì thu được 3,36 lít khí H2 (Dktc)Tính thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp A
Đọc tiếp
Để xác định thành phần phần trăm theo khối lượng của hỗn hợp A gồm Al và Fe người ta thực hiện 2 thí nghiệm sau
TN1: Cho 10 gam hỗn hợp A tác dụng hết với dung dịch H2SO4 loạn dư thu được 8,96 lít khí H2 ở(Dktc)
TN2: Cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư thì thu được 3,36 lít khí H2 (Dktc)
Tính thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp A
Cho 19,3 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với 200 ml dung dịch gồm HCl 2M và H2SO4 2,25M (loãng) thu được V lít khí H2 (đktc) và dung dịch B.
a) Tính thành phần phần trăm khối lượng của Al và Fe trong hỗn hợp ban đầu.
b) Tính tổng khối lượng muối có trong dung dịch B.
\(n_{Al}=a\left(mol\right)\)
\(n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=19.3\left(g\right)\left(1\right)\)
\(n_{H^+}=0.2\cdot2+0.2\cdot2.25\cdot2=1.3\left(mol\right)\)
\(2Al+6H^+\rightarrow2Al^{3+}+3H_2\)
\(Fe+2H^+\rightarrow Fe^{2+}+H_2\)
\(n_{H^+}=3a+2b=1.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.3,b=0.2\)
\(\%Al=\dfrac{0.3\cdot27}{19.3}\cdot100\%=41.96\%\)
\(\%Fe=58.04\%\)
\(b.\)
\(n_{H_2}=\dfrac{1}{2}n_{H^+}=0.65\left(mol\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=19.3+0.4\cdot36.5+0.45\cdot98-0.65\cdot2=76.7\left(g\right)\)
Đúng 4
Bình luận (4)
Cho m gam hỗn hợp Mg, Al vào 250ml dung dịch X chứa hỗn hợp axit HCl 1M và H2SO4 0,5M thu được 5,32 lít H2 (đktc) và dung dịch Y (coi thể tích dung dịch không đổi). Dung dịch Y có pH là: A. 1 B. 2 C. 6 D. 7
Đọc tiếp
Cho m gam hỗn hợp Mg, Al vào 250ml dung dịch X chứa hỗn hợp axit HCl 1M và H2SO4 0,5M thu được 5,32 lít H2 (đktc) và dung dịch Y (coi thể tích dung dịch không đổi). Dung dịch Y có pH là:
A. 1
B. 2
C. 6
D. 7
Cho m gam hỗn hợp Mg, Al vào 250ml dung dịch X chứa hỗn hợp axit HCl 1M và H2SO4 0,5M thu được 5,32 lít H2 (đktc) và dung dịch Y (coi thể tích dung dịch không đổi). Dung dịch Y có pH là: A. 1. B. 2. C. 6. D. 7.
Đọc tiếp
Cho m gam hỗn hợp Mg, Al vào 250ml dung dịch X chứa hỗn hợp axit HCl 1M và H2SO4 0,5M thu được 5,32 lít H2 (đktc) và dung dịch Y (coi thể tích dung dịch không đổi). Dung dịch Y có pH là:
A. 1.
B. 2.
C. 6.
D. 7.
Lấy 10,3g gam hỗn hợp gồm Al và Mg trong dung dịch H2SO4 loãng dư thu được 11,2 lít khí H2 (đktc) tính khối lượng muối sunfat tạo thành 9 (áp dụng định luật bảo toàn khối lượng)
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$Mg + H_2SO_4 \to MgSO_4 + H_2$
Theo PTHH :
$n_{H_2SO_4\ pư} = n_{H_2} = \dfrac{11,2}{22,4} = 0,5(mol)$
Bảo toàn khối lượng :
$m_{muối} = 10,3 + 0,5.98 - 0,5.2 = 58,3(gam)$
Đúng 2
Bình luận (0)