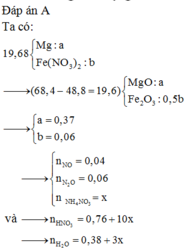Trong quá trình chuyển đổi muối tan Ba(NO3)2 thành phần muối BaSO4 thấy khối lượng 2 muối khác nhau là 8,4g. Tìm khối lượng của mỗi muối.

Những câu hỏi liên quan
trong quá trình chuyển hóa muối tan Ba(No3)2 thành muối ko tan BaSo4 thấy khối lượng 2 muối khác nhau 8,4 g . Tính khối lượng mỗi muối đó
Bạn có thể ghi đề rõ hơn không,''thấy khối lượng 2 muối khác nhau 8,4(g)'' là sao?
Đúng 0
Bình luận (0)
Trong quá trình chuyển hóa muối tan Ba(NO3)2 thành kết tủa Ba3(PO4)2 thấy khối lượng 2 muối khác nhau 9,1 g. Khối lượng mỗi muối tương ứng
X,Y là 2 oxit của kim loại A chưa rõ hóa trị. Hòa tan một lượng oxit X như nhau đến hoàn toàn trong dung dịch HCl, HNO3 rồi cô cạn dung dịch sau phản ứng thì thu được muối (=NO3),(-HCl) của kim loại A ngoài ra khối lượng muối NO3 lớn hơn khối lượng muối Cl một lượng bằng 99,33% khối lượng oxit đem hòa tan trong mỗi axit và phân tử khối của Y bằng 45% phân tử khối của X. Xác định, X,Y
X,Y là 2 oxit của kim loại A chưa rõ hóa trị. Hòa tan một lượng oxit X như nhau đến hoàn toàn trong dung dịch HCl, HNO3 rồi cô cạn dung dịch sau phản ứng thì thu được muối (=NO3),(-HCl) của kim loại A ngoài ra khối lượng muối NO3 lớn hơn khối lượng muối Cl một lượng bằng 99,33% khối lượng oxit đem hòa tan trong mỗi axit và phân tử khối của Y bằng 45% phân tử khối của X. Xác định, X,Y
X,Y là 2 oxit của kim loại A chưa rõ hóa trị. Hòa tan một lượng oxit X như nhau đến hoàn toàn trong dung dịch HCl, HNO3 rồi cô cạn dung dịch sau phản ứng thì thu được muối (NO3),(-HCl) của kim loại A ngoài ra khối lượng muối NO3 lớn hơn khối lượng muối Cl một lượng bằng 99,33% khối lượng oxit đem hòa tan trong mỗi axit và phân tử khối của Y bằng 45% phân tử khối của X. Xác định, X,Y
Đọc tiếp
X,Y là 2 oxit của kim loại A chưa rõ hóa trị. Hòa tan một lượng oxit X như nhau đến hoàn toàn trong dung dịch HCl, HNO3 rồi cô cạn dung dịch sau phản ứng thì thu được muối (=NO3),(-HCl) của kim loại A ngoài ra khối lượng muối NO3 lớn hơn khối lượng muối Cl một lượng bằng 99,33% khối lượng oxit đem hòa tan trong mỗi axit và phân tử khối của Y bằng 45% phân tử khối của X. Xác định, X,Y
bài 1: trong 28 lít nước biển có 1 kg muối, trong đó 85% là muối ăn NaCl. tính khối lượng muối ăn có trong nước biển, biết khối lượng riêng của nước biển là 1,03g/mlbài 2: chia 9,6 gam kim loại M có hoá trị II thành 2 phần bằng nhau:- hoà tan phần 1 vào dung dịch chứa 9,125 gam HCl thì sau phản ứng thấy còn kim loại M không hoà tan hết- hoà tan phần 2 vào dung dịch chứa lượng HCl gấp đôi lượng HCl ở phần 1 thì sau phản ứng thấy hoà tan hết, không còn kim loại Ma) xác định Mb) tính thể tích H2 th...
Đọc tiếp
bài 1: trong 28 lít nước biển có 1 kg muối, trong đó 85% là muối ăn NaCl. tính khối lượng muối ăn có trong nước biển, biết khối lượng riêng của nước biển là 1,03g/ml
bài 2: chia 9,6 gam kim loại M có hoá trị II thành 2 phần bằng nhau:
- hoà tan phần 1 vào dung dịch chứa 9,125 gam HCl thì sau phản ứng thấy còn kim loại M không hoà tan hết
- hoà tan phần 2 vào dung dịch chứa lượng HCl gấp đôi lượng HCl ở phần 1 thì sau phản ứng thấy hoà tan hết, không còn kim loại M
a) xác định M
b) tính thể tích H2 thu được ở phần 2
Hòa tan hết 19,68 gam hỗn hợp gồm Mg và Fe(NO3)2 trong dung dịch chứa HNO3 25,2%, thu được dung dịch X chỉ chứa các muối có tổng khối lượng 68,4 gam và 2,24 lít (đktc) hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu ngoài không khí. Tỷ khối của Y so với He là 9,6. Thu toàn bộ lượng muối trong X cho vào bình chân không nung đến khối lượng không đổi thấy khối lượng chất rắn giảm 48,8 gam. Giả sử nước bay hơi không đáng kể. Nồng độ phần trăm của muối Fe(NO3)3 có trong dung dịch X...
Đọc tiếp
Hòa tan hết 19,68 gam hỗn hợp gồm Mg và Fe(NO3)2 trong dung dịch chứa HNO3 25,2%, thu được dung dịch X chỉ chứa các muối có tổng khối lượng 68,4 gam và 2,24 lít (đktc) hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu ngoài không khí. Tỷ khối của Y so với He là 9,6. Thu toàn bộ lượng muối trong X cho vào bình chân không nung đến khối lượng không đổi thấy khối lượng chất rắn giảm 48,8 gam. Giả sử nước bay hơi không đáng kể. Nồng độ phần trăm của muối Fe(NO3)3 có trong dung dịch X là
A. 1,89%
B. 2,31%
C. 3,09%
D. 1,68%
Hòa tan 6 gam hỗn hợp hai muối MgCO3 và MgSO4 bằng dung dịch H2SO4 vừa đủ thì thu được 0,672 lít khí CO2 (đktc).
a.Viết phương trình hóa học xảy ra.
b.Tính thành phần phần trăm theo khối lượng của mỗi muối trong hỗn hợp ban đầu.
C .Tính khối lượng muối MgSO4 thu được sau phản ứng.
Ta có: \(n_{CO_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
a. PTHH:
\(MgCO_3+H_2SO_4--->MgSO_4+H_2O+CO_2\)
\(MgSO_4+H_2SO_4--\times-->\)
b. Theo PT: \(n_{MgCO_3}=n_{CO_2}=0,03\left(mol\right)\)
\(\Rightarrow m_{MgCO_3}=0,03.84=2,52\left(g\right)\)
\(\Rightarrow m_{MgSO_4}=6-2,52=3,48\left(g\right)\)
\(\Rightarrow\%_{m_{MgCO_3}}=\dfrac{2,52}{6}.100\%=42\%\)
\(\%_{m_{MgSO_4}}=100\%-42\%=58\%\)
c. Theo PT: \(n_{MgSO_4}=n_{CO_2}=0,03\left(mol\right)\)
\(\Rightarrow m_{MgSO_4}=0,03.120=3,6\left(g\right)\)
\(\Rightarrow m_{MgSO_{4_{thu.được.sau.phản.ứng}}}=3,6+3,48=7,08\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan 3,82 hỗn hợp hai muối sunfat của hai kim loại A, B có hóa trị tương ứng là I và II vào H2O, sau đó thêm BaCl2 vào thu được 6,99 g BaSO4.
a, Tính khối lượng muối clorua thu được.
b, Xác định 2 kim loại và khối lượng mỗi muối trong hỗn hợp ban đầu.
- Gọi công thức chung của hai muối là : \(M_2\left(SO_4\right)_n\)
\(PTHH:M_2\left(SO_4\right)_n+nBaCl_2\rightarrow nBaSO_4+2MCl_n\)
................0,03/n..................................0,03................
\(\Rightarrow\dfrac{0,03}{n}=\dfrac{3,82}{2M+96n}\)
\(\Rightarrow M=\dfrac{47}{3}n\)
Mà \(1< n< 2\)
\(\Rightarrow\dfrac{47}{3}< \dfrac{47}{3}n< \dfrac{94}{3}\)
\(\Rightarrow\dfrac{47}{3}< M< \dfrac{94}{3}\)
Nên A và B có thể là : Na và Mg .
- Gọi Na2SO4 và MgSO4 có mol là a, b .
b, \(BT_{SO_4^{-2}}=a+b=0,03\)
\(PTKL:142a+120b=3,82\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,01\\b=0,02\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Na2SO4}=1,42g\\m_{MgSO4}=2,4g\end{matrix}\right.\)
a, \(m_{MCl}=m_{NaCl}+m_{MaCl2}=2,485g\)
Đúng 2
Bình luận (0)
Câu b á thiếu dữ kiện nhe (mk bổ sung thêm là 2 kl này phải cùng vị trị chu kì )
a) PTHH: A2SO4+BaCl2 \(\rightarrow\) 2ACl+BaSO4
BSO4+BaCl2 \(\rightarrow\) BCl2+BaSO4
nBaCl2 = nBaSO4 = \(\dfrac{6.99}{233}\) = 0,03mol
\(\Rightarrow\)mBaCl2 = 0,03.208 = 6,24g.
b)mhh =3,82g
nSO4(2-)=0,03mol
-Nếu hh chỉ có A2SO4, MA2SO4\(=\dfrac{3,82}{0,03}=127,33\rightarrow M_A=15,67\)
-Nếu hh chỉ có BSO4, MBSO4\(=\dfrac{3,82}{0,03}=127,33\rightarrow M_B=31,33\)
Mà hh có cả A2SO4 và BSO4 nên
15,67 Mà A,B ở cùng chu kỳ nên A là Na (23) và B là Mg (24)
Đúng 0
Bình luận (0)