so sánh thể tích khí hidro (cùng điều kiện t* và p) thu được trong trường hợp sau
a) 1 mol Fe tác dụng với dung dịch H2SO4 loãng vừa đủ
b) 1 mol Zn tác dụng với dung dịch H2SO4 loãng vừa đủ
So sánh thể tích khí hidro ( đktc) thu được trong mỗi trường hợp sau:
0,1 mol Zn tác dụng với dung dịch H 2 S O 4 loãng, dư.
0,1 mol Al tác dụng với dung dịch H 2 S O 4 loãng, dư
So sánh thể tích khí hiđro (cùng điều kiện t ° và p) thu được của từng cặp phản ứng trong những thí nghiệm sau :
Thí nghiệm 1:
0,1 mol Zn tác dụng với dung dịch HCl dư.
0,1 mol Zn tác dụng với dung dịch H 2 SO 4 dư.
Thí nghiệm 2 :
0,1 mol H 2 SO 4 tác dụng với Zn dư.
0,1 mol HCl tác dụng với Zn dư.
So sánh thể tích khí hiđro sinh ra
TN1 : Dùng dư axit để toàn lượng Zn tham gia phản ứng.
Theo (1) : 0,1 mol Zn điều chế được 0,1 mol H 2
Theo (2) : 0,1 mol Zn điều chế được 0,1 mol H 2
Kết luận : Những thể tích khí hiđro thu được trong thí nghiệm 1 là bằng nhau.
TN 2 - Dùng dư Zn để toàn lượng axit tham gia phản ứng.
Theo (1) : 0,1 mol HCl điều chế được 0,05 mol H 2
Theo (2) : 0,1 mol H 2 SO 4 điều chế được 0,1 mol H 2
Kết luận . Những thể tích khí hiđro thu được trong thí nghiệm 2 là không bằng nhau. Thể tích khí hiđro sinh ra ở (2) nhiều gấp 2 lần ở (1).
Aminoaxit A có khả năng tác dụng với H2SO4 trong dung dịch loãng theo tỉ lệ mol tương ứng 2 : 1. Nếu lấy 1 lượng A cho tác dụng vừa đủ với 100 ml dung dịch HCl 0,25M thì thu được dung dịch B. Để trung hòa dung dịch B thì cần vừa đủ 100 ml dung dịch NaOH 1M. Mặt khác, khi đốt cháy hoàn toàn A bằng lượng vừa đủ O2 thì thấy VO2 : VCO2 : VH2O = 3,5 : 4 : 3 (đo ở cùng điều kiện). Công thức phân tử của A là ?
A. C5H9NO6
B. C6H9NO6
C. C6H9N2O6
D. C2H7NO2
1:cho 13g Zn tác dụng vừa đủ với dung dịch H2SO4 1M.
a,tính thể tích khí H thu được ở đktc
b,tính thể tích dung dịch HCL
2:cho Mg tác dụng vừa đủ với 200ml dung dịch HCL 2M
a,tính khối lượng Mg đã dùng
b,tính thể tích H thu được ở điều kiện tiêu chuẩn
1:
a) \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
______0,2------>0,2------------------->0,2_____(mol)
=> \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b) \(V_{ddH_2SO_4}=\dfrac{0,2}{1}=0,2\left(l\right)\)
2:
a)
\(n_{HCl}=2.0,2=0,4\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
______0,2<------0,4------------------>0,2______(mol)
=> \(m_{Mg}=0,2.24=4,8\left(g\right)\)
b) \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Bài 3 :Cho 11,2 gam sắt tác dụng vừa đủ với 400 ml dung dịch H2SO4. Sau phản ứng thu được muối FeSO4 và khí hidro bay lên.
a) Viết PTHH xảy ra.
b) Tính thể tích khí hidro sinh ra ở điều kiện chuẩn ?
c) Tính nồng độ mol / lít của dung dịch H2SO4 đã dùng ?
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\a, PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ b,n_{H_2}=n_{H_2SO_4}=n_{Fe}=0,2\left(mol\right)\\ V_{H_2\left(đkc\right)}=0,2.24,79=4,958\left(l\right)\\ c,C_{MddH_2SO_4}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
Cho 5,6 gam Fe tác dụng vừa đủ với 100 ml dung dịch H2SO4, thu được FeSO4 và khí hidro.
a) Viết PTHH
b) Tính nồng độ mol dung dịch H2SO4
c) Tính thể tích khí hidro ở đktc
Fe+H2SO4->FeSO4+H2
0,1---0,1--------0,1-------0,1
n Fe=0,1 mol
CMH2SO4=\(\dfrac{0,1}{0,1}=1M\)
=>VH2=0,1.22,4=2,24l
Hỗn hợp X gồm Fe2O3 và Cu. Cho m gam hỗn hợp X tác dụng với dung dịch HCl vừa đủ thu được dung dịch chứa 122,76 gam chất tan. Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 loãng vừa đủ thu được dung dịch Y chứa 3 chất tan với tỉ lệ số mol 1 : 2 : 3. Dung dịch Y làm mất màu tối đa bao nhiêu gam KMnO4 trong môi trường axit sunfuric?
A. 6,162
B. 6,004.
C. 5,846.
D. 5,688
Chọn đáp án D
Xét thí nghiệm 2: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4 → n C u S O 4 : n F e S O 4 = 1 : 2 .
⇒ n C u S O 4 : n F e S O 4 : n F e 2 ( S O 4 ) 3 = 1 : 2 : 3 .
Đặt n C u S O 4 = x mol ⇒ n F e S O 4 = 2x mol và n F e 2 ( S O 4 ) 3 = 3x mol.
⇒ n C u 2 + = x mol; n F e 2 + = 2x mol; n F e 3 + = 6x mol
⇒ n C u C l 2 = x mol; n F e C l 2 = 2x mol; n F e C l 3 = 6x mol.
⇒ mchất tan = 135x + 127 × 2x + 162,5 × 6x = 122,76 gam ⇒ x = 0,09 mol.
⇒ Y chứa 0,18 mol FeSO4. Bảo toàn electron: 5 n K M n O 4 = n F e S O 4 .
![]()
![]()
Hỗn hợp X gồm Fe2O3 và Cu. Cho m gam hỗn hợp X tác dụng với dung dịch HCl vừa đủ thu được dung dịch chứa 122,76 gam chất tan. Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 loãng vừa đủ thu được dung dịch Y chứa 3 chất tan với tỉ lệ số mol 1 : 2 : 3. Dung dịch Y làm mất màu tối đa bao nhiêu gam KMnO4 trong môi trường axit sunfuric?
A. 6,162.
B. 6,004.
C. 5,846.
D. 5,688.
Xét thí nghiệm 2: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
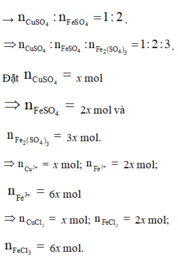
mchất tan = 135x + 127 × 2x + 162,5 × 6x = 122,76 gam ⇒ x = 0,09 mol.
Y chứa 0,18 mol FeSO4. Bảo toàn electron:
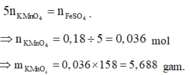
Đáp án D
Hỗn hợp X gồm Fe2O3 và Cu. Cho m gam hỗn hơp X tác dụng với dung dịch HCl vừa đủ thu được dung dịch chứa 122,76 gam chất tan. Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 loãng vừa đủ thu được dung dịch Y chứa 3 chất tan với tỉ lệ số mol 1 : 2 : 3. Dung dịch Y làm mất màu tối đa bao nhiêu gam KMnO4 trong môi trường axit sunfuric?
A. 6,162
B. 5,846
C. 5,688
D. 6,004