.Xác định công thức phân tử của CuxOy, biết tỉ lệ khối lượng giữa đồng và oxi trong oxit là 4 : 1. Viết phương trình phản ứng điều chế đồng và đồng sunfat từ CuxOy (các hóa chất khác tự chọn).

Những câu hỏi liên quan
xác định công thức phân tử của CuxOy, biết tỉ lệ khối lượng giữa đồng và oxi trong oxit là 4:1 . viết phương trình phản ứng điều chế đồng và đồng sunfat từ CuxOy (các hóa chất khác tự chọn)
Có: M(Cu) = 64x ; M(O) =16y
=> \(\frac{64x}{16y}=\frac{4}{1}\Rightarrow\frac{x}{y}=1\)
=> Công thức: CuO
Điều chế: CuO + H2 ------> Cu + H2O ( ở nhiệt độ 400oC)
Hoặc: 3CuO +2 Al ---------> Al2O3 + 3Cu
CuO + H2SO4 ---------> CuSO4 + H2O
Xác định CTHH của CuxOy, biết tỉ lệ khối lượng giữa đồng và oxi là 4:1
Ta có : CuxOy
x : y = \(\frac{m_{Cu}}{M_{Cu}}=\frac{m_O}{M_O}\)
= \(\frac{4}{64}:\frac{1}{16}\)= \(\frac{1}{1}\)
Suy ra CTHH của CuxOy là CuO
Đúng 0
Bình luận (1)
Ta có : CuxOy
x : y = \(\frac{m_{Cu}}{M_{Cu}}:\frac{m_O}{M_O}\)
= \(\frac{4}{64}:\frac{1}{16}\)= \(\frac{1}{1}\)
Suy ra CTHH của CuxOy là CuO
Đúng 0
Bình luận (0)
Xác định CTHH của CuxOy,biết tỉ lệ khối lượng giữa đồng và oxi là 4:1
- Gọi CTHH là CuxOy- Tỉ lệ :64x / 16y = 4 / 1--> 64x = 64y
--> x /y = 64/ 64 = 1 / 1
--> x= 1 ; y= 1
Vậy CTHH là CuO
--> x /y = 64/ 64 = 1 / 1
--> x= 1 ; y= 1
Vậy CTHH là CuO
Đúng 0
Bình luận (0)
Gọi CTHH của hợp chất cần tìm là \(Cu_xO_y\) Ta có:
\(m_{Cu}\) : \(m_{O_2}\) = 4:1 =80%: 20% Theo giả thiết bài cho: x : y = \(\frac{\%Cu}{M_{Cu}}\):\(\frac{\%O_2}{M_{O_2}}\)
= \(\frac{80}{64}\) : \(\frac{20}{32}\)
= 1,25: 0,625 =2:1 \(\Rightarrow\) x=2 y=1 Vậy CTHH của hợp chất cần tìm là \(Cu_2O\) **** CÓ MẤY LỖI ĐÁNH MÁY NÊN CÁC CTHH CÓ THÊM DẤU "|" Ở CUỐI![]()
Đúng 0
Bình luận (0)
1. Oxit đồng có công thức CuxOy và có mCu : mO 4 : 1. Tìm công thức oxit. 2. X là oxit của một kim loại M chưa rõ hoá trị. Biết tỉ lệ về khối lượng của M và O bằng 7:3. Xác định công thức hóa học của X? 3. Oxit cao nhất của một nguyên tố có công thức R2Ox phân tử khối của oxit là 102 đvC, biết thành phần khối lượng của oxi là 47,06%. Xác định R. ...
Đọc tiếp
1. Oxit đồng có công thức CuxOy và có mCu : mO = 4 : 1. Tìm công thức oxit.
2. X là oxit của một kim loại M chưa rõ hoá trị. Biết tỉ lệ về khối lượng của M và O bằng 7:3. Xác định công thức hóa học của X?
3. Oxit cao nhất của một nguyên tố có công thức R2Ox phân tử khối của oxit là 102 đvC, biết thành phần khối lượng của oxi là 47,06%. Xác định R.
4.Oxit kim loại R có hóa trị III. Biết trong oxit thì oxi chiếm 30% về khối lượng. Xác định CTHH của oxit
1)
Có mCu : mO = 4 : 1
=> 64.nCu : 16.nO = 4:1
=> nCu : nO = 1:1
=> CTHH: CuO
2) CTHH: MxOy
\(\dfrac{M_M.x}{16y}=\dfrac{7}{3}\)
=> \(M_M=\dfrac{112y}{3x}=\dfrac{2y}{x}.\dfrac{56}{3}\)
Xét \(\dfrac{2y}{x}=1\) => L
Xét \(\dfrac{2y}{x}=2\) => L
Xét \(\dfrac{2y}{x}=3\) => MM = 56(Fe) => \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH: Fe2O3
3)
\(m_O=\dfrac{47,06.102}{100}=48\left(g\right)=>n_O=\dfrac{48}{16}=3\left(mol\right)\)=> x = 3
=> MR2O3 = 102
=> MR = 27(Al)
4)
CTHH: R2O3
\(\dfrac{16.3}{2.M_R+16.3}.100\%=30\%=>M_R=56\left(Fe\right)\)
=> Fe2O3
Đúng 2
Bình luận (1)
Câu 9: (3,0 điểm)
a. Viết phương trình hóa học biểu diễn sự cháy của các chất sau trong khí oxi: đồng,
nhôm, lưu huỳnh, butan (C4H10)
b. Một oxit được tạo bởi 2 nguyên tố sắt và oxi trong đó tỉ lệ khối lượng giữa sắt và
oxi là 7:3. Tìm công thức phân tử của oxit đó.
a)\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(C_4H_{10}+\dfrac{13}{2}O_2\underrightarrow{t^o}4CO_2+5H_2O\)
b)Gọi CTHH là \(Fe_xO_y\)
\(x:y=\dfrac{m_{Fe}}{56}:\dfrac{m_O}{16}=\dfrac{7}{56}:\dfrac{3}{16}=0,125:0,1875=2:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\Rightarrow Fe_2O_3\)
Đúng 2
Bình luận (0)
Đốt bột sắt trong khí oxi thu được oxit sắt từ (Fe3O4).a. Viết phương trình chữ của phản ứng. b. Lập phương trình hóa học và cho biết tỉ lệ số nguyên tử, số phân tử của các chất trong mỗi phản ứng.c. Biết khối lượng sắt là 7,9 gam, khối lượng oxit sắt từ là 11,3 gam. Tính khối lượng khí oxi đã tham gia phản ứng.
Đọc tiếp
Đốt bột sắt trong khí oxi thu được oxit sắt từ (Fe3O4).
a. Viết phương trình chữ của phản ứng.
b. Lập phương trình hóa học và cho biết tỉ lệ số nguyên tử, số phân tử của các chất trong mỗi phản ứng.
c. Biết khối lượng sắt là 7,9 gam, khối lượng oxit sắt từ là 11,3 gam. Tính khối lượng khí oxi đã tham gia phản ứng.
\(a,\) Sắt + oxi ---to---> oxit sắt từ
\(b,PTHH:3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\\ \text{Tỉ lệ: }3:2:1\\ c,\text{Bảo toàn KL: }m_{Fe}+m_{O_2}=m_{Fe_3O_4}\\ \Rightarrow m_{O_2}=m_{Fe_3O_4}-m_{Fe}=11,3-7,9=3,4(g)\)
Đúng 0
Bình luận (0)
a. Sắt + Oxi \(\underrightarrow{t^0}\) Oxit Sắt từ
b. \(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\)
Tỉ lệ: \(3..........2...........1\)
c. Theo ĐLBTKL: \(m_{Fe}+m_{O_2}=m_{Fe_3O_4}\)
\(\Rightarrow m_{O_2}=m_{Fe_3O_4}-m_{Fe}=11,3-7,9=3,4\left(g\right)\)
Đúng 0
Bình luận (0)
Câu 7. Đốt bột sắt trong khí oxi thu được oxit sắt từ (Fe3O4). a. Viết phương trình chữ của phản ứng. b. Lập phương trình hóa học và cho biết tỉ lệ số nguyên tử, số phân tử của các chất trong mỗi phản ứng. c. Biết khối lượng sắt là 7,9 gam, khối lượng oxit sắt từ là 11,3 gam. Tính khối lượng khí oxi đã tham gia phản ứng.
\(a,\) Sắt + Oxi ----to----> Oxit sắt từ
\(b,3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\)
Số nguyên tử Fe : Số phân tử O2 : Số phân tử Fe3O4 \(=3:2:1\)
\(c,\) Bảo toàn KL: \(m_{Fe}+m_{O_2}=m_{Fe_3O_4}\)
\(\Rightarrow m_{O_2}=11,3-7,9=3,4(g)\)
Đúng 1
Bình luận (0)
Đốt cháy đồng và oxi phản ứng thu được 16g đồng2 oxit
a) lập phương trình hoá học của phản ứng trên
b) tính khối lượng của oxi và đồng biết tỉ lệ là 1:4
c)Nếu có 9.10^23 nguyên tử đồng tham gia phản ứng thì cần bao nhiêu phân tử khí oxi và bao nhiêu phân tử đồng 2 oxit
a) phân tử khôi của đồng oxit và đồng sunfat có tỉ lệ 1/2 . biết khối lượng phân tử CuSO4 là 160 đvC . công thức phân tử đồng oxit là:
b) phân tích một khối lượng hợp chất M , người ta nhận thấy thành phần khối lượng của nó có 50% là lưu huỳnh và 50% là oxi . công thức của hợp chất M có thể là:
Phân tử khối của Đồng ôxit và Đồng sunfat có tỉ lệ 1/2
Mà phân tử khối của đồng sunfat (CUSO4) là 160 đvC
=> Phân tử khối của đồng oxit là :
160 * 1/2 = 80 (đvC)
Do đồng oxit gồm Cu và O nêncông thức hóa học của đồng oxit có dạng CuxOy
Ta có :
PTKđồng oxit = NTKCu * x + NTKO * y
=> 80 đvC = 64 * x + 16 * y
=> x < 2 vì nếu x = 2 thì 64 * 2 > 80
=> x = 1 , khi đó :
y = ( 80 - 64*1 ) : 16 = 1
Vậy công thức hóa học của đồng oxit là CuO
b) Gọi công thức của oxit là SxOy
x : y = nS : nO =
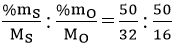
= 1,5625 : 3,125 = 1 : 2
Vậy công thức đơn giản của hợp chất M là: SO2
Đúng 4
Bình luận (0)























