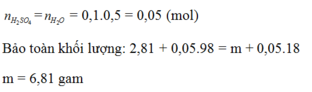Hòa tan 55g hỗn hợp X2SO3 và X2CO3 cần 500ml HCl 2M. Tính khối lượng muối khan sau phản ứng.
Các cậu giúp tớ với

Những câu hỏi liên quan
Hòa tan 55g hỗn hợp X2SO3 và X2CO3 cần 500ml HCl 2M. Tính khối lượng muối khan sau phản ứng.
...Thỉnh cao nhân, tôi giải mãi không ra
\(n_{hh}=\dfrac{nHCl}{2}=\dfrac{1}{2}=0,5\left(mol\right)\)
=> M(tb) = 55/0,5 = 110
(2X + 60 ) < 100 < (2X + 80 )
=> 15 < X < 25
=> X là Na
=> mhh muối = mNaCl = 0,5 .2 . 58,5 = 58,5 gam
Đúng 0
Bình luận (2)
Hòa tan 55g hỗn hợp gồm Na2CO3 và Na2SO3 phải dùng 250g dd HCl 14,6%. Biết phản ứng chỉ tạo muối trung hòa.
a. Tính thể tích khí thu đc sau phản ứng (đktc).
b. Tính tp % về khối lượng của mỗi chất trong hỗn hợp.
c. Tính C% sau phản ứng.
cho 200ml dd HCl 3,5M. hòa tan vừa hết 20g hỗn hợp hai oxit CuO và Fe2O3
a, tính khối lượng muối khan thu được sau phản ứng.
b, tính % theo khối lượng mỗi oxit trong hỗn hợp ban đầu.
giúp em với ạ ;-;
Đổi 200ml = 0,2 lít
Ta có: \(n_{HCl}=0,2.3,5=0,7\left(mol\right)\)
a. Gọi x, y lần lượt là số mol của CuO và Fe2O3.
PTHH:
CuO + 2HCl ---> CuCl2 + H2O (1)
Fe2O3 + 6HCl ---> 2FeCl3 + 3H2O (2)
Theo PT(1): \(n_{HCl}=2.n_{CuO}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=6.n_{Fe_2O_3}=6y\left(mol\right)\)
\(\Rightarrow2x+6y=0,7\) (*)
Mà theo đề, ta có: \(80x+160y=20\) (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+6y=0,7\\80x+160y=20\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
Theo PT(1): \(m_{CuCl_2}=n_{CuO}=0,05\left(mol\right)\)
\(\Rightarrow m_{CuCl_2}=0,05.135=6,75\left(g\right)\)
Theo PT(2): \(n_{FeCl_3}=2.n_{Fe_2O_3}=2.0,1=0,2\left(mol\right)\)
\(\Rightarrow m_{FeCl_3}=0,2.162,5=32,5\left(g\right)\)
\(\Rightarrow m_{muối.khan}=6,75+32,5=39,25\left(g\right)\)
b. Từ câu a, suy ra:
\(\%_{m_{CuO}}=\dfrac{0,05.80}{20}.100\%=20\%\)
\(\%_{m_{Fe_2O_3}}=100\%-20\%=80\%\)
Đúng 3
Bình luận (1)
Đáp án: Giải thích các bước giải: Đổi 200ml = 0,2 lít Ta có: NHCL=0,2.3,5=0,7(mol) a. Gọi x, y lần lượt là số mol của CuO và Fe2o3 PTHH: Cuo + 2HCl ---> Cucl2+ H20(1) Fe2o3+ 6HCl ---> 2Fecl3+ 3H2O (2) Theo PT(1): nHCl=2.ncuo=2x(mol) Theo PT(2): nHCL=6.nf2o3=6y(mol) ⇒2x+6y=0,7 (*) Mà theo đề, ta có: 80x+160y=20 (**) Từ (*) và (**), ta có HPT: {2x+6y=0,780x+160y=20⇔{x=0,05y=0,1 Theo PT(1): mCucl2=nCuo=0,05(mol) ⇒mCucl2=0,05.135=6,75(g) Theo PT(2): nFecl3=2.nF2o3=2.0,1=0,2(mol) ⇒mFecl3=0,2.162,5=32,5(g) ⇒m muối.khan =6,75+32,5=39,25(g) b. Từ câu a, suy ra: %mcuo=0,05.8020.100%=20% %mfe2=100%−20%=80%
Đúng 0
Bình luận (0)
200 ml = 0,2l
nHCl = 0,2 . 3,5 = 0,7 ( mol)
Đặt x = nCuO, y = nFe2O3
CuO + 2HCl \(\rightarrow\) CuCl2 + H2O
x 2x x x (mol)
Fe2O3 + 6HCl \(\rightarrow\) 2FeCl3 + 3H2O
y 6y 2y 3y (mol)
80x + 160y = 20 (1)
2x + 6y = 0,7 (2)
Từ (1) và (2)
\(\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
a) mCuCl2 = 0,05. 135 = 6,75 (g)
mFeCl3 = 2.0,1.162,5
= 0,2 . 162,5 = 32,5(g)
b) m CuO = 0,05 . 80 = 4 (g)
%m CuO = \(\dfrac{4.100\%}{20\%}\)= 20%
mFe2O3 = 20 - 4 = 16 (g)
%m Fe3O3 = 100% - 20% = 80%
Đúng 0
Bình luận (0)
hòa tan hoàn toàn 14,6g hỗn hợp gồm Zn và ZnO bằng dung dịch HCl 7,3%. cô cạn dung dịch sau phản ứng thu được 27,2g muối khan
a. tính phần trăm khối lượng mỗi chất ban đầu
b. tính khối lượng dung dịch cần dùng
a) Gọi n Zn = a(mol) ; n ZnO = b(mol)
=> 65a + 81b = 14,6(1)
$Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
n ZnCl2 = a + b = 27,2/136 = 0,2(2)
Từ (1)(2) suy ra : a = b = 0,1
%m Zn = 0,1.65/14,6 .100% = 44,52%
%m ZnO = 100% -44,52% = 55,45%
b)
n HCl = 2n Zn + 2n ZnO = 0,4(mol)
m dd HCl = 0,4.36,5/7,3% = 200(gam)
Đúng 5
Bình luận (0)
hòa tan hết 7,74 gam hỗn hợp hai lim loại magie và nhôm bằng 500ml dung dịch chứa hai axit HCl 1M và H2SO4 0,28M thu được dung A và 8,736 lít khí hidro đo ở điều kiện tiêu chuẩn.a) Tính khối lượng muối khan thu được. b) cho dung dịch A phản ứng với V lít dung dịch NaOH 2M. Tính thể tích dung dịch NaOH cần dùng để thu được kết tủa lớn nhất. Tính khối lượng của kết tủa đó.
Đọc tiếp
hòa tan hết 7,74 gam hỗn hợp hai lim loại magie và nhôm bằng 500ml dung dịch chứa hai axit HCl 1M và H2SO4 0,28M thu được dung A và 8,736 lít khí hidro đo ở điều kiện tiêu chuẩn.
a) Tính khối lượng muối khan thu được.
b) cho dung dịch A phản ứng với V lít dung dịch NaOH 2M. Tính thể tích dung dịch NaOH cần dùng để thu được kết tủa lớn nhất. Tính khối lượng của kết tủa đó.
a) \(\left\{{}\begin{matrix}n_{HCl}=0,5.1=0,5\left(mol\right)\\n_{H_2SO_4}=0,5.0,28=0,14\left(mol\right)\end{matrix}\right.\)
=> \(n_H=0,5+0,14.2=0,78\left(mol\right)\)
\(n_{H_2}=\dfrac{8,736}{22,4}=0,39\left(mol\right)\)
Do \(n_{H_2}=2.n_H\)
=> Lượng axit pư hết
BTKL: \(m_{KL}+m_{HCl}+m_{H_2SO_4}=m_{muối}+m_{H_2}\)
=> mmuối = 7,74 + 0,5.36,5 + 0,14.98 - 0,39.2
= 38,93 (g)
b)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
=> 24a + 27b = 7,74 (1)
PTHH: Mg + 2HCl --> MgCl2 + H2
Mg + H2SO4 --> MgSO4 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
=> \(n_{H_2}=n_{Mg}+1,5.n_{Al}\)
=> a + 1,5b = 0,39 (2)
(1)(2) => a = 0,12 (mol); b = 0,18 (mol)
Kết tủa lớn nhất khi Mg2+, Al3+ bị kết tủa hoàn toàn và không có sự hòa tan kết tủa
\(\left\{{}\begin{matrix}n_{Mg\left(OH\right)_2}=0,12\left(mol\right)\\n_{Al\left(OH\right)_3}=0,18\left(mol\right)\end{matrix}\right.\)
=> mkt = 0,12.58 + 0,18.78 = 21 (g)
Bảo toàn (OH): nNaOH = 0,12.2 + 0,18.3 = 0,78 (mol)
=> \(V_{dd.NaOH}=\dfrac{0,78}{2}=0,39\left(l\right)\)
Đúng 1
Bình luận (0)
Hòa tan hết 7,74 gam hỗn hợp hai kim loại magie và nhôm bằng 500ml dd chứa hai axit HCl 1M và H2SO4 0,28M thu được dung dịch A và 8,736 lít khí hiđro đo ở điều kiện tiêu chuẩn.
1/ Tính khối lượng muối khan thu được.
2/ Cho dd A phản ứng với V lít dd NaOH 2M. Tính thể tích dung dịch NaOH cần dùng để thu được kết tủa lớn nhất. Tính khối lượng kết tủa đó.
1/ nH2 = 0,39 mol; nHCl = 0,5 mol; nH2SO4 = 0,14 mol
nH+= 0,5 + 0,14.2 = 0,78 = 2nH2
=> axit phản ứng vừa đủ
Bảo toàn khối lượng: mkim loại + mHCl + mH2SO4 = mmuối khan + mH2
=> mmuối khan = 7,74 + 0,5.36,5 + 0,14.98 – 0,39.2 = 38,93 gam
2/ Đặt x, y là số mol Mg, Al
\(\left\{{}\begin{matrix}24x+27y=7,74\\x+\dfrac{3}{2}y=0,39\end{matrix}\right.\)
=> x=0,12 ; y=0,18
Để thu được kết tủa lớn nhất thì Al(OH)3 không bị tan trong NaOH
Dung dịch A : Mg2+ (0,12 mol) , Al3+ (0,18 mol)
\(Mg^{2+}+2OH^-\rightarrow Mg\left(OH\right)_2\)
\(Al^{3+}+3OH^-\rightarrow Al\left(OH\right)_3\)
=> \(n_{OH^-}=n_{NaOH}=0,12.2+0,18.3=0,78\left(mol\right)\)
=> \(V_{NaOH}=\dfrac{0,78}{2}=0,39\left(lít\right)\)
Đúng 2
Bình luận (1)
108, hòa tan hỗn hợp 2 muối XCO3 và YCO3 trong dung dịch HCl dư thấy thoát ra 10,08 lít khí(dktc). Nếu cô cạn dung dịch sau phản ứng thì thu được khối lượng muối khan nhiều hơn khối lượng hỗn hợp 2 muối khan ban đầu là bao nhiêu
\(n_{CO_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
XCO3 + 2HCl --> XCl2 + CO2 + H2O
YCO3 + 2HCl --> YCl2 + CO2 + H2O
=> nHCl = 2nCO2 = 2nH2O = 0,9 (mol)
Theo ĐLBTKL:
mhh ban đầu + mHCl = mhh sau pư + mCO2 + mH2O
=> mhh sau pư - mhh ban đầu = 0,9.36,5 - 0,45.44 - 0,45.18 = 4,95(g)
=> khối lượng muối sau phản ứng nhiều hơn khối lượng muối ban đầu là 4,95g
Đúng 2
Bình luận (0)
Hòa tan hết 11,61 gam hỗn hợp bột kim loại Mg, Al, Zn, Fe bằng 500ml dung dịch hỗn hợp axit HCl 1,5M và H2SO4 0,45M (loãng) thu được dung dịch X và 13,44 lít khí H2 (đktc). Cho rằng các axit phản ứng đồng thời với các kim loại. Tổng khối lượng muối tạo thành sau phản ứng là A. 38,935 gam B. 59,835 gam C. 38,395 gam D. 40,935 gam
Đọc tiếp
Hòa tan hết 11,61 gam hỗn hợp bột kim loại Mg, Al, Zn, Fe bằng 500ml dung dịch hỗn hợp axit HCl 1,5M và H2SO4 0,45M (loãng) thu được dung dịch X và 13,44 lít khí H2 (đktc). Cho rằng các axit phản ứng đồng thời với các kim loại. Tổng khối lượng muối tạo thành sau phản ứng là
A. 38,935 gam
B. 59,835 gam
C. 38,395 gam
D. 40,935 gam
Đáp án : B
Vì phản ứng các axit đồng thời => số mol HCl và H2SO4 phản ứng theo tỷ lệ mol giống như nồng độ mol ban đầu của chúng
=> nHCl : nH2SO4 = 1,5 : 0,45 = 10 : 3 = 10x : 3x
=> 2nH2 = nHCl + 2nH2SO4 => 1,2 mol = 10x + 2.3x
=> x = 0,075 mol
=> Trong muối có : 0,225 mol SO42- và 0,75 mol Cl- ; ion kim loại
( phản ứng hết axit)
=> mmuối = 11,61 + 0,225.96 + 0,75.35,5 = 59,835g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 2,81 gam hỗn hợp gồm Fe2O3, MgO, ZnO trong 500ml axit H2SO4 0,1M (vừa đủ). Sau phản ứng cô cạn dung dịch hỗn hợp muối sunfat khan thu được có khối lượng là:
A. 6,81 gam
B. 4,81 gam
C. 3,81 gam
D. 5,81 gam