Một dd có z mol CuSO4, cho vào dd đó 1 hh bột gồm x mol Mg và y mol Fe. Sau pư thu được chất rắn gồm 2 kim loại. Xác định mối liên hệ giữa x, y, z

Những câu hỏi liên quan
cho hh x mol Fe và y mol Al vào dd chứa z mol AgNO3 thì thu đc dd A và chất rắn B xđ mối qh giữa x y z thỏa mãn đk sao. Chất rắn B gồm 3 kl, gồm 2 kl, gồm 1 kl
Cho hỗn hợp gồm x mol Fe và y mol Al vào dung dịch chứa z mol AgNO3 thì thu được dung dịch A và rắn B xác định quan hệ giữa x y z thỏa mãn các điều kiện sau
a) rắn B gồm 3 kim loại
B)rắn B gồm 2 kim loại
C)rắn b gồm 1 Kim loại
cho m g hh x gồm mg và fe vào 50g dd cuso4 9,6% sau phản ứng thu được 2,48g răn y chứa 2 kl và dd z thêm naoh vào dd z rồi lọc kết tủa đem nung trong không khí đến khối lượng không đổi thu được 2g chất rắn .tính m và % từng kim loại tính c% các chất trong dd z
Bảo toàn Cu: `n_{Cu}=n_{CuSO_4}={50.9,6\%}/{160}=0,03(mol)`
`->m_{Cu}=0,03.64=1,92<2,48`
`->Y` chứa `Fe` dư và `Cu.`
`->m_{Fe\ du}=2,48-1,92=0,56(g)`
`Mg+CuSO_4->MgSO_4+Cu`
`Fe+CuSO_4->FeSO_4+Cu`
Đặt `n_{Mg}=x(mol);n_{Fe\ pu}=y(mol)`
Theo PT: `n_{Cu}=x+y=0,03(1)`
`MgSO_4+2NaOH->Mg(OH)_2+Na_2SO_4`
`FeSO_4+2NaOH->Fe(OH)_2+Na_2SO_4`
`Mg(OH)_2` $\xrightarrow{t^o}$ `MgO+H_2O`
`4Fe(OH)_2+O_2` $\xrightarrow{t^o}$ `2Fe_2O_3+4H_2O`
Theo PT: `n_{MgO}=x(mol);n_{Fe_2O_3}=0,5y(mol)`
`->40x+160.0,5y=2(2)`
`(1)(2)->x=0,01;y=0,02`
`->m=0,01.24+0,02.56+0,56=1,92(g)`
`\%m_{Mg}={0,01.24}/{1,92}.100\%=12,5\%`
`\%m_{Fe}=100-12,5=87,5\%`
`m_{dd\ spu}=1,92+50-2,48=49,44(g)`
`Z` gồm `MgSO_4:0,01(mol);FeSO_4:0,02(mol)`
`->C\%_{MgSO_4}={0,01.120}/{49,44}.100\%\approx 2,43\%`
`C\%_{FeSO_4}={0,02.152}/{49,44}.100\%\approx 6,15\%`
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm a mol Mg và b mol Fe vào dung dịch chứa c mol AgNO3, khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 2 muối và chất rắn Y (gồm 2 kim loại). Mối quan hệ giữa a, b, c là
Đọc tiếp
Cho hỗn hợp gồm a mol Mg và b mol Fe vào dung dịch chứa c mol AgNO3, khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 2 muối và chất rắn Y (gồm 2 kim loại). Mối quan hệ giữa a, b, c là
![]()
![]()
![]()
![]()
Cho hỗn hợp gồm a (mol) Mg và b (mol) Fe vào dung dịch chứa c (mol)
A
g
N
O
3
, khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 2 muối và chất rắn Y (gồm 2 kim loại). Mối quan hệ giữa a, b, c là
A
.
2
a
≤
c
≤
2
a
+
b
B...
Đọc tiếp
Cho hỗn hợp gồm a (mol) Mg và b (mol) Fe vào dung dịch chứa c (mol) A g N O 3 , khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 2 muối và chất rắn Y (gồm 2 kim loại). Mối quan hệ giữa a, b, c là
A . 2 a ≤ c ≤ 2 a + b
B . 2 a < c < 2 a + b
C . c ≤ 2 a + b
D . 2 a - b < c < 2 a + b
Đ á p á n B M g : a m o l F e : b m o l + A g N O 3 → A g F e + M g N O 3 2 F e N O 3 2 ⇒ M g , A g N O 3 p ư h ế t F e t h a m g i a p ư 1 p h ầ n ⇒ 2 n M g < n A g N O 3 < 2 n M g + 2 n F e ⇒ 2 a < c < 2 a + b
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm a mol Mg và b mol Fe vào dung dịch chứa c mol AgNO3, khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 2 muối và chất rắn Y (gồm 2 kim loại). Mối quan hệ giữa a, b, c là A.
c
≤
2
a
+
b
. B.
2
a
c
2
a
+
b
C. ...
Đọc tiếp
Cho hỗn hợp gồm a mol Mg và b mol Fe vào dung dịch chứa c mol AgNO3, khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 2 muối và chất rắn Y (gồm 2 kim loại). Mối quan hệ giữa a, b, c là
A. c ≤ 2 a + b .
B. 2 a < c < 2 a + b
C. 2 a - b < c < 2 a + b .
D. 2 a ≤ c ≤ 2 a + b .
Cho hỗn hợp X chứa x mol Mg và y mol Fe vào dung dịch Y chứa y mol Fe3+ và z mol Ag+. Đến phản ứng hoàn toàn thu được dung dịch Z và chất rắn E. Cho NaOH dư vào Z thu được kết tủa T, nung T trong không khí đến khối lượng không đổi thu được hỗn hợp chất rắn F chứa nhiều hơn 2 chất. Mối liên hệ giữa x, y, z là: A.
x
z
-
3
y...
Đọc tiếp
Cho hỗn hợp X chứa x mol Mg và y mol Fe vào dung dịch Y chứa y mol Fe3+ và z mol Ag+. Đến phản ứng hoàn toàn thu được dung dịch Z và chất rắn E. Cho NaOH dư vào Z thu được kết tủa T, nung T trong không khí đến khối lượng không đổi thu được hỗn hợp chất rắn F chứa nhiều hơn 2 chất. Mối liên hệ giữa x, y, z là:
A. x < z - 3 y 2
B. x ≤ z - 3 y 2
C. x < z - 2 y 2
D. x ⩽ z - 2 y 2
Hòa tan 8,9g hh X gồm 2 kim loại A và B bằng dd HCl dư thấy hh X tan hết, sau pư thu được dd Y và khí Z(đktc). Cô cạn dd Y thì thu được 23,1g chất rắn khan
a) Viết PTHH, tính thể tích khí Z
b) Thêm 50% lượng kim loại B trong X vào hh X, sau đó cũng hào tan bằng dd HCl dư thì thu được 5,6 lít Z (đktc), cô cạn dd sau pư thì thu được 27,85g chất rắn khan. Tìm kim loại A và B
a)
PTHH: 2A + 2nHCl --> 2ACln + nH2
2B + 2mHCl --> 2BClm + mH2
Gọi số mol H2 là a (mol)
=> nHCl = 2a (mol)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> 8,9 + 36,5.2a = 23,1 + 2a
=> a = 0,2 (mol)
=> VH2 = 0,2.22,4 = 4,48 (l)
b)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
=> \(n_{H_2\left(tăng\right)}=0,25-0,2=0,05\left(mol\right)\)
PTHH: 2B + 2mHCl --> 2BClm + mH2
\(\dfrac{0,1}{m}\)<------------\(\dfrac{0,1}{m}\)<---0,05
Khối lượng rắn sau pư tăng lên do có thêm BClm sinh ra
=> \(m_{BCl_m}=\dfrac{0,1}{m}\left(M_B+35,5m\right)=27,85-23,1=4,75\left(g\right)\)
=> MB = 12m (g/mol)
Xét m = 2 thỏa mãn => MB = 24 (g/mol) => B là Mg
\(n_{Mg\left(thêm\right)}=\dfrac{0,1}{m}=\dfrac{0,1}{2}=0,05\left(mol\right)\)
=> \(n_{Mg\left(bđ\right)}=0,1\left(mol\right)\)
=> \(m_A=8,9-0,1.24=6,5\left(g\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
0,1-------------------->0,1
2A + 2nHCl --> 2ACln + nH2
\(\dfrac{0,2}{n}\)<-------------------0,1
=> \(M_A=\dfrac{6,5}{\dfrac{0,2}{n}}=32,5n\left(g/mol\right)\)
Xét n = 2 thỏa mãn => MA = 65 (g/mol)
=> A là Zn
Đúng 1
Bình luận (0)
Cho 300 ml dung dịch AgNO3 vào 200 ml dd Fe(NO3)2 sau khi phản ứng kết thúc thu được 19,44 gam chất rắn và dd X trong đó số mol của Fe(NO3)3 gấp đôi số mol của Fe(NO3)2 còn dư. Dung dịch X có thể tác dụng tối đa bao nhiêu gam hỗn hợp bột kim loại gồm Al và Mg có tỉ lệ số mol tưong ứng là 1: 3? A. 11,88 g. B. 7,92 g. C. 8,91 g. D. 5,94 g.
Đọc tiếp
Cho 300 ml dung dịch AgNO3 vào 200 ml dd Fe(NO3)2 sau khi phản ứng kết thúc thu được 19,44 gam chất rắn và dd X trong đó số mol của Fe(NO3)3 gấp đôi số mol của Fe(NO3)2 còn dư. Dung dịch X có thể tác dụng tối đa bao nhiêu gam hỗn hợp bột kim loại gồm Al và Mg có tỉ lệ số mol tưong ứng là 1: 3?
A. 11,88 g.
B. 7,92 g.
C. 8,91 g.
D. 5,94 g.
Đáp án B
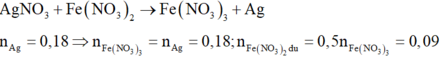
Gọi số mol Al và Mg tối đa mà dung dịch X có thể phản ứng được là x và 3x
Nên 3x + 2.3x = 0,09.2 + 0,18.3(ne cho =ne nhận)
Suy ra x = 0,08 => mAl + mMg = 7,92(g)
Đúng 0
Bình luận (0)












