Hòa tan hoàn toàn 13,7g Ba vào nước tạo thành 200ml dung dịch A
a. Tính thể tích khí đktc
b. Tính CM chất tan trong dung dịch A
c. Dẫn 3,36 lít khí CO2 đktc vào dung dịch A. Tính khối lượng chất tan thu đc
Hòa tan hoàn toàn 24,4g hỗn hợp Fe và Fe2O3 vào 800ml dung dịch HCl 1,5M thu được dung dịch A và 3,36 lít khí (đktc).
a) Tính thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp ban đầu.
b) Tính CM của các chất trong dung dịch A.
c) Để trung hòa dung dịch A cần dùng bao nhiêu ml dung dịch NaOH 1M?
mong mn giải giùm
nH2 = \(\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Fe + 2HCl ---> FeCl2 + H2
0,15 0,3 0,15 0,15
mFe = 0,15.56 = 8,4 (g)
mFe2O3 = 24,4 - 8,4 = 16 (g)
nFe2O3 = \(\dfrac{16}{160}=0,1\left(mol\right)\)
%mFe = \(\dfrac{8,4}{24,4}=34,42\%\)
%mFe2O3 = \(100\%-34,42\%=65,58\%\)
Fe2O3 + 6HCl ---> 2FeCl3 + 3H2O
0,1 0,6 0,2 0,3
nHCl (ban đầu) = 0,8.1,5 = 1,2 (mol)
nHCl (dư) = 1,2 - 0,3 - 0,6 = 0,3 (mol)
=> \(\left\{{}\begin{matrix}C_{MFeCl_3}=\dfrac{0,2+0,15}{0,8}=0,4375M\\C_{MHCl\left(dư\right)}=\dfrac{0,3}{0,8}=0,375M\end{matrix}\right.\)
PTHH:
FeCl3 + 3NaOH ---> Fe(OH)3 + 3NaCl
0,35 1,05
HCl + NaOH ---> NaCl + H2O
0,3 0,3
=> \(V_{ddNaOH}=\dfrac{1,05+0,3}{1}=1,35\left(l\right)=1350\left(ml\right)\)
Câu 3 : Hòa tan hoàn toàn 4,8g Mg vào dung dịch HCl 10,95%
a) Viết phương trình
b) Tính khối lượng dung dịch HCl cần dùng
c) Tính thể tích khí sinh ra ở đktc
d) Tính nồng độ % các chất trong dung dịch tạo thành
Câu 3 :
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
a) Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
b) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
\(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(m_{ddHCl}=\dfrac{14,6.100}{10,95}=133,3\left(g\right)\)
c) \(n_{H2}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
d) \(n_{MgCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{MgCl2}=0,2.95=19\left(g\right)\)
\(m_{ddspu}=4,8+133,3-\left(0,2.2\right)=137,7\left(g\right)\)
\(C_{MgCl2}=\dfrac{19.100}{137,7}=13,8\)0/0
Chúc bạn học tốt
Hòa tan hoàn toàn 4,8g Mg vào dung dịch HCl 10,95% a) Viết phương trình b) Tính khối lượng dung dịch HCl cần dùng c) Tính thể tích khí sinh ra ở đktc d) Tính nồng độ % các chất trong dung dịch tạo thành (Cho : Mg = 24; Cl = 35,5; H = 1
Hấp thụ hoàn toàn 3,36 lít khí C O 2 (đktc) vào 125 ml dung dịch B a ( O H ) 2 1M, thu được dung dịch X. Coi thể tích dung dịch không thay đổi, tính nồng độ mol của chất tan trong dung dịch.
Câu 4: Hợp chất B có khối lượng mol phân tử là 106g. Thành phần các nguyên tố 43,6%Na;11,3%C và 45,3%O. Hãy tìm công thức hóa học của B ?
Câu 5: Hòa tan hoàn toàn 5,6g sắt (Fe) vào dung dịch axit clohidric ( HCl) thu được sắt ( II ) clorua ( FeCl2) và khí Hidro ( H2)
a) Hãy lập phương trình hóa học xảy ra ?
b) Tính khối lượng của FeCl2 tạo thành sau phản ứng?
c) tính thể tích khí Hidro ( ở đktc) tạo thành sau phản ứng ?
Câu 6:Hòa tan 6,5g Zn bằng dung dịch H2SO4 (loãng) vừa đủ thu được dung dịch A và V lít khí (ở đktc). Tính khối lượng chất tan có trong dung dịch A ?
Mình thay trên câu a luôn nhé.
5. Số mol của Fe là :
nFe = 5,6/56 = 0,1 (mol)
a) Ta có PTHH :
Fe + 2HCl \(\rightarrow\) FeCl2 + H2\(\uparrow\)
1 mol 2 mol 1 mol 1 mol
0,1 mol 0,2 mol 0,1 mol 0,1 mol
Số mol của Fe là :
nFe = 5,6/56 = 0,1 (mol)
b) Khối lượng của FeCl2 tạo thành sau p.ứng là :
mFeCl2 = 0,1.127 = 12,7 (g)
c) Thể tích khí Hiđro (đktc) tạo thành sau p.ứng là :
VH2 = 0,1.22,4 = 2,24 (l)
4. Công thức của B là : NaxCyOz
+ \(m_{Na}=\frac{106.43,6}{100}\approx46\left(g\right)\)
\(m_C=\frac{106.11,3}{100}\approx12\left(g\right)\)
\(m_O=\frac{106.45,3}{100}\approx48\left(g\right)\)
+ \(n_{Na}=\frac{46}{23}=2\left(mol\right)\)
\(n_C=\frac{12}{12}=1\left(mol\right)\)
\(n_O=\frac{48}{16}=3\left(mol\right)\)
Suy ra trong một p.tử h/c có 2 n.tử Na, 1 n.tử C và 3 n.tử O.
\(\Rightarrow\) CTHH của hợp chất B là Na2CO3.
Hòa tan hoàn toàn 16,4 gam hỗn hợp X gồm MgO và MgCO3 trong dung dịch H2SO4. Sau phản ứng thu được dung dịch A và 2,24 lít khí CO2 (đktc)
a. Tính khối lượng mỗi chất có trong 16,4 gam hỗn hợp X
b. Cho 300 ml dung dịch Ba(OH)2 1,5M vào dung dịch A thu được 110,6 gam kết tủa và 500 ml dung dịch B. Tính nồng độ mol của các chất có trong dung dịch B
a, Ta có : \(n_{CO2}=\dfrac{V}{22,4}=0,1\left(mol\right)\)
\(BTNT\left(C\right):n_{MgCO3}=n_{CO2}=0,1\left(mol\right)\)
\(\Rightarrow m_{MgCO3}=n.M=8,4\left(g\right)\)
\(\Rightarrow m_{MgO}=8\left(g\right)\)
b, Thấy sau khi phản ứng xảy ra thu được dung dịch A gồm \(MgSO_4\) và có thể còn \(H_2SO_4\) dư .
\(BTNT\left(Mg\right):n_{MgSO_4}=n_{MgCO3}+n_{MgO}=0,3\left(mol\right)\)
\(PTHH:MgSO_4+Ba\left(OH\right)_2\rightarrow Mg\left(OH\right)_2\downarrow+BaSO_4\downarrow\)
.................0,3............0,3..................0,3..................0,3.............
\(\Rightarrow m_{\downarrow}=m_{Mg\left(OH\right)2}+m_{BaSO4}=87,3\left(g\right)\)
Mà \(\left\{{}\begin{matrix}m\downarrow=110,6\left(g\right)>87,3g\\n_{Ba\left(OH\right)2}=C_M.V=0,45>n_{Ba\left(OH\right)2pu}\left(0,3mol\right)\end{matrix}\right.\)
=> Dung dịch A vẫn còn H2SO4 dư và mol BaSO4 được tạo ra tiếp là :
\(n_{BaSO4}=\dfrac{110,6-87,3}{M}=0,1\left(mol\right)\)
\(PTHH:H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
..................0,1............0,1...............0,1........................
Lại có : \(n_{Ba\left(OH\right)2}=0,45\left(mol\right)\)
=> Trong dung dịch B còn có Ba(OH)2 dư ( dư 0,45 - 0,3 - 0,1 = 0,05mol)
\(\Rightarrow C_{MBa\left(OH\right)2}=\dfrac{n}{V}=\dfrac{0,05}{0,5}=0,1\left(M\right)\)
Vậy ...
hoà tan hoàn toàn 21,5 gam hỗn hợp K và Ba vào nước tạo thành 200ml dung dịch (c) và 4,48 lít khí (đktc)
a) %(m) K trong trong (B)
b)tính nồng độ mol từng chất tan trong (C)
c)tính tổng số mol Nhóm OH có trong (C)
PT: \(2K+2H_2O\rightarrow2KOH+H_2\)
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
a, Giả sử: \(\left\{{}\begin{matrix}n_K=x\left(mol\right)\\n_{Ba}=y\left(mol\right)\end{matrix}\right.\)
⇒ 39x + 137y = 21,5 (1)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_K+n_{Ba}=\dfrac{1}{2}x+y\left(mol\right)\)
\(\Rightarrow\dfrac{1}{2}x+y=0,2\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_K=\dfrac{0,2.39}{21,5}.100\%\approx36,28\%\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{KOH}=n_K=0,2\left(mol\right)\\n_{Ba\left(OH\right)_2}=n_{Ba}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{KOH}}=\dfrac{0,2}{0,2}=1M\\C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,1}{0,2}=0,5M\end{matrix}\right.\)
c, Ta có: \(n_{OH}=n_{KOH}+2n_{Ba\left(OH\right)_2}=0,4\left(mol\right)\)
Bạn tham khảo nhé!
đốt cháy hoàn toàn 18.6 gam photpho trong không khí được chất rắn A. Hòa tan hoàn toàn chất rắn A vào 200 gam nước được dung dịch B
a/ Tính thể tích không khí ở đktc đã cung cấp cho sự cháy
b/ tính nồng độ phần trăm chất tan trong dung dịch B
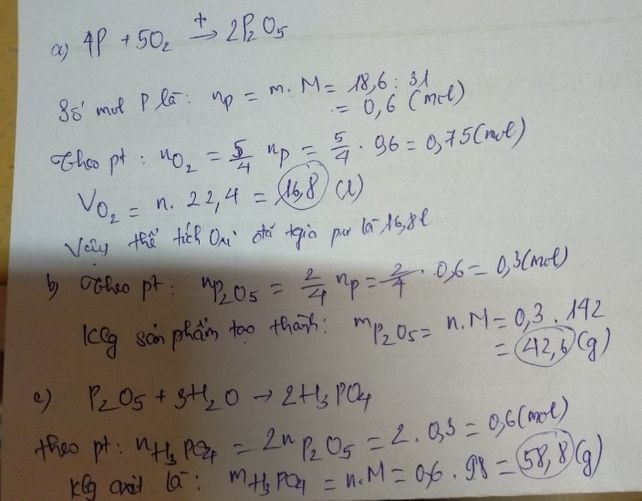
 Bạn tham khảo cách làm nhé! cho mik 1 like nha
Bạn tham khảo cách làm nhé! cho mik 1 like nha