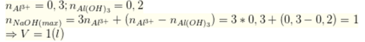cho V lít dung dịch ( ZnCl2 0.01M va ZnSO4 0.03M ) tác dụng 300ml dung dịch NaOH 0.2M thu được 0.693 gam kết tủa. Tính V.

Những câu hỏi liên quan
Cho 300ml dung dịch AlCl3 1M tác dụng vói V lít dung dịch NaOH 1M, lượng kết tủa thu được là 15,6 gam. Giá trị lớn nhất của V là A.1,0 B.0,6 C.0,9 D.1,2
Đọc tiếp
Cho 300ml dung dịch AlCl3 1M tác dụng vói V lít dung dịch NaOH 1M, lượng kết tủa thu được là 15,6 gam. Giá trị lớn nhất của V là
A.1,0
B.0,6
C.0,9
D.1,2
Đáp án A
n(Al3+) = 0,3; n(Al(OH)3) = 0,2
Giá trị V lớn nhất khi kết tủa khi NaOH hòa tan 1 phần kết tủa.
BTNT (Al): n(Al3+) = n(Al(OH)3) + n(AlO2-) => n(AlO2-) = 0,3 - 0,2 = 0,1.
BTĐT: n(AlO2-) = n(OH-) - 3n(Al3+) => n(OH-) = 0,1 + 3.0,3 = 1 mol =>V = 1 lít
Đúng 0
Bình luận (0)
Cho 300ml dung dịch AlCl3 1M tác dụng với V lít dung dịch NaOH 1M, lượng kết tủa thu được là 15,6 gam. Giá trị lớn nhất của V là
A. 1,0
B. 0,6
C. 0,9
D. 1,2
cho 1 lượng bột nhôm oxit tác dụng vừa đủ với 150ml dung dịch hcl 2M. dung dịch thu được đem tác dụng với v lít dung dịch naoh 2M thì thu được 5,85 gam kết tủa trắng dạng keo. tính v lít dung dịch naoh 0,2M đã dùng
cho 300 ml dung dịch ZnSO4 1M tác dụng với V lít dung dịch NaOH 0,5M, lượng kết tủa tu được là 19,8 gam. giá trị lớn nhất của V là?
cho 16,8 gam Fe tác dụng vừa đủ với dung dịch H2SO4 đặc nóng, thu được dung dịch A và V lít khí SO2(đktc) A) Tính V B) Cho dung dịch A tác dụng hoàn toàn với dung dịch NaOH thu được m gam kết tủa. Tính m
a, \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
BT e, có: 3nFe = 2nSO2 ⇒ nSO2 = 0,45 (mol)
⇒ VSO2 = 0,45.22,4 = 10,08 (l)
b, BTNT Fe, có: nFe(OH)3 = nFe = 0,3 (mol)
⇒ mFe(OH)3 = 0,3.107 = 32,1 (g)
Đúng 1
Bình luận (0)
Cho 300ml dung dịch NaOH 1,2M tác dụng với 100ml dung dịch ZnCl2 1,5M
a) Tính nồng độ các chất trong dung dịch thu được
b) Tính khối lượng kết tủa sau phản ứng
Hấp thụ 4.48 lít CO2 vào 0.5 lít hỗn hợp NaOH 0.4M và Ca(OH)2 0.01M thu được dung dịch X . lấy 1/2 X tác dụng với dung dịch Ba(OH)2 dư thu được m gam kết tủa và dung dịch Y . tính m và khối lượng kim loại muối khan thu được khi cô cạn Y
cho 200ml dung dịch H3PO4 tác dụng hết với 300ml dung dịch ZnCl2 2Ma, Viết PTHH xảy ra
b, Tính khối lượng kết tủa thu đc
c, Tách bỏ kết tủa. Tính nồng độ M của dung dịch thu được
PTHH 3ZnCl2+2H3PO4----->Zn3(PO4)2+6HCl
\(n_{ZnCl_2}\)=0,3.2=0,6(mol)
Theo phương trình =>\(\dfrac{1}{3}n_{ZnCl_2}=n_{Zn_3\left(PO_4\right)_2}=0,2\left(mol\right)\)
=>\(m_{Zn_3\left(PO_4\right)_2}\)=0,2.385=77(g)
Theo phương trình =>\(2n_{ZnCl_2}=n_{HCl}=1,2\left(mol\right)\)
=>\(C_{M_{HCl}}\)=\(\dfrac{1,2}{0,2+0,3}=2,4M\)
Đúng 1
Bình luận (0)
Cho 100 ml dung dịch ZnSO4 1M tác dụng với 200 ml dung dịch NaOH thu được kết tủa cực đại. Nồng độ mol/lít của dung dịch NaOH là
\(n_{ZnSO_4}=0.1\cdot1=0.1\left(mol\right)\)
\(ZnSO_4+2NaOH\rightarrow Zn\left(OH\right)_2+Na_2SO_4\)
\(0.1..............0.2\)
\(C_{M_{NaOH}}=\dfrac{0.2}{0.2}=1\left(M\right)\)
Đúng 3
Bình luận (0)