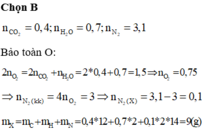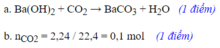Đốt cháy 16g A cần dùng 14,8l ôxi (đktc) thu được khí CO² và hơi nước theo tỉ lệ mol là ½ . Tính khối lượng khí CO² và hơi nước .

Những câu hỏi liên quan
Đốt cháy amin X với không khí (
N
2
và
O
2
với tỉ lệ mol 4:1) vừa đủ, sau phản ứng thu được 17,6 gam
C
O
2
, 12,6 gam
H
2
O
và 69,44 lít
N
2
(đktc). Khối lượng của amin là: A. 9,2 gam B. 9 gam C. 11 gam D. 9,5 gam
Đọc tiếp
Đốt cháy amin X với không khí ( N 2 và O 2 với tỉ lệ mol 4:1) vừa đủ, sau phản ứng thu được 17,6 gam C O 2 , 12,6 gam H 2 O và 69,44 lít N 2 (đktc). Khối lượng của amin là:
A. 9,2 gam
B. 9 gam
C. 11 gam
D. 9,5 gam
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan và propan được 7,84 lít CO2 (đktc) và 9,9 gam nước. Thể tích O2 (đktc) tối thiểu cần dùng là A. 8,4 lít B. 14 lít C. 15,6 lít D. 4,48 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan và propan được 7,84 lít CO2 (đktc) và 9,9 gam nước. Thể tích O2 (đktc) tối thiểu cần dùng là
A. 8,4 lít
B. 14 lít
C. 15,6 lít
D. 4,48 lít
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan và propan được 7,84 lít CO2 (đktc) và 9,9 gam nước. Thể tích O2 (đktc) tối thiểu cần dùng là A. 8,4 lít. B. 14 lít. C. 15,6 lít. D. 4,48 lít.
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan và propan được 7,84 lít CO2 (đktc) và 9,9 gam nước. Thể tích O2 (đktc) tối thiểu cần dùng là
A. 8,4 lít.
B. 14 lít.
C. 15,6 lít.
D. 4,48 lít.
Để đơn giản ta xem xăng là hỗn hợp các đồng phân của hexan và không khí gồm 80% N2 và 20% O2 (theo thể tích). Tỉ lệ thể tích xăng (hơi) và không khí cần lấy là bao nhiêu để xăng được cháy hoàn toàn trong các động cơ đốt trong ? A. 1 : 9,5 B. 1 : 47,5 C. 1 : 48 D. 1 : 50
Đọc tiếp
Để đơn giản ta xem xăng là hỗn hợp các đồng phân của hexan và không khí gồm 80% N2 và 20% O2 (theo thể tích). Tỉ lệ thể tích xăng (hơi) và không khí cần lấy là bao nhiêu để xăng được cháy hoàn toàn trong các động cơ đốt trong ?
A. 1 : 9,5
B. 1 : 47,5
C. 1 : 48
D. 1 : 50
Biết 2,24 lít khí Cacbonic (đktc) tác dụng hết với 200 ml dung dịch
B
a
(
O
H
)
2
, sản phẩm thu được là muối trung hòa và nước.a. Viết phương trình xảy ra.b. Tính nồng độ mol của dung dịch
B
a
(
O
H
)
2
cần dùng.c. Tính khối lượng kết tủa...
Đọc tiếp
Biết 2,24 lít khí Cacbonic (đktc) tác dụng hết với 200 ml dung dịch B a ( O H ) 2 , sản phẩm thu được là muối trung hòa và nước.
a. Viết phương trình xảy ra.
b. Tính nồng độ mol của dung dịch B a ( O H ) 2 cần dùng.
c. Tính khối lượng kết tủa thu được
đốt chay 5,6 lít khí, etilen trong không khí thu được khí cacbonic và hơi nước hãy tính:
a, thể tích khí cacbonic thu được
b, thể tích khí oxi cần dùng
< Các khí đều do ở ĐKT'C >
\(n_{C_2H_4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
0,25 0,75 0,5 ( mol )
\(V_{CO_2}=0,5.22,4=11,2\left(l\right)\)
\(V_{O_2}=0,75.22,4=16,8\left(l\right)\)
Đúng 1
Bình luận (0)
PTHH: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(n_{C_2H_4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PTHH: \(n_{CO_2}=2n_{C_2H_4}=2.0,25=0,5\left(mol\right)\)
=> \(V_{CO_2}=0,5.22,4=11,2\left(l\right)\)
Theo PTHH: \(n_{O_2}=3n_{C_2H_4}=3.0,25=0,75\left(mol\right)\)
=> \(V_{O_2}=0,75.22,4=16,8\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 7,45 gam hỗn hợp X gồm các axit hữu cơ (phân tử chỉ chứa một loại nhóm chức) tác dụng hết với dung dịch
NaHCO
3
dư, thấy giải phóng 3,36 lít khí
CO
2
(đktc). Mặt khác, đốt cháy hoàn toàn 7,45 gam hỗn hợp X cần dùng vừa hết 2,52 lít
O
2
(đktc), thu được sản phẩm gồm
CO...
Đọc tiếp
Cho 7,45 gam hỗn hợp X gồm các axit hữu cơ (phân tử chỉ chứa một loại nhóm chức) tác dụng hết với dung dịch NaHCO 3 dư, thấy giải phóng 3,36 lít khí CO 2 (đktc). Mặt khác, đốt cháy hoàn toàn 7,45 gam hỗn hợp X cần dùng vừa hết 2,52 lít O 2 (đktc), thu được sản phẩm gồm CO 2 và hơi nước. Dẫn toàn bộ sản phẩm cháy vào 150 ml dung dịch Ba OH 2 1M, sau khi phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch Ba OH 2
A. giảm 8,65 gam
B. giảm 19,7 gam
C. tăng 11,05 gam
D. giảm 18,5 gam
Đáp án A
Dựa vào bản chất phản ứng của X với NaHCO 3 , bảo toàn nguyên tố O; bảo toàn electron trong phản ứng đốt cháy X, ta có :
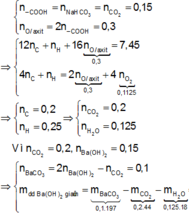
= 8,65 gam
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 62g Natri ( Na) trong không khí thu được 124g Natri oxit. Khối lượng khí oxi cần dùng là
\(n_{Na_2O}=\dfrac{124}{62}=2\left(mol\right)\)
PTHH: 4Na + O2 --to--> 2Na2O
1<----------2
=> mO2 = 1.32 = 32 (g)
Đúng 1
Bình luận (0)
Hỗn hợp khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hỗn hợp X bằng một lượng oxi vừa đủ, thu được 550 ml hỗn hợp Y gồm khí và hơi nước. Nếu cho Y đi qua dung dịch axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân tử của hai hiđrocacbon là A. C2H6 và C3H8 B. C3H6 và C4H8 C. CH4 và C2H6 D. C2H4 và C3H6
Đọc tiếp
Hỗn hợp khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hỗn hợp X bằng một lượng oxi vừa đủ, thu được 550 ml hỗn hợp Y gồm khí và hơi nước. Nếu cho Y đi qua dung dịch axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân tử của hai hiđrocacbon là
A. C2H6 và C3H8
B. C3H6 và C4H8
C. CH4 và C2H6
D. C2H4 và C3H6