Đốt cháy hoàn toàn m(g) chất hữu cơ A chưa C, H, O. Khối lượng sản phẩm cháy là p(g). Cho toàn bộ sản phẩm này qua dd nước vôi trong có dư thì thu được t(g) kết tủa, biết p=0,71t. t=(m+p)/1,02. Xác định CTPT A?

Những câu hỏi liên quan
đốt cháy hoàn toàn m (g) một hydrocacbon mạch hở T , toàn bộ sản phẩm cháy hấp thụ vào bình đựng nước vôi trong dư, sau pứ thu được 40g kết tủa trắng.
mặt khác, m (g) T pứ tối đa với 64g Br2 trong dd
biết 13< tỉ khối T/H2 < 26
Xác định CTCT của T.
Đốt cháy hoàn toàn 11,2 g khí metan, dẫn toàn bộ sản phẩm cháy qua dung dịch nước vôi trong dư. Khối lượng kết tủa thu được là (Cho H = 1; c = 12; O = 16; Ca = 40)
A. 70g
B. 40g
C. 80g
D. 50g
\(n_{CH_4}=\dfrac{11.2}{16}=0.7\left(mol\right)\)
Bảo toàn C :
\(n_{CO_2}=n_{CH_4}=0.7\left(mol\right)\)
\(m_{CaCO_3}=0.7\cdot100=70\left(g\right)\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn m gam ancol X, sản phẩm thu được cho đi qua bình đựng dung dịch nước vôi trong dư thấy khối lượng bình tăng thêm p gam và có t gam kết tủa. Biết
p
0
,
71
t
;
1
,
02
t
m
+
p
. Công thức...
Đọc tiếp
Đốt cháy hoàn toàn m gam ancol X, sản phẩm thu được cho đi qua bình đựng dung dịch nước vôi trong dư thấy khối lượng bình tăng thêm p gam và có t gam kết tủa. Biết p = 0 , 71 t ; 1 , 02 t = m + p . Công thức của X là
A. C3H5(OH)3
B. C2H5OH
C. C2H4(OH)2.
D. C3H5OH
Hỗn hợp A gồm hiđrocacbon X và chất hữu cơ Y (C, H, O) có tỉ khối so với H2 bằng 13,8. Để đốt cháy hoàn toàn 1,38 g A cần 0,095 mol O2, sản phẩm cháy thu được có 0,08 mol CO2 và 0,05 mol H2O. Cho 1,38 g A qua lượng dư AgNO3/NH3 thu được m (gam) kết tủa. Giá trị của m là A. 11,52 (g). B. 12,63 (g) C. 15,84 g D. 8,31.
Đọc tiếp
Hỗn hợp A gồm hiđrocacbon X và chất hữu cơ Y (C, H, O) có tỉ khối so với H2 bằng 13,8. Để đốt cháy hoàn toàn 1,38 g A cần 0,095 mol O2, sản phẩm cháy thu được có 0,08 mol CO2 và 0,05 mol H2O. Cho 1,38 g A qua lượng dư AgNO3/NH3 thu được m (gam) kết tủa. Giá trị của m là
A. 11,52 (g).
B. 12,63 (g)
C. 15,84 g
D. 8,31.
Đáp án C
nA = 0,05
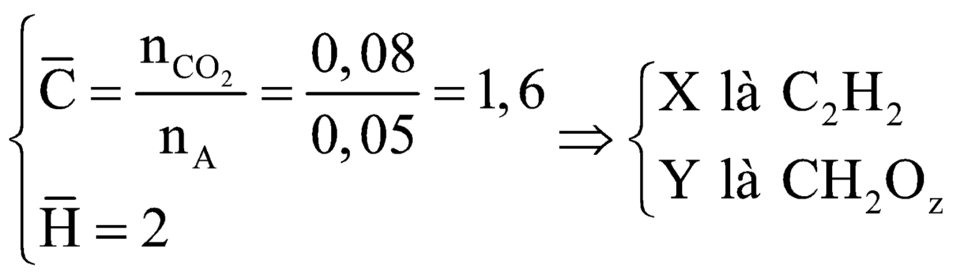
Áp dụng định luật bảo toàn nguyên tố C được:
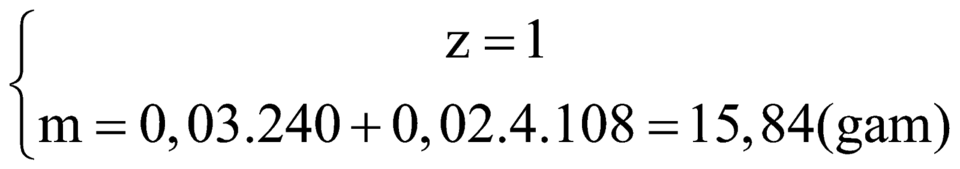
Đúng 0
Bình luận (0)
Đốt cháy m(g) hỗn hợp gồm metan , etilen . dẫn toàn bộ sản phẩm cháy và dd nước vôi trong dư thu được 50g kết tủa trắng . cùng hh trên khi dẫn vào dd br dư thì m Br phản ứng là 8g . A. viết pthh B)tính m và thành phần trăm theo khối lượng của mỗi chất ban đầu
a)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ b) n_{C_2H_4} = n_{Br_2} = \dfrac{8}{160}=0,05(mol)\\ n_{CaCO_3} = n_{CO_2} = n_{CH_4} + 2n_{C_2H_4} = \dfrac{50}{100} = 0,5(mol)\\ \Rightarrow n_{CH_4} = 0,5 - 0,05.2 = 0,4(mol)\\ \%m_{CH_4}= \dfrac{0,4.16}{0,4.16 + 0,05.28}.100\% = 82,05\%\\ \%m_{C_2H_4} =100\% - 82,05\% = 17,95\%\)
Đúng 1
Bình luận (0)
Hợp chất X có chứa C,H. Đốt cháy hoàn toàn 3,0 gam hữu cơ X và dẫn toàn bộ sản phẩm cháy vào dung dịch nước vôi trong dư, th được 30 gam kết tủa. Biết tỉ khối hơi của X so với H2 là 15 a) Xác định CTPT và CTCT của X b) Viết phương trình phản ứng của X với khí Cl2 (ánh sáng)
Đọc tiếp
Hợp chất X có chứa C,H. Đốt cháy hoàn toàn 3,0 gam hữu cơ X và dẫn toàn bộ sản phẩm cháy vào dung dịch nước vôi trong dư, th được 30 gam kết tủa. Biết tỉ khối hơi của X so với H2 là 15 a) Xác định CTPT và CTCT của X b) Viết phương trình phản ứng của X với khí Cl2 (ánh sáng)
Gọi CTHH của X là: CxHy
Theo đề, ta có:
\(d_{\dfrac{X}{H_2}}=\dfrac{M_{C_xH_y}}{M_{H_2}}=\dfrac{M_{C_xH_y}}{2}=15\left(lần\right)\)
=> \(M_{C_xH_y}=30\left(g\right)\)
a. PTHH: \(4C_xH_y+\left(4x+y\right)O_2\overset{t^o}{--->}4xCO_2+2yH_2O\) (1)
\(CO_2+Ca\left(OH\right)_2--->CaCO_3\downarrow+H_2O\) (2)
Ta có: \(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
Theo PT(2): \(n_{CO_2}=n_{CaCO_3}=0,3\left(mol\right)\)
=> \(m_{C_{\left(CO_2\right)}}=m_{C_{\left(X\right)}}=0,3.12=3,6\left(g\right)\)
(Lỗi đề thì phải bn nhé.)
Đúng 2
Bình luận (0)
Đốt cháy m(g) hỗn hợp ch4 và c2h2. Dẫn toàn bộ sản phẩm cháy vào dd nước vôi trong thu được 50g kết tủa trắng . cùng hh trên khi dẫn vào dd br dư thì m Br phản ứng là 8g . a) viết phương trình hóa học b ) tính m và thành phần trăm theo khối lượng của mỗi chất ban đầu
\(a)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ 2C_2H_2 + 5O_2 \xrightarrow{t^o} 4CO_2 + 2H_2O\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ C_2H_2 + 2Br_2 \to C_2H_2Br_4\\ b) n_{Br_2} = \dfrac{8}{160}=0,05(mol)\\ \Rightarrow n_{C_2H_2}= \dfrac{1}{2}n_{Br_2}= 0,025(mol)\\ n_{CO_2} = n_{CH_4} + 2n_{C_2H_2} = n_{CaCO_3} = \dfrac{50}{100} = 0,5(mol)\\ \Rightarrow n_{CH_4} = 0,5 - 0,025.2 = 0,45(mol)\\ \Rightarrow m = 0,45.16 + 0,05.26 = 8,5(gam)\)
\(\%m_{CH_4} = \dfrac{0,45.16}{8,5}.100\% = 84,7\%\\ \%m_{C_2H_2} = 100\% - 84,7\% = 15,3\%\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 7.4 gam hợp chất hữu cơ X ( chứa C,H,O) dẫn sản phẩm cháy qua bình đựng dung dịch nước vôi trong dư, sau phản ứng thu được 40 gam kết tủa. Thành phần % khối lượng của cacbon trong X là?
Ghi cả lời giải ra giúp mình nha
nCO2 = nCaCO3 = 40 / 100 = 0.4 (mol)
nC = nCO2 = 0.4 (mol)
mC = 0.4 * 12 = 4.8 (g)
%mC = 4.8 / 7.4 * 100% = 64.86%
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn hợp chất CxHy. Sau đó dẫn toàn bộ sản phẩm cháy vào 400ml dd Ba(OH)2 1M. Thấy có 29,55(g) kết tủa và thấy khối lượng dd giảm 17,15g. Xác định Công thức của CxHy biết M(CxHy)= 28(g/mol)
Ta có: \(n_{Ba\left(OH\right)_2}=0,4.1=0,4\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{29,55}{197}=0,15\left(mol\right)\)
TH1: Ba(OH)2 dư.
BTNT C, có: nCO2 = nBaCO3 = 0,15 (mol) = nC
Có: m dd giảm = mBaCO3 - mCO2 - mH2O ⇒ mH2O = 5,8 (g)
\(\Rightarrow n_{H_2O}=\dfrac{5,8}{18}=\dfrac{29}{90}\left(mol\right)\Rightarrow n_H=\dfrac{29}{45}\left(mol\right)\)
\(\Rightarrow x:y=0,15:\dfrac{29}{45}\approx23:100\) → vô lý
TH2: Ba(OH)2 hết.
BTNT Ba, có: nBa(HCO3)2 = 0,4 - 0,15 = 0,25 (mol)
BTNT C, có: nCO2 = 0,25.2 + 0,15 = 0,65 (mol)
Có: m dd giảm = mBaCO3 - mCO2 - mH2O ⇒ mH2O = -16,2 → vô lý
Bạn xem lại đề nhé.
Đúng 2
Bình luận (2)
















