Một oxit sắt ( FexOy ) biết trong 32g oxit thì số mol oxi là 0.6 mol. Gọi tên oxi sắt. Tks mọi người
hử hoàn toàn một oxit sắt chưa biết (FexOy) bằng nhôm thu được 0,2 mol nhôm oxit và 0,4 mol mol sắt theo sơ đồ phản ứng sau: FexOy + Al ----> Fe + Al2O3. Công thức oxit sắt là: *
$3Fe_xO_y + 2yAl \xrightarrow{t^o} 3xFe +y Al_2O_3$
Theo PTHH :
$n_{Fe} = \dfrac{3x}{y}n_{Al_2O_3}$
$\Rightarrow 0,4 = \dfrac{3x}{y}.0,2$
$\Rightarrow \dfrac{x}{y} = \dfrac{2}{3}$
Vậy oxit là $Fe_2O_3$
Đốt cháy 1 mol sắt trong oxi được 1 mol sắt oxit. Oxit sắt tạo thành là
A. F e O
B. F e 2 O 3
C. F e 3 O 4
D. k h ô n g x á c đ ị n h đ ư ợ c
Đốt cháy 1 mol sắt trong oxi, thu được 1 mol sắt oxit. Công thức oxit sắt này là:
A. FeO
B. Fe 2 O 3
C. Fe 3 O 4
D. Fe 3 O 2
Đáp án A
1mol Fe → 1 mol oxit sắt → CT có chứa 1 nguyên tử Fe
→ CT: FeO
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 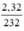 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
Một oxit của Sắt có thành phần trăm của Sắt là 70% và Oxi là 30%. Biết oxit này có khối lượng mol phân tử là 160 g/mol. Hãy tìm công thức hóa học của oxit trên.
Giải nhanh giùm mik
Khối lượng của các nguyên tố trong hợp chất là:
\(m_{FE}=\dfrac{70.160}{100}=112\left(g\right)\)
\(m_O=\dfrac{30.160}{100}=48\left(g\right)\)
Số mol có trong mỗi nguyên tố là:
\(n_{FE}=\dfrac{m_{FE}}{M_{FE}}=\dfrac{112}{56}=2\left(mol\right)\)
\(n_O=\dfrac{m_O}{M_O}=\dfrac{48}{16}=3\left(mol\right)\)
Vậy hợp chất có 2 nguyên tử Fe, 3 nguyên tử O
Công thức hóa học của hợp chất là: \(FE_2O_3\)
\(m_{Fe}=\dfrac{160.70}{100}=112g\\ m_O=160-112=48g\\ n_{Fe}=\dfrac{112}{56}=2mol\\n_O=\dfrac{48}{16}=3mol\\ \Rightarrow CTHH:Fe_2 O_3\)
gọi CT tổng quát là FexOy
mFe:mO=56x:16y
=70:30
=70/56:30/16
=2:3
vậy CTHH là Fe2O3
Một loại oxi sắt có thành phần là: 7 phần khối lượng sắt kết hợp với 3 phần khối lượng oxi. Em hãy cho biết: Khối lượng mol của oxit sắt tìm được ở trên
Khối lượng mol của F e 2 O 3 : ( 56.2) + (16.3) = 160(g)
Có 0,75 mol một oxit sắt chứa 22.5 * 10 ^ 23 nguyên tử sắt và oxi. Tìm công thức hóa học của oxit sắt.
Đặt oxit sắt đó là FexOy, ta có:
(x+y)*6*10^23 = (22.5/0.75)*10^23
<=> (x+y)*6 = 30
<=> x+y=5
Nếu x=1, FexOy: FeO => x+y=2 (0 t/m)
Nếu x=2, FexOy: Fe2O3 => x+y= 2+3 = 5 (t/m)
Nếu x=3, FexOy: Fe3O4 => x+y= 3+4 = 7 (0 t/m)
Vậy x=2 => y=3. CTHH của oxit đó là Fe2O3
Bài 1: Đốt cháy 16,8 g sắt trong oxi thu được oxit sắt từ(Fe3O4)
a/ Viết phương trình phản ứng
b/ Tính thể tích khí oxi tham gia phản ứng ở đktc và khối lượng sản phẩm
c/ Nếu dùng số mol khí hidro bằng số mol sắt ở trên để khử 16g đồng(II)oxit (CuO) ở nhiệt độ cao thì thu được bao nhiêu gam đồng?
a, \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b, \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{2}{3}n_{Fe}=0,2\left(mol\right)\Rightarrow V_{O_2}=0,2.22,4=4,48\left(l\right)\)
\(n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=0,1\left(mol\right)\Rightarrow m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\)
c, \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,3}{1}\), ta được H2 dư.
Theo PT: \(n_{Cu}=n_{CuO}=0,2\left(mol\right)\Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)
X 1 Có 0,75 mol một oxit sắt chứa 22.5 * 10 ^ 23 nguyên tử sắt và oxi. Tìm công thức hóa học của oxit sắt.
CTTQ:FexOy
ta có: 0,75x+0,75y=3,75
=>y=(3,75-0,75x)/0,75
x có giá trị 1 2 3
=>x=2 =>y=3
=>CTHH:Fe2O3