cho 15,3g oxit kim loại hóa trị (2) vào nước thu được 200g dung dịch bazo với nồng độ 8,55%. Hãy xác định công thức của oxit trên

Những câu hỏi liên quan
1.Hòa tan 4g ZnO vào 150g dd HCl 3,65%.Tính C% dd thu được sau phản ứng
2.Cho 15,3g oxit của kim loại hóa trị II vào nước thu đc dd bazo nồng độ 8,55%.Xác định công thức oxit trên
Cho 15,3 gam oxit của kim loại hoá trị II vào nước thu được 200gam dung dịch bazo với nồng độ 8,55%.Xác định công thức oxit trên
đặt công thức oxit cần tìm là: XO
mX(OH)2= C%*mdd/100=8.55*200/100=17.1g
áp dụng bảo toàn khối lượng: mH2O=17.115.3=1.8g =>nH2O=1.8/18=0.1mol
pt: XO + H2O--> X(OH)2
0.1 0.1
MXO=15.3/0.1=153 g/mol
=> MX= MXO - MO2= 153-16=137
Vậy X là Ba. CTHH của oxit là BaO
Chúc em học tốt!!!:))
Đúng 4
Bình luận (0)
Cho 15,3 gam oxit của kim loại hoá trị II vào nước thu được 200 gam dung dịch bazơ với nồng độ 8,55%. Hãy xác định công thức của oxit trên.
Cách 1: Đặt công thức hoá học của oxit là MO ⇒ công thức bazơ là M OH 2
MO + H 2 O → M OH 2
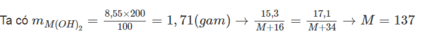
→ Công thức oxit là BaO.
Cách 2: m H 2 O ( p / u ) = m M OH 2 - m MO = 17,1 - 15,3 = 1,8(g)
MO + H 2 O → M OH 2
![]()
Công thức oxit là BaO
Đúng 0
Bình luận (0)
Cho 15,3 gam oxit của kim loại hóa trị II vào nước thu được 200 gam dung dịch bazơ với nồng độ 8,55%. Công thức của oxit trên là
A. N a 2 O
B. CaO
C. BaO
D. K 2 O
Chọn C
Đặt công thức hóa học của oxit là MO
PTHH:
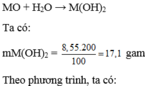
![]()
=> kim loại M là Ba
=> công thức oxit là BaO
Đúng 0
Bình luận (0)
có ai biết giải bài này k mình đang cần rất gấp mong các bạn giúp cho
Bài 1: cho 5,6g oxit của kim loại hóa trị (II) vào nước thu đc 200g dd bazo với nồng độ 3,7%. hãy xác định công thức của oxit trên.
PTHH: \(RO+H_2O\rightarrow R\left(OH\right)_2\)
Theo PTHH: \(n_{RO}=\dfrac{5,6}{R+16}\left(mol\right)=n_{ROH}\)
\(\Rightarrow\dfrac{\dfrac{5,6}{R+16}\cdot\left(R+34\right)}{200}=0,037\) \(\Leftrightarrow R=40\) (Canxi)
Vậy CTHH của oxit là CaO
Đúng 2
Bình luận (1)
Cho 15,3 gam oxit của kim loại hóa trị II vào nước thu được 200 gam dung dịch bazơ với nồng độ 8,55%. Công thức hóa học của oxit trên là?
Con chưa hiểu câu này thầy ơi:((
Gọi CTHH của oxit là $RO$
$RO + H_2O \to R(OH)_2$
$m_{R(OH)_2} = 200.8,55\% = 17,1(gam)$
Theo PTHH : $n_{RO} = n_{R(OH)_2}$
$\Rightarrow \dfrac{15,3}{R + 17} = \dfrac{17,1}{R + 34}$
$\Rightarrow R = 137(Bari)$
Vậy CTHH của oxit là $BaO$
Đúng 6
Bình luận (0)
Cho 15,3 gam oxide của kim loại hóa trị II vào nước thu được 200 gam dung dịch base với nồng độ 8,55%. Hãy xác định công thức của oxide trên.
Gọi CTHH của oxide là $RO$
$RO + H_2O \to R(OH)_2$
$m_{R(OH)_2} = 200.8,55\% = 17,1(gam)$
Theo PTHH :
$n_{RO} = n_{R(OH)_2}$
$\Rightarrow \dfrac{15,3}{R + 16} = \dfrac{17,1}{R + 34}$
$\Rightarrow R = 137(Ba)$
Vậy CT của oxide là $BaO$
Đúng 1
Bình luận (0)
Chọn 15,3gam oxit của một kim loại hóa trị II vào nước thu được 200gam dung dịch bazo có nồng độ 8,55% . Xác định công thức phân tử của oxit .
Gọi CTPT của oxit là RO
PTHH : RO + H2O \(\rightarrow\) R(OH)2
Theo đề bài ta có: \(n_{RO}=\dfrac{15,3}{R+16}\left(mol\right)\)
\(m_{R\left(OH\right)_2}=\dfrac{200.8,55}{100}=17,1\left(g\right)\)
\(\Rightarrow n_{R\left(OH\right)_2}=\dfrac{17,1}{R+34}\left(mol\right)\)
Theo phương trình : nRO = nR(OH)2
hay: \(\dfrac{15,3}{R+16}\) = \(\dfrac{17,1}{R+34}\)
\(\Leftrightarrow15,3R+520,2=17,1R+273,6\)
\(\Leftrightarrow1,8R=246,6\)
\(\Leftrightarrow R=137\)
=> R là Bari ( Ba)
Vậy CTPT của oxit là BaO
Đúng 0
Bình luận (0)
Cho 15,3 g Oxit của 1 kim loại có hóa trị II vào nước thu được 200g dd Bazo có C% là 8,55 %.Hãy tìm CT và tên kim loại
Gọi CTHH của oxit kim loại hóa trị II là MO
MO + H2O ------> M(OH)2
\(\frac{15,3}{M+16}\) --------------> \(\frac{15,3}{M+16}\)(mol)
C%(dd bazơ) =[\(\frac{15,3}{M+16}\).(M+34)] : 200 . 100% = 8,55%
=> Giải pt ta được: M=137 (g/mol)
=> M là Ba (Bari)
Đúng 0
Bình luận (0)

















