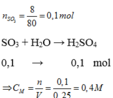Hòa tan 40g lưu huỳnh dioxit với H2O thu dc 250ml dung dịch axit sunfuric. Tính nồng độ mol của dung dịch axit

Những câu hỏi liên quan
cho 8 g lưu huỳnh trioxit tác dụng với nước ,thu được 250ml dung dịch axit sunfuric
a) viết phương trình hóa học
b)xác định nồng độ mol của dung dịch axit
c)nếu trung hòa hết lượng axit thu được ở trên bằng dung dịch KOH 5,6% có khối lượng riêng là 1,045 g/ml thì cần bao nhiêu ml dung dịch KOH ?
Ta có: \(n_{SO_3}=\dfrac{8}{80}=0,1\left(mol\right)\)
a. PTHH: SO3 + H2O ---> H2SO4 (1)
b. Theo PT(1): \(n_{H_2SO_4}=n_{SO_3}=0,1\left(mol\right)\)
Đổi 250ml = 0,25 lít
=> \(C_{M_{H_2SO_4}}=\dfrac{0,1}{0,25}=0,4\left(M\right)\)
c. PTHH: H2SO4 + 2KOH ---> K2SO4 + 2H2O
Theo PT(2): \(n_{KOH}=2.n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
=> \(m_{KOH}=0,2.56=11,2\left(g\right)\)
Ta có: \(C_{\%_{KOH}}=\dfrac{11,2}{m_{dd_{KOH}}}.100\%=5,6\%\)
=> \(m_{dd_{KOH}}=200\left(g\right)\)
Ta có: \(d_{KOH}=\dfrac{200}{V_{dd_{KOH}}}=1,045\)(g/ml)
=> \(V_{dd_{KOH}}=191,4\left(ml\right)\)
Đúng 0
Bình luận (0)
Cho 8 gam lưu huỳnh trioxit (
S
O
3
) tác dụng với
H
2
O
, thu được 250 ml dung dịch axit sunfuric (
H
2
S
O
4
). Nồng độ mol của dung dịch axit thu được là A. 0,1M B. 0,4M C. 0,5M D. 0,6M
Đọc tiếp
Cho 8 gam lưu huỳnh trioxit ( S O 3 ) tác dụng với H 2 O , thu được 250 ml dung dịch axit sunfuric ( H 2 S O 4 ). Nồng độ mol của dung dịch axit thu được là
A. 0,1M
B. 0,4M
C. 0,5M
D. 0,6M
Cho 8 gam lưu huỳnh trioxit ( SO 3 ) tác dụng với H 2 O , thu được 250 ml dung dịch axit sunfuric ( H 2 SO 4 ).
Xác định nồng độ mol của dung dịch axit thu được.
Nồng độ mol của dung dịch H 2 SO 4 :
n H 2 SO 4 = n SO 3 = 8/80 = 0,1 mol
Theo phương trình hoá học :
C Mdd H 2 SO 4 = 1000x0,1/250 = 0,4M
Đúng 0
Bình luận (0)
250ml dung dịch có hòa tan 0,1 mol H2SO4. Hãy tính nồng độ mol của dung dịch axit
\(C_{M_{H_2SO_4}}=\dfrac{n}{V}=\dfrac{0,1}{0,25}=0,4M\)
Đúng 1
Bình luận (0)
Cho 8 gam lưu huỳnh trioxit vào nước thu được 250ml dung dịch axit sunfuric
a) Viết phương trình phản ứng
b) Tính nồng độn mol dung dịch axit thu được
HELP ME !!!
SO3 + H2O => H2SO4
nSO3 = m/M = 8/80 = 0.1 (mol)
Theo phương trình
==> nH2SO4 = 0.1 (mol)
250 ml dd = 0.25 (l) dd
CM ddH2SO4 = n/V = 0.1/0.25 = 0.4M
Đúng 0
Bình luận (0)
Cho 2,24 lít khí SO3 (đktc) hòa tan vào nước thu được 500ml dung dịch axit sunfuric(H2SO4)
a) Tính nồng độ mol của dung dịch axit H2SO4.
b)Tính khối lượng Zn có thể phản ứng hết với axit có trong dung dịch trên?
a, PTPƯ: SO3 + H2O ---> H2SO4
nSO3=\(\dfrac{2,24}{22,4}=0,1mol\)
1 mol SO3 ---> 0,1 mol H2SO4
nên 0,1 mol SO3 ---> 0,1 mol H2SO4
CM H2SO4=\(\dfrac{0,1}{0,5}\)=0,2 M
b, PTPƯ: Zn + H2SO4 ---> ZnSO4 + H2
1 mol H2SO4 ---> 1 mol Zn
nên 0,1 mol H2SO4 ---> 0,1 mol Zn
mZn=0,1.65=6,5 g
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 16,8 gam sắt (Fe) bằng 200 gam ( quy đổi thể tích là 250ml ) dung dịch axit sunfuric (H2SO4) vừa đủ thu được dung dịch FeSO4 và V lít khí H2 thoát ra ở (đktc)a) Tìm V , nồng độ mol và nồng độ phần trăm của dung dịch H2SO4 đã dùng ?b) Lượng khí H2 sinh ra ở trên được dẫn qua ống nghiệm đựng 16 (g) CuO đun nóng, phản ứng xảy ra hoàn toàn. Tính khối lượng kim loại thu được?
Đọc tiếp
Hòa tan hoàn toàn 16,8 gam sắt (Fe) bằng 200 gam ( quy đổi thể tích là 250ml ) dung dịch axit sunfuric (H2SO4) vừa đủ thu được dung dịch FeSO4 và V lít khí H2 thoát ra ở (đktc)
a) Tìm V , nồng độ mol và nồng độ phần trăm của dung dịch H2SO4 đã dùng ?
b) Lượng khí H2 sinh ra ở trên được dẫn qua ống nghiệm đựng 16 (g) CuO đun nóng, phản ứng xảy ra hoàn toàn. Tính khối lượng kim loại thu được?
a)
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$n_{H_2SO_4} = n_{H_2} = n_{Fe} = \dfrac{16,8}{56} = 0,3(mol)$
$V = 0,3.22,4 = 6,72(lít)$
$C_{M_{H_2SO_4}} = \dfrac{0,3}{0,25} = 1,2M$
b)
$n_{CuO} = \dfrac{16}{80} = 0,2(mol)$
$CuO + H_2 \xrightarrow{t^o} Cu + H_2O$
$n_{CuO} < n_{H_2}$ nên $H_2$ dư
$n_{Cu} = n_{CuO} = 0,2(mol)$
$m_{Cu} = 0,2.64 = 12,8(gam)$
Đúng 4
Bình luận (0)
\(n_{Fe}=\dfrac{m}{M}=\dfrac{16,8}{56}=0,3\left(mol\right)\\ PT:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,3 0,3 0,3 (mol)
a) V= n. 22,4 = 0,3 . 22,4 = 6,72(l)
\(C\%=\dfrac{m_{H_2SO_4}}{m_{dd}}.100\%=\dfrac{0,3.98}{200}.100\%=11,76\%\)
b) PT: \(H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
0,3 0,3
=> mCu=n.M=0,3.64=19,2(g)
Đúng 0
Bình luận (0)
Cho 8g lưu huỳnh trioxit SO3 tác dụng với nước thu được 250ml dung dịch axit sunfuric H2SO4
a. Viết phương trình hóa học
b. Xác định nồng độ CM của axit thu được
Đổi 250ml=0,25l
\(SO_3+H_2O\)→\(H_2SO_4\)
+\(n_{SO_3}=\frac{8}{64}=0,125\left(mol\right)\)
+\(n_{H_2SO_4}=n_{SO_3}=0,125\left(mol\right)\)
+\(C_M=\frac{0,125}{0,25}=0,5M\)
ta có 250ml=0,25l
n\(_{SO_3}\)=\(\frac{m_{SO3}}{M_{SO3}}\)= \(\frac{8}{64}\) =0.125 (mol)
a.PTHH:SO3 + H2O-> H2SO4
b.Axit thu được là H2SO4
=> CM=\(\frac{n_{H_2SO_4}}{V_{H_2O}}\) = \(\frac{0.125}{0.25}\) = 0.5 M
Hòa tan 14,6g axit clohidric thu được 250ml dung dịch axit sunfuric.
a) Hãy tính nồng độ mol dung dịch?
b) Tính nồng độ phần trăm dung dịch ( biết \(D_{ddHCl}\)=1,25g/ml)