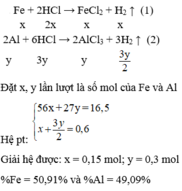Bài 19. Cho 22,2 gam hỗn hợp gồm Fe, Al tan hoàn toàn trong HCl, ta thu được 13,44 lít H2 (đktc). Tính thành phần % khối lượng mỗi chất trong hỗn hợp và khối lượng muối clorua khan thu được.

Những câu hỏi liên quan
cho 22,2gam hỗn hợp gồm Al,Fe hòa tan trong dung dịch HCl thu được 13,44 lít H2(đktc).Tính thành phần % khối lượng mỗi chất trong hỗn hợp và khối lượng muối clorua khan thu được
PTHH:
(1) 2 Al + 6 HCl -> 2AlCl3 + 3 H2
x_____3x_________x_______1,5x (mol)
(2) Fe + 2 HCl -> FeCl2 + H2
y___________2y___y___y (mol)
Ta có: nH2= 13,44/22,4= 0,6(mol)
nH2(1) + nH2(2)= nH2(tổng)
<=> 1,5x+y=0,6 (a)
Ta có: mAl+mFe= 22,2
<=> 27x+56y=22,2 (b)
Từ (a), (b) ta có hpt:
\(\left\{{}\begin{matrix}1,5x+y=0,6\\27x+56y=22,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
Ta có: mAl= 0,2.27=5,4(g)
=> %mAl= \(\frac{5,4}{22,2}.100\approx24,324\%\)
=> \(\%mFe\approx100\%-24,324\%\approx75,676\%\)
* nAlCl3= x= 0,2(mol)
nFeCl2= y=0,3(mol)
=> mAlCl3= 133,5.0,2=26,7(g)
mFeCl2= 127.0,3= 38,1(g)
=> %mAlCl3= \(\frac{26,7}{26,7+38,1}.100\approx41,204\%\\ \Rightarrow\%mFeCl2\approx100\%-41,204\%\approx58,796\%\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có :
\(\left\{{}\begin{matrix}27x+56y=22,2\\1,5x+y=\frac{13,44}{22,4}\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
\(\rightarrow\%m_{Al}=\frac{0,2.27}{22,2}.100\%=24,32\%,\%m_{Fe}=100\%-24,32\%=75,68\%\)
\(m_{AlCl3}=0,2.133,5=26,7\left(g\right)\)
\(m_{FeCl_2}=0,3.127=38,1\left(g\right)\)
PTHH ( I ) : \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
......................x.........3x..............x............\(\frac{3}{2}\)x......
PTHH ( II ) : \(Fe+2HCl\rightarrow FeCl_2+H_2\)
.......................y.........2y..............y............y.......
- Gọi số mol của nhôm và sắt có trong hỗn hợp lần lượt là x, y (x, y> 0 )
a, - Ta có : \(m_{hh}=m_{Fe}+m_{Al}=n_{Fe}.M_{Fe}+n_{Al}.M_{Al}=22,2\)
=> \(56y+27x=22,2\) ( I )
\(n_{H_2}=\frac{V_{H_2}}{22,4}=\frac{13,44}{22,4}=0,6\left(mol\right)\)
Mà \(n_{H_2}=n_{H_2\left(I\right)}+n_{H_2\left(II\right)}\)
=> \(1,5x+y=0,6\) ( II )
- Từ ( I ) và ( II ) ta có hệ phương trình : \(\left\{{}\begin{matrix}27x+56y=22,2\\1,5x+y=0,6\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}27x+56\left(0,6-1,5x\right)=22,2\\y=0,6-1,5x\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}27x-84x=-11,4\\y=0,6-1,5x\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,2\\y=0,6-1,5.0,2=0,3\left(mol\right)\end{matrix}\right.\) ( TM )
=> \(\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,3\left(mol\right)\end{matrix}\right.\)
-> \(m_{Al}=n_{Al}.M_{Al}=0,2.27=5,4\left(g\right)\)
-> \(\%Al=\frac{m_{Al}}{m_{hh}}=\frac{5,4}{22,2}.100\%\approx24,3\%\)
Mà \(\%hh=\%Al+\%Fe=24,3\%+\%Fe=100\%\)
=> \(\%Fe=75,6\%\)
b, Ta có : \(\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,3\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{\left(Al\right)}=0,2\left(mol\right)\\n_{\left(Fe\right)}=0,3\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{AlCl_3}=0,2\left(mol\right)\\n_{FeCl_2}=0,3\left(mol\right)\end{matrix}\right.\)
=> mMuối khan = \(m_{AlCl3}+m_{FeCl2}=n_{AlCl3}.M_{AlCl3}+n_{FeCl2}.M_{FeCl2}\)
=> mMuối khan = \(0,2.\left(27+35,5.3\right)+0,3.\left(56+35,5.2\right)=64,8\left(g\right)\)
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau. - Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc). - Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,78; 0,54; 1,12 B. 0,39; 0,54; 1,40 C. 0,39; 0,54; 0,56 D. 0,78; 1,08; 0,56
Đọc tiếp
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.
- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc).
- Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc).
Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,78; 0,54; 1,12
B. 0,39; 0,54; 1,40
C. 0,39; 0,54; 0,56
D. 0,78; 1,08; 0,56
Chia hỗn hợp X gồm K, Al, Fe thành hai phần bằng nhau. Cho phần 1 vào dung dịch KOH dư thu được 0,784 lít khí H2 (đktc). Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl dư, thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,39; 0,54; 0,56 B. 0,39; 0,54; 1,40 C. 0,78; 1,08; 0,56. D. 0,78; 0,54; 1,12
Đọc tiếp
Chia hỗn hợp X gồm K, Al, Fe thành hai phần bằng nhau.
Cho phần 1 vào dung dịch KOH dư thu được 0,784 lít khí H2 (đktc).
Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl dư, thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,39; 0,54; 0,56
B. 0,39; 0,54; 1,40
C. 0,78; 1,08; 0,56.
D. 0,78; 0,54; 1,12
Hoà tan hoàn toàn 16,5 gam hỗn hợp A gồm Fe và Al vào 500 dung dịch HCl 2,5M (d =1,1g/ml) thu được 13,44 lít H 2 (đktc) và dung dịch B. Tính % khối lượng mỗi kim loại trong hỗn hợp A
Chia hỗn hợp X gồm K, AI và Fe thành hai phần bằng nhau. Cho phần một vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc). Cho phần hai vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,39; 0,54; 1,40. B. 0,78; 0,54;1,12 C. 0,39; 0,54; 0,56 D. 0,78; 1,08;0,56
Đọc tiếp
Chia hỗn hợp X gồm K, AI và Fe thành hai phần bằng nhau.
Cho phần một vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc).
Cho phần hai vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc).
Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,39; 0,54; 1,40.
B. 0,78; 0,54;1,12
C. 0,39; 0,54; 0,56
D. 0,78; 1,08;0,56
Hòa tan hoàn toàn 14,15 gam hỗn hợp X gồm Al và Cu trong dung dịch HCl dư thu được dung dịch Y, chất rắn Z và thoát ra V lít khí H2 (đktc). Cô cạn dung dịch Y thu được 6,675 gam muối khan. a. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu. b. Tính V c. Nếu đốt cháy hoàn toàn lượng X trên trong khí O2 thì thể tích O2 đem đốt cháy là bao nhiêu.
Đọc tiếp
Hòa tan hoàn toàn 14,15 gam hỗn hợp X gồm Al và Cu trong dung dịch HCl dư thu được dung dịch Y, chất rắn Z và thoát ra V lít khí H2 (đktc). Cô cạn dung dịch Y thu được 6,675 gam muối khan.
a. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu. b. Tính V c. Nếu đốt cháy hoàn toàn lượng X trên trong khí O2 thì thể tích O2 đem đốt cháy là bao nhiêu.
a) \(n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,05<-----------0,05---->0,075
=> \(\%Al=\dfrac{0,05.27}{14,15}.100\%=9,54\%\)
=> \(\%Cu=\dfrac{14,15-0,05.27}{14,15}.100\%=90,46\%\)
b) \(V_{H_2}=0,075.22,4=1,68\left(l\right)\)
c) \(n_{Cu}=\dfrac{14,15-0,05.27}{64}=0,2\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
2Cu + O2 --to--> 2CuO
0,2-->0,1
=> \(V_{O_2}=\left(0,1+0,0375\right).22,4=3,08\left(l\right)\)
Đúng 1
Bình luận (0)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ m_{AlCl_3}=6,675\left(mol\right)\\ n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\\ \Rightarrow n_{Al}=n_{AlCl_3}=0,05\left(mol\right)\\ \Rightarrow m_A=0,05.27=1,35\left(g\right);m_{Cu}=14,15-1,35=12,8\left(g\right)\\ \%m_{Cu}=\dfrac{12,8}{14,15}.100\approx90,459\%\\ \Rightarrow\%m_{Al}\approx9,541\%\\ b,n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\\ n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,05=0,075\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,075.22,4=1,68\left(l\right)\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Cu+O_2\rightarrow\left(t^o\right)2CuO\\ n_{O_2}=\dfrac{3}{4}.n_{Al}+\dfrac{1}{2}.n_{Cu}=\dfrac{3}{4}.0,05+\dfrac{1}{2}.0,2=0,0875\left(mol\right)\)
\(\Rightarrow V_{O_2\left(đktc\right)}=0,0875.22,4=1,96\left(l\right)\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 4,34 gam hỗn hợp gồm Fe, Mg, Al trong dung dịch HCl thu được 1,792 lít H2 (đktc). Khối lượng muối muối khan thu được khi cô cạn dung dịch sau phản ứng là
A. 12,02 gam
B. 11,05 gam
C. 10,02 gam
D. 10,2 gam.
Hòa tan hoàn toàn 4,34 gam hỗn hợp gồm Fe, Mg, Al trong dung dịch HCl thu được 1,792 lít H2 (đktc). Khối lượng muối muối khan thu được khi cô cạn dung dịch sau phản ứng là A. 12,02 gam. B. 11,05 gam. C. 10,02 gam. D. 10,2 gam.
Đọc tiếp
Hòa tan hoàn toàn 4,34 gam hỗn hợp gồm Fe, Mg, Al trong dung dịch HCl thu được 1,792 lít H2 (đktc). Khối lượng muối muối khan thu được khi cô cạn dung dịch sau phản ứng là
A. 12,02 gam.
B. 11,05 gam.
C. 10,02 gam.
D. 10,2 gam.
Đáp án C.
→ n C l - = 2 n H 2 = 0 , 16 → m m u o i = 4 , 34 + 0 , 16 . 35 , 5 = 10 , 02
Đúng 0
Bình luận (0)
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí
H
2
(đktc).- Cho phần 2 vào một lượng dư
H
2
O
, thu được 0,448 lít khí
H
2
(đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí
H
2
(đktc). Tính khối lượng mỗi kim loại trong mỗi phần.
Đọc tiếp
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.
- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H 2 (đktc).
- Cho phần 2 vào một lượng dư H 2 O , thu được 0,448 lít khí H 2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H 2 (đktc). Tính khối lượng mỗi kim loại trong mỗi phần.