Cho biết Al có 13 prôtn,13 electon và 14 notron
a)Tính khối lượng của nguyên tử Al
b)Một nguyên tử gam Al có khối lượng là 27g.Tính số nguyên tử nhôm có trong 1 nguyên tử gam Al

Những câu hỏi liên quan
Phân tử nhôm bromua là hợp chất đc tạo nên từ 1 nguyên tử Al và 3 nguyên tử br tính thành phần phần trăm theo khối lượng của các nguyên tố có trong hợp chất
công thuc hoa hoc la AlBr3
nguyen tu khoi cua Br = 80
%Al = 27/(27+80.3) = 10%
%Br = 90%
Đúng 0
Bình luận (0)
1.Hợp chất X tạo bởi nguyên tố Al và O, có phân tử khối là 102. Biết tỉ lệ khối lượng của Al với O là 6,75/6. Tìm số nguyên tử Al và O trong X.2.Nung nóng hợp chất A, A bị phân hủy hoàn toàn tạo thành 56 gam CaO và 44 gam CO2. Cho biết các nguyên tố tạo nên A. Khối lượng của mỗi nguyên tố trong A.Giải chi tiết giúp mình với! Cảm ơn nhìu
Đọc tiếp
1.Hợp chất X tạo bởi nguyên tố Al và O, có phân tử khối là 102. Biết tỉ lệ khối lượng của Al với O là 6,75/6. Tìm số nguyên tử Al và O trong X.
2.Nung nóng hợp chất A, A bị phân hủy hoàn toàn tạo thành 56 gam CaO và 44 gam CO2. Cho biết các nguyên tố tạo nên A. Khối lượng của mỗi nguyên tố trong A.
Giải chi tiết giúp mình với! Cảm ơn nhìu![]()
bài 1: gọi công thức hợp chất X là AlxOy
theo đề ta có : \(\frac{27x}{16y}=\frac{6,75}{6}\)
=> \(\frac{27x+16y}{6,75+6}=\frac{102}{12,75}=8\)
=> x=8.6,75:27=2
y=8.6:16=3
vậy CTHH của X là Al2O3
Đúng 0
Bình luận (0)
1) tính khối lượng gam của các nguyên tố có trong 10g CuSO4
2) trong phân tử R2On (R là nguyên tố chưa biết; n chưa biết). trong phân tử trên, nguyên tố R chiếm 80% về khối lượng. tính % về khối lượng của các nguyên tố có trong phân tử R2(SO4)n
1/ Số mol CuSO4 trong 10g CuSO4 là:
\(n_{CuSO_4}=\dfrac{m}{M}=\dfrac{10}{160}=0,0625\left(mol\right)\)
Vậy, \(m_{Cu}=0,0625\cdot64=4\left(g\right)\)
\(m_S=0,0625\cdot32=2\left(g\right)\)
\(m_O=0,0625\cdot4\cdot16=4\left(g\right)\)
Đúng 0
Bình luận (0)
Một hợp chất A có phân tử gồm nguyên tử nguyên tố X liên kết với 4 nguyên tử H và nặng bằng nguyên tử Oa/ Tính nguyên tử khối, cho biết tên và kí hiệu hóa học của nguyên tố X.b/ Tính phần trăm về khối lượng của nguyên tố X trong hợp chất A. Biết rằng phần trăm về khối lượng của một nguyên tố trong hợp chât bằng phần trăm về khối lượng của nguyên tố đó trong 1 phân tử
Đọc tiếp
Một hợp chất A có phân tử gồm nguyên tử nguyên tố X liên kết với 4 nguyên tử H và nặng bằng nguyên tử O
a/ Tính nguyên tử khối, cho biết tên và kí hiệu hóa học của nguyên tố X.
b/ Tính phần trăm về khối lượng của nguyên tố X trong hợp chất A. Biết rằng phần trăm về khối lượng của một nguyên tố trong hợp chât bằng phần trăm về khối lượng của nguyên tố đó trong 1 phân tử
1) tính khối lượng mol (M) của kali pemanganat
2) Tính số mol nguyên tử và khối lượng của mỗi nguyên tố hóa học có trong một mol kali pemanganat
3) Trong phân tử kali pemanganat, nguyên tố nào có thành phần phần trăm theo khối lượng lớn nhất? Tại sao?
1/ MKMnO4 = 39 + 55 + 16 x 4 = 158 g/mol
2/ K : 1 nguyên tủ
Mn: 1 nguyên tử
O2 : 4 nguyên tử
3/ Trong phân tử KMnO4 , nguyên tố O có thành phần phần trăm theo khối lượng lớn nhất vì O chiếm khối lượng lớn nhất ( là 64 gam)
Đúng 0
Bình luận (0)
Một lượng khí có khối lượng là 30 kg và chứa
11
,
28
.
10
26
phân tử. Phân tử khí này gồm các nguyên tử hiđrô và cacbon. Biết 1 mol khí có
N
A
6
,
02
.
10
23
phân tử. Khối lượng của các nguyển tử cacbon và hiđrô trong khí này là A....
Đọc tiếp
Một lượng khí có khối lượng là 30 kg và chứa 11 , 28 . 10 26 phân tử. Phân tử khí này gồm các nguyên tử hiđrô và cacbon. Biết 1 mol khí có N A = 6 , 02 . 10 23 phân tử. Khối lượng của các nguyển tử cacbon và hiđrô trong khí này là
A. m C = 2 . 10 - 26 k g ; m H = 0 , 66 . 10 - 26 k g
B. m C = 4 . 10 - 26 k g ; m H = 1 , 32 . 10 - 26 k g
C. m C = 2 . 10 - 6 k g ; m H = 0 , 66 . 10 - 6 k g
D. m C = 4 . 10 - 6 k g ; m H = 1 , 32 . 10 - 6 k g
Chọn A.
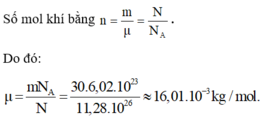
Trong khi có hiđrô và cacbon, chí CH4 có
μ = (12 + 4).10-3 kg/mol
Vì thế, khí đã cho là CH4. Khối lượng của 1 phân tử khí CH4 là 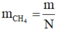
Khối lượng của nguyên tử hiđrô là:
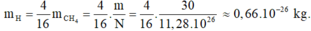
Khối lượng của nguyên tử cacbon là:
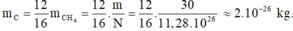
Đúng 0
Bình luận (0)
Một lượng khí có khối lượng là 30 kg và chứa
11
,
28
.
10
26
phân tử. Phân tử khí này gồm các nguyên tử hiđrô và cacbon. Biết 1 mol khí có
N
A
6
,
02
.
10
23
phân tử. Khối lượng của các nguyển tử cacbon và hiđrô trong khí này là A.
m...
Đọc tiếp
Một lượng khí có khối lượng là 30 kg và chứa 11 , 28 . 10 26 phân tử. Phân tử khí này gồm các nguyên tử hiđrô và cacbon. Biết 1 mol khí có N A = 6 , 02 . 10 23 phân tử. Khối lượng của các nguyển tử cacbon và hiđrô trong khí này là
A. m C = 2 . 10 - 26 k g ; m H = 0 , 66 . 10 - 26 k g
B. m C = 4 . 10 - 26 k g ; m H = 1 , 32 . 10 - 26 k g
C. m C = 2 . 10 - 6 k g ; m H = 0 , 66 . 10 - 6 k g
D. m C = 4 . 10 - 6 k g ; m H = 1 , 32 . 10 - 6 k g
Chọn A.
Số mol khí bằng
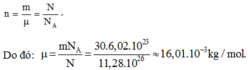
Trong khi có hiđrô và cacbon, chí CH4 có μ = (12 + 4).10-3 kg/mol
Vì thế, khí đã cho là CH4. Khối lượng của 1 phân tử khí CH4 là
![]()
Khối lượng của nguyên tử hiđrô là:
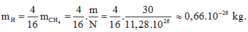
Khối lượng của nguyên tử cacbon là:
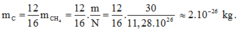
Đúng 0
Bình luận (0)
a. Hãy tính khối lượng bằng gam của một nguyên tử Na, hai nguyên tử canxi.
b. 2,5. 1023 nguyên tử natri; 1,5.1023 phân tử nước có bao nhiêu gam?
SNa=6.1023(ng tử)\(\Rightarrow\) \(n_{Na}=\frac{6.10^{23}}{6.10^{23}}=1\left(mol\right)\)
mNa=1.23=23 g
SCa=2.1023 (ng tử)\(\Rightarrow n_{Ca}=\frac{2.10^{23}}{6.10^{23}}=\frac{1}{3}\left(mol\right)\)
mCa=\(\frac{1}{3}.40=\frac{40}{3}g\)
b) nNa=\(\frac{2,5.10^{23}}{6.10^{23}}=\frac{5}{12}\left(mol\right)\)
\(\Rightarrow m_{Na}=\frac{5}{12}.23=\frac{115}{12}\left(g\right)\)
\(n_{H2O}=\frac{1,5.10^{23}}{6.10^{23}}=0,25\left(mol\right)\)
\(\Rightarrow m_{H2O}=0,25.18=4,5\left(g\right)\)
Đúng 0
Bình luận (0)
Bài 1: Nguyên tử X có tổng số hạt là 52 và có khối lượng là 35. Tìm số hạt proton, nơtron,electron của XBài 2: Trong nguyên tử X, tổng số hạt bằng 52, số hạt mang điện nhiều hơn số hạt ko mang điện là 16. Tìm số proton và khối lượng của X.Bài 3: Nguyên tử X có tổng số hạt là 60. Trong đó số hạt nơtron bằng số proton. Tìm nguyên tố X.Bài 4: Nguyên tử của nguyên tố X đc cấu tạo bởi 36 hạt, hạt mang điện gấp đôi số hạt ko mang điện. Ti...
Đọc tiếp
Bài 1: Nguyên tử X có tổng số hạt là 52 và có khối lượng là 35. Tìm số hạt proton, nơtron,electron của X
Bài 2: Trong nguyên tử X, tổng số hạt bằng 52, số hạt mang điện nhiều hơn số hạt ko mang điện là 16. Tìm số proton và khối lượng của X.
Bài 3: Nguyên tử X có tổng số hạt là 60. Trong đó số hạt nơtron bằng số proton. Tìm nguyên tố X.
Bài 4: Nguyên tử của nguyên tố X đc cấu tạo bởi 36 hạt, hạt mang điện gấp đôi số hạt ko mang điện. Tìm số khối của nguyên tử nguyên tố X
Bạn nào biết giúp mình vs. Mình cần gấp lắm rồi




















