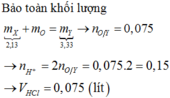Cho cho 19,2 gam hỗn hợp x gồm Mg và Fe tác dụng hoàn toàn với oxi sau phản ứng thu được 27,2 gam hỗn hợp 2 oxit tính phần trăm khối lượng các kim loại trong X

Những câu hỏi liên quan
Cho 19,2 gam hỗn hợp x gồm Mg và Fe tác dụng hoàn toàn với oxi dư sau phản ứng thu được 27,2 gam hỗn hợp 2 oxit tính phần trăm khối lượng các kim loại trong X
2Mg + O2 \(\rightarrow\)2MgO (1)
3Fe + 2O2 \(\rightarrow\)Fe3O4 (2)
Đặt nMg=a
nFe=b
Ta có:
\(\left\{{}\begin{matrix}24a+56b=19,2\\40a+\dfrac{232}{3}b=27,2\end{matrix}\right.\)
a=0,1;b=0,3
mMg=24.0,1=2,4(g)
% Mg=\(\dfrac{2,4}{19,2}.100\%=12,5\%\)
% Fe=100-12,5=87,5%
Đúng 0
Bình luận (1)
Hỗn hợp X gồm CuO, Fe3O4. Hòa tan hoàn toàn 27,2 gam hỗn hợp X cần dùng vừa hết
450 gam dung dịch HCl 7,3%.
a. Tính phần trăm khối lượng mỗi oxit kim loại trong hỗn hợp X.
b. Cho 27,2 gam X tác dụng với một lượng dư khí CO nung nóng thu được m gam kim
loại. Tính giá trị m.
Hỗn hợp khí X gồm clo và oxi. Cho X phản ứng vừa hết với một hỗn hợp Y gồm 4,8 gam Mg và 8,1 gam Al, sau phản ứng thu được 37,05 gam hỗn hợp rắn Z gồm muối clorua và oxit của 2 kim loại. Phần trăm theo khối lượng của Clo trong hỗn hợp X là A. 26,5% B. 73,5% C. 62,5% D. 37,5%
Đọc tiếp
Hỗn hợp khí X gồm clo và oxi. Cho X phản ứng vừa hết với một hỗn hợp Y gồm 4,8 gam Mg và 8,1 gam Al, sau phản ứng thu được 37,05 gam hỗn hợp rắn Z gồm muối clorua và oxit của 2 kim loại. Phần trăm theo khối lượng của Clo trong hỗn hợp X là
A. 26,5%
B. 73,5%
C. 62,5%
D. 37,5%
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là A. 57 ml B. 50 ml C. 75 ml D. 90 ml
Đọc tiếp
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là
A. 57 ml
B. 50 ml
C. 75 ml
D. 90 ml
Chọn đáp án C
n H C l = 2 n O o x i t = 2 3 , 33 - 2 , 13 16 = 0,15 (mol)
→ V d d H C l = 0 , 15 0 , 2 = 0,075 (lít)
Đúng 0
Bình luận (0)
Cho 4,26 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 6,66 gam. Thể tích dung dịch H2SO4 1M vừa đủ để phản ứng hết với Y là A. 75 ml B. 150 ml C. 55 ml D. 90 ml
Đọc tiếp
Cho 4,26 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 6,66 gam. Thể tích dung dịch H2SO4 1M vừa đủ để phản ứng hết với Y là
A. 75 ml
B. 150 ml
C. 55 ml
D. 90 ml
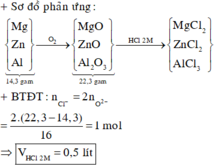
Cho 14,3 gam hỗn hợp X gồm ba kim loại Mg, Zn và Al ở dạng bột tác dụng hoàn toàn với oxi, thu được hỗn hợp Y gồm các oxit có khối lượng 22,3 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là A. 2,0 lít. B. 1,0 lít. C. 0,5 lít. D. 1,5 lít.
Đọc tiếp
Cho 14,3 gam hỗn hợp X gồm ba kim loại Mg, Zn và Al ở dạng bột tác dụng hoàn toàn với oxi, thu được hỗn hợp Y gồm các oxit có khối lượng 22,3 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là
A. 2,0 lít.
B. 1,0 lít.
C. 0,5 lít.
D. 1,5 lít.
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là A. 57 ml. B. 50 ml. C. 75 ml D. 90 ml
Đọc tiếp
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là
A. 57 ml.
B. 50 ml.
C. 75 ml
D. 90 ml
2. Cho 16,8 gam hỗn hợp Fe, Mg và Cu tác dụng hoàn toàn với dung dịch HCl dư. Sau phản ứng thu được 6,72 lít khí (ở đktc) và 6,4 gam chất rắn không tan. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu?
Cho Fe = 56; Mg = 24; Cu = 64.
Xem chi tiết
\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 16,8 - 6,4 = 10,4(1)\\ Fe + 2HCl \to FeCl_2 + H_2\\ Mg + 2HCl \to MgCl_2 + H_2\\ n_{H_2} = a + b = \dfrac{6,72}{22,4} = 0,3(2)\)
Từ (1)(2) suy ra: a = 0,1 ; b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,1.56}{16,8}.100\% = 33,33\%\\ \%m_{Mg} = \dfrac{0,2.24}{16,8}.100\% = 28,57\%\\ \%m_{Cu} = 100\% - 33,33\% - 28,57\% = 38,1\%\)
Đúng 3
Bình luận (0)
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu, Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Tính thể tích dung dịch H2SO4 2M vừa đủ để phản ứng hết với Y là?
mtăng=mO=3,33-2,13=1,2g
nO=1,2 : 16= 0,075 mol
nH2SO4 = nO(trong oxit)=0,075mol
VddHCl =0,075:2=0,0375 lit=37,5 ml
Đúng 0
Bình luận (0)