Bài 15 trong cốc đựng A2CO3. Thêm từ từu H2SO4 10% vào cốc cho tới khi khí vừa thoát ra hết thu đc dd muối nồng độ 13,63%. XĐ tên kim loại A

Những câu hỏi liên quan
Trong một cái cốc đựng muối cacbonat của kim loại hóa trị I. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hóa trị I là:
A. Li
B. Na
C. K
D. Ag
Đáp án B
Đặt công thức muối cacbonat kim loại là M2CO3
M2CO3+ H2SO4 → M2SO4 + CO2+ H2O
Giả sử n M 2 C O 3 = 1 mol
→ n H 2 S O 4 = n M 2 S O 4 = n C O 2 = 1mol
→ m H 2 S O 4 = 98 gam; m M 2 S O 4 = 2M+96 gam;
m C O 2 = 44 gam; m d d H 2 S O 4 10 % =980 g
Ta có: mdd sau pứ = m M 2 C O 3 + m d d H 2 S O 4 - m C O 2
=2M + 60+980-44= 2M+996 (gam)
C % M 2 S O 4 = 2 M + 96 2 M + 996 . 100 % = 13 , 63 % → M = 23 → M l à N a
Đúng 0
Bình luận (0)
Trong một cái cốc đựng một muối cacbonat của kim I loại hoá trị. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hoá trị I là A. Li. B. Na. C. K. D. Ag.
Đọc tiếp
Trong một cái cốc đựng một muối cacbonat của kim I loại hoá trị. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hoá trị I là
A. Li.
B. Na.
C. K.
D. Ag.
Đáp án B
Giả sử

khối lượng dung dịch sau phản ứng:
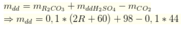
![]()
![]()
Đúng 0
Bình luận (0)
Một cốc đựng dung dịch muối cacbonat của một kim loại hóa trị II .Rót từ từ dung dịch H2SO4 có nồng độ 20% vào cốc cho đến khi khí thoát ra vừa hết thì thu được dung dịch muối có nồng độ 24,91%.Hãy xác định muối cacbonat của kim loại gì ?
gọi dd muối CO3 là ACO3
ACO3 +H2SO4 -->ASO4 +CO2+H2O
giả sử có 1 mol ACO3
=>mACO3= MA +60(g)
theo PTHH : nH2SO4=nACO3=1(mol)
=>mdd H2SO4=1.98.100/20=490(g)
nASO4=nACO3=1(mol)
=>mASO4=MA +96(g)
nCO2=nACO3=1(mol)
=>mCO2=44(g)
=>\(\dfrac{MA+96}{MA+60+490-44}\).100=24,91
giải ra ta được MA=40(g/mol0
=>ACO3:CaCO3
Đúng 1
Bình luận (0)
ta có pthh: ACO3 +H2SO4--ASO4+H2O+CO2
(A+60)g......98g.......(A+96)g..........44g
mdd H2SO4=(98.100):20=490g
mdd muối sau phản ứng=(A+60)+490-44= (A+506)g
theo đê bài ta có:C% ASO4=(A+96).100:A+506
suy ra A=40 CÓ: CTHH :CACO3
Đúng 0
Bình luận (0)
mdd muối sau phản ứng=(A+60)+490-44: (A+506)g=24,91%
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Giúp mk : Trong 1 chiếc cốc đựng muối cacbonat trung hòa kloại hóa trị I, thêm từ từ dd H2SO4 10% vào cốc cho tới khi khí thoát hết thu đk muối sunfat có nộng độ 13,63%. Xác định muối cacbonat.
giả sử muối cacbonat là A2CO3
A2CO3 +H2SO4 --> A2SO4 +CO2+H2O(1)
giả sử nA2CO3=1(mol)
=>mA2CO3=(2MA+60) (g)
theo (1) : nCO2=nA2SO4=nH2SO4=nA2CO3=1(Mol)
=>mddH2SO4=980(g)
mCO2=44(g)
mA2SO4=(2MA+96) (g)
=>\(\dfrac{2MA+96}{2MA+60+980-44}.100=13,63\left(\%\right)\)
=>MA=23(g/mol)
=>A:Na,A2CO3:Na2CO3
Đúng 0
Bình luận (0)
Hòa tan 3,2g oxit kim loại hóa trị III bằng 200 gam dung dịch H2SO4 loãng. Khi thêm vào hh sau phản ứng 1 lượng CaCO3 vừa đủ thấy thoát ra 0,224lít CO2. Sau đó khô cạn dd thu đuợc 9,36gam muối khan.A. Tìm công thức oxitB. Nồng độ phần trăm dd H2SO42. Hòa tan 18,4 gam hh kim loại hóa trị II và III bang dd hcl thu đc dd A và khí B chia đôi Ba. Phần b1 đem đốt cháy thu đc 4,5 gam nuớc khô cạn dd A thu đc bao nhiêu gam muối khanB. Phần b2 td hết với khí Clo rồi cho sản phẩm vào 200 ml dd NaO 20% d1...
Đọc tiếp
Hòa tan 3,2g oxit kim loại hóa trị III bằng 200 gam dung dịch H2SO4 loãng. Khi thêm vào hh sau phản ứng 1 lượng CaCO3 vừa đủ thấy thoát ra 0,224lít CO2. Sau đó khô cạn dd thu đuợc 9,36gam muối khan.
A. Tìm công thức oxit
B. Nồng độ phần trăm dd H2SO4
2. Hòa tan 18,4 gam hh kim loại hóa trị II và III bang dd hcl thu đc dd A và khí B chia đôi B
a. Phần b1 đem đốt cháy thu đc 4,5 gam nuớc khô cạn dd A thu đc bao nhiêu gam muối khan
B. Phần b2 td hết với khí Clo rồi cho sản phẩm vào 200 ml dd NaO 20% d=1,12g/ml. Tính c% chat tan có trong dd sau phản ứng
c. Tìm tên kim loại biet tỉ lệ số mol là 1:1 và khoi luong mol của kim loại này nặng hơn kim loại kia là 2,4lần
Giúp minh với nhé!
1 Gọi công thức oxit của kim loại hóa trị III là A2O3,ta có các phương trình sau
A2O3+3H2SO4--->A2(SO4)3+3H2O (1)
0,02 0,06 0,02
Vì sau phản ứng (1) dung dịch còn có thể phản ứng với CaCO3 giải phóng khí CO2=>axit H2SO4 dư,ta có phương trình
H2SO4+CaCO3--->CaSO4+CO2+H2O (2)
0,01 0,01 0,01 0,01
nCO2=0,224:22,4=0,01 mol
Khối lượng muối A2(SO4)3 sau khi cô cạn là
9,36-0,01x(40+96)=8 g
Ta thấy rằng A2O3=3,2 g,sau phản ứng tạo thành muối A2(SO4)3=8g Như vậy khối lượng tăng thêm là do 3 gốc -SO4 thay thế cho 3 nguyên tử Oxi,vậy khối lượng tăng thêm là 8-3,2 =4,8 g
nA2SO4=4,8:(96x3-16x3)=0,02 mol
=>khối lượng muối=0,02x(2xR+96x3)=8
=>R=56
R hóa trị III, có M=56=>R là Fe,công thức oxit là Fe2O3
nH2SO4=0,01+0,06=0,07 mol
mH2SO4=0,07x98=6,86g
C% dd H2SO4=(6,86:200)x100%=3,43%
2.
a/ Khí B: H2nH2O = 0.25 mol => nH2 = 0.25 mol
=> nH2/ B = 0.5 mol => nH+ = 1 mol = nHCl pứ = nCl- ( H+ + Cl- = HCl )
=> mCl- = 35.5g => m muối A = 35.5 + 18.4 = 53.9g
b/ m ( dd NaOH ) = 240g => m NaOH = 48g => n NaOH = 1.2 mol
H2 + Cl2 ---> 2HCl
0.5 1
NaOH + HCl --> NaCl + H2O
1 1 1 1
Khối lượng dd lúc này: 1*36.5 + 240 = 276.5 gam
mNaCl tạo thành = 58.5g => C% NaCl = 21.15%
%NaOH dư = ( 1.2 - 1 ) * 40 / 276.5 = 2.89%
c/ Gọi khối lượng mol của KL nhẹ hơn ( A ) là x => khối lượng mol của KL còn lại ( B ) là 2.4 * x
Vì số mol của 2 KL bằng nhau và bằng a mol
=> 3a + 2a = 5a = 1 mol => a = 0.2 mol ( KL hóa trị III td với 3 mol HCl, KL hóa trị II td 2 mol HCl )
=> 0.2*x + 0.2*2.4*x = 18.4 => x = 27.
A: Al
B: Zn
Anh giải đặt ẩn nhiều,trông hơi khó coi nên em trình bày cho đẹp nha!!Bài 2 còn 1 cách giải đấy em tự tìm tham khảo nha!!Chúc em học tốt!!
Đúng 0
Bình luận (2)
Thêm từ từ dd H2SO4 10% vào li đựng một muối cacbonat của kim loại hoá trị I,
cho tới khi vừa thoát hết khí CO2 thì thu được dd muối Sunfat có nồng độ 13,63%. Xác
định CTPT cuûa muối cacbonat?
cho 6,75 g một kim loại M chưa rõ hóa trị vào cốc đựng 392g dd H2SO4 10%,sau khi miếng kim loại tan hết thấy trong cốc dung dịch vẫn trong suốt và còn dd H2SO4 dư có nồng độ 0,62%.Xác định tên kim loại trên
Cho khí CO dư đi qua ống sứ nung nóng, chứa hỗn hợp gồm 2 oxit kim loại, thu được a gam chất rắn X và 1,12 lít khí CO2 (đktc). Cho toàn bộ X vào cốc đựng b gam dd H2SO4 10%(vừa đủ) đặt trên đĩa cân, phản ứng kết thúc số chỉ thị của cân là (a+b) gam, dd muối sau phản ứng có nồng độ 11,765% và còn lại 3,2 gam chất rắn không tan. Xác định 2 kim loại trong 2 oxit ban đầu (Các pứ xảy ra hoàn toàn).
Đọc tiếp
Cho khí CO dư đi qua ống sứ nung nóng, chứa hỗn hợp gồm 2 oxit kim loại, thu được a gam chất rắn X và 1,12 lít khí CO2 (đktc). Cho toàn bộ X vào cốc đựng b gam dd H2SO4 10%(vừa đủ) đặt trên đĩa cân, phản ứng kết thúc số chỉ thị của cân là (a+b) gam, dd muối sau phản ứng có nồng độ 11,765% và còn lại 3,2 gam chất rắn không tan. Xác định 2 kim loại trong 2 oxit ban đầu (Các pứ xảy ra hoàn toàn).
Cho hỗn hợp X vào H2SO4 thu được (a+b)g --> hh X gồm oxit kim loại A và kim loại B
Trong đó: oxit kim loại A ko bị khử bởi CO, kim loại B ko tan trong d.d H2SO4
-->Dễ suy ra kim loại B là Cu
(*)Giả sử oxit kim loại A là AO
AO+H2SO4-->ASO4+H2O
1..........1..........1 mol
m d.d sau pư=A+16+980=A+996 g
C% ASO4=11,765%
\(\Rightarrow\frac{A+96}{A+996}=0,11765\)
\(\Rightarrow A=24\left(Mg\right)\)
(*) Giả sử là A2O3 làm tương tự -->loại
Nếu ko chia trường hợp thì gọi là A2Ox hoặc AxOy
Đúng 0
Bình luận (0)
Bài : Trên 2 đĩa cân ở vị trí cân bằng có 2 cốc thủy tinh .Cốc thứ nhất đựng 100 g dd HCl 20% và cốc thứ 2 đựng 100 g dd NaOH 20% . Thêm 10 g muối NH4Cl vào cốc thứ 2 . Vậy cần phải thêm bao nhiêu g MgCO3 vào cốc thứ nhất để sau phản ứng 2 đĩa vẫn giữ đc cân bằng . Giả sử khí tạo ra đều thoát ra khỏi 2 cốc .
Cần gấp lắm , ai nhanh ngày nào mình cũng tick cho
















