Một oxit có công thức SOx. Trong phân tử này khối lượng S = khối lượng Oxi. Phân tử khối của oxit là 64 đvc. Hãy xác định CTHH ?

Những câu hỏi liên quan
Câu 1 Xác định công thức phân tử của oxit sắt biết nồng độ % theo khối lượng của Fe=70% còn lại là oxi Câu 2 cho biết nồng độ % theo khối lượng của các chất trong oxit là Al=52,94% còn lại là oxi Xác định công thức phân tử Câu 3 tìm CTHH của 1 oxit biết tỉ lệ về khối lượng là \(\dfrac{m_N}{m_O}\)=\(\dfrac{7}{12}\)
Câu 1 :
\(CT:Fe_xO_y\)
\(\%O=100-70=30\%\)
\(\dfrac{\%Fe}{\%O}=\dfrac{56x}{16y}=\dfrac{70}{30}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:Fe_2O_3\)
Đúng 2
Bình luận (0)
Câu 2 :
\(CT:Al_xO_y\)
\(\%O=100-52.94=47.06\%\)
Ta có :
\(\dfrac{27x}{16y}=\dfrac{\%Al}{\%O}=\dfrac{52.94}{47.06}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:Al_2O_3\)
Đúng 3
Bình luận (0)
Câu 3 :
\(CT:N_xO_y\)
Ta có :
\(\dfrac{m_N}{m_O}=\dfrac{7}{12}\Rightarrow\dfrac{14x}{16y}=\dfrac{7}{12}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:N_2O_3\)
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
Oxit Y có 30% oxi về khối lượng, còn lại là sắt. Biết phân tử khối của Y là 160 đvC. Hãy xác định công thức hóa học và tên gọi của Y.
%Fe = 100 - 30 = 70%
CT : FexOy
%Fe = 56x/ 160 * 100% = 70%
=> x = 2
%O = 16y/160 * 100% = 30%
=> y = 3
CTHH : Fe2O3 : Sắt (III) oxit
Đúng 1
Bình luận (0)
Oxit X có 22,3% oxi về khối lượng, còn lại là sắt. Biết phân tử khối của X là 72 đvC. Hãy xác định công thức hóa học và tên gọi của X.
Oxit : FexOy
Ta có : 56x + 16y = 72(1)
%O = 16y/(56x + 16y) .100% = 22,3%
=> 56x = 55,749y(2)
Từ (1)(2) suy ra x = y = 1
Vậy : CTHH là FeO(Sắt II oxit)
Đúng 1
Bình luận (0)
1.Oxit cao nhất của 1 nguyên tố R có dạng R2Ox. Phân tử khối của oxit là 102 đvC. Xác định R.
2. Cho biết phân tử khối của một oxit kim loại là 160, phần trăm khối lượng của kim loại trong
oxit là 70%. Lập công thức oxit đó.
1)
PTKR2Ox = 2.NTKR + 16x = 102 (đvC)
| x | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| NTKR | 43(Loại) | 35(Loại) | 27(Al) | 19(Loại) | 11(Loại) | 3(Loại) | Loại | Loại |
=> R là Al
2)
CTHH: RxOy
\(\%R=\dfrac{x.NTK_R}{160}.100\%=70\%\)
=> \(NTK_R=\dfrac{112}{x}\left(đvC\right)\)
Chỉ có x = 2 thỏa mãn \(NTK_R=\dfrac{112}{2}=56\left(đvC\right)\)
=> R là Fe
PTKFe2Oy = 160 (đvC)
=> y = 3
CTHH: Fe2O3
Đúng 2
Bình luận (0)
Câu 4 (1 điểm): Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%. Biết oxit này có khối lượng mol phân tử là 64 g/mol. Hãy tìm công thức hóa học của oxit đó.
Cho nguyên tử khối: O=16, Cu=64, Mg=24, Fe=56, Cl=35,5, Ag =108, N=14
\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=\dfrac{64.50}{100}=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2
Đúng 0
Bình luận (2)
hóa 8 Một oxit của sắt có khối lượng phân tử là 160g trong đó chiếm 70%khối lượng . Xác định công thức phân tử của oxit đó
Một oxit tạo thành bởi mangan và oxi, trong đó tỉ lệ khối lượng giữa mangan và oxi là 55:24. Hãy xác định công thức phân tử của oxi.
Gọi công thức tổng quát của oxit: M n x O y
Theo đề bài ta có:
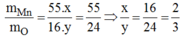
Vậy công thức phân tử của oxit là M n 2 O 3
Đúng 0
Bình luận (0)
Một oxit đồng, trong đó đồng chiếm 88,89% về khối lượng, và có phân tử khối là 144. Xác định công thức phân tử oxit đồng.
\(Đặt:Cu_xO_y\\ \Rightarrow\dfrac{m_{Cu}}{m_O}=\dfrac{88,89\%}{11,11\%}=\dfrac{8}{1}\\ \Leftrightarrow\dfrac{64x}{16y}=\dfrac{8}{1}\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{8.16}{64.1}=\dfrac{2}{1}\\ \Rightarrow\left\{{}\begin{matrix}x=2\\y=1\end{matrix}\right.\\ \Rightarrow CTHH:Cu_2O\)
Đúng 1
Bình luận (0)
một oxit của sắt có khối lượng phân tử là 160g/mol trong đó sắt chiếm 70‰ khối lượng . Xác định công thức phân tử của oxit đó biết Fe=56;O=16.(trả lời chi tiết giúp em với ![]() )
)
Gọi CTTQ : FexOy (x,y: nguyên, dương)
mFe= 70% . 160=112 => x=nFe=112/56=2
mO=160-112=48 -> y=nO=48/16=3
Với x=2;y=3 -> CTHH oxit sắt: Fe2O3
Đúng 2
Bình luận (0)
















