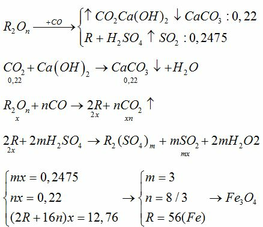Dẫn H2 dư qua bình chứa 16g một ôxit của kim loại R, sau phản ứng chỉ thu được 12,8g R. Tìm công thức của ôxit (RxOy)

Những câu hỏi liên quan
khử hoàn toàn 0,8 ôxit kim loại x cần dùng 336ml khí Hidro ở dktc cho khối lượng kim loại thu được phản ứng với dung dịch Axit Hcl Lấy dư thu được 224ml khí H2 (dktc) , Xác định công thức ôxit của kim loại x
MxOy+yH2\(\rightarrow\)xM+yH2O
\(n_{H_2}=\dfrac{\dfrac{336}{1000}}{22,4}=0,015mol\)
- Ta thấy: \(n_{O\left(oxit\right)}=n_{H_2}=0,015mol\)\(\rightarrow\)mO(oxit)=0,015.16=0,24 gam
\(\rightarrow\)mM(oxit)=0,8-0,24=0,56 gam
2M+2nHCl\(\rightarrow\)2MCln+nH2
\(n_{H_2}=\dfrac{\dfrac{224}{1000}}{22,4}=0,01mol\)
\(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,02}{n}mol\)
M=\(\dfrac{0,56n}{0,02}=28n\)
n=1\(\rightarrow\)M=28(loại)
n=2\(\rightarrow\)M=56(Fe)
n=3\(\rightarrow\)M=84(loại)
\(\rightarrow\)\(n_{Fe}=\dfrac{0,56}{56}=0,01mol\)
\(\dfrac{x}{y}=\dfrac{n_{Fe}}{n_O}=\dfrac{0,01}{0,015}=\dfrac{2}{3}\)
\(\rightarrow\)Fe2O3
Đúng 0
Bình luận (0)
Dẫn toàn bộ 2,24 lít H2 ở câu a qua bình đựng oxit kim loai của R hóa trị II nung nóng, sau khi phản ứng kết thúc thu được 12,8 kim loại R. Xác định công thức hóa học của oxit kim loại ?
Hóa học 8 :
Đốt cháy hoàn toàn 12,8g kim loại R hóa trị \(x\le3\)bằng một lượng õi vừa đủ thu được oxit (tạo bởi R và oxi) có khối lượng bằng 16g.
Xác định công thức của kim loại R và công thức oxit
a;2R + O2 →→2RO
b;Theo định luật BTKL ta có:
mR+mO=mRO
=>mO=8-4,8=3,2(g)
c;Theo PTHH ta có:
nR=nRO
<=>4,8R=8R+164,8R=8R+16
=>R=24
Vậy R là magie,KHHH là Mg
Dựa theo công thức bài này lm cậu nhé !
Dẫn khí CO dư đi qua 36 gam bột oxit kim loại R hóa trị II và nung nóng. Khi phản ứng xảy ra xong, dẫn toàn bộ khí CO2 lội qua dung dịch Ca(OH)2 dư thu được 50 gam kết tủa. Công thức oxit của kim loại R là : A. ZnO B. CuO C. FeO D. MgOghi rõ cách làm hộ mình nhé 3
Đọc tiếp
Dẫn khí CO dư đi qua 36 gam bột oxit kim loại R hóa trị II và nung nóng. Khi phản ứng xảy ra xong, dẫn toàn bộ khí CO2 lội qua dung dịch Ca(OH)2 dư thu được 50 gam kết tủa. Công thức oxit của kim loại R là :
A. ZnO B. CuO C. FeO D. MgO
ghi rõ cách làm hộ mình nhé <3
Đặt CTHH của oxit là RO
Ta có: \(n_{CaCO_3}=n_{kt}=\dfrac{50}{100}=0,5\left(mol\right)\)
PTHH:
\(RO+CO\xrightarrow[]{t^o}R+CO_2\)
0,5<-----------------0,5
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,5<-----0,5
\(\Rightarrow M_{RO}=\dfrac{36}{0,5}=72\left(g/mol\right)\\ \Rightarrow M_R=72-16=56\left(g/mol\right)\)
Vậy R là Fe. CTHH của oxit sắt là FeO
Chọn C
Đúng 2
Bình luận (0)
cho hơi nước qua than nung đỏ thu 2,24l khí có M =7,8 Mh2.Dẫn hỗn hợp qua RxOy ta thu kim loại(vừa đủ).cho kim loại R tác dụng hcl dư thu 1,792 l h2. xác định RxOy
Xét tất cả các quá trình thì cuối cùng chỉ có C và N thay đổi số oxi hóa. Bảo toàn electron —> 4nCO2 = 3nNO —> nCO2 = 0,045 nCaCO3 = 0,014, bảo toàn C —> nCa(HCO3)2 = 0,0155 Khi đun nước lọc: Ca(HCO3)2 —> CaCO3 + CO2 + H2O —> nCaCO3 = 0,0155 —> mCaCO3 = 1,55
Đúng 0
Bình luận (0)
Dẫn từ từ 0,5mol khí CO đi qua 28,8g hỗn hợp gồm R và RxOy nung nóng. Sau khi phản ứng hoàn toàn thu được khí A có dA/H2=20,4. Lượng kim loại sinh ra cho tác dụng hết với dung dich HCl dư thấy thoát ra 8,96 lít khí H2 (đktc). Viết PTHH của các PU xảy ra và tìm R?
Khử hoàn toàn 12,76 gam một oxit kim loại (RxOy) bằng khí CO vừa đủ thu được kim loại R và khí CO2. Hấp thụ hết khí CO2 sinh ra vào dung dịch Ca(OH)2 dư, thu được 22 gam kết tủa trắng. Cho toàn bộ lượng kim loại R thu được ở trên tác dụng hết với dung dịch H2SO4 đặc nóng, dư thu được 5,544 lít một khí có mùi hắc (đktc). Xác định công thức của RxOy
Đọc tiếp
Khử hoàn toàn 12,76 gam một oxit kim loại (RxOy) bằng khí CO vừa đủ thu được kim loại R và khí CO2. Hấp thụ hết khí CO2 sinh ra vào dung dịch Ca(OH)2 dư, thu được 22 gam kết tủa trắng. Cho toàn bộ lượng kim loại R thu được ở trên tác dụng hết với dung dịch H2SO4 đặc nóng, dư thu được 5,544 lít một khí có mùi hắc (đktc). Xác định công thức của RxOy
Dẫn 6,72 lít khí H2 (đktc) qua ống chứa 16g oxit KL (chưa rõ hoá trị) phản ứng xong thu đc m g kim loại và hơi .Xác định CTHH của oxit đem dùng
Gọi tên kim loại là A
AxOy + yH2 => xA + yH2O
VH2 = 6.72l => nH2 = V/22.4 = 0.3 (mol)
===> nAxOy = 0.3/y (mol)
Ta có: Ax + 16y = m/n = 16/(0.3/y)
==> Ax + 16y = 160/3y
==> Ax = 112/3y
===> A = \(\frac{112}{3}.\frac{y}{x}\)
Nếu x = 1, y = 1 ==> Loại
Nếu x = 2, y = 1 ==> Loại
Nếu x = 2, y = 3 ==> A = 56 (Nhận)
Vậy CT: Fe2O3. Kim loại là Fe
Đúng 0
Bình luận (0)
cho kim loại Al có dư vào dd HCl 2M. Sau phản ứng dẫn khí sinh ra qua ống nghiệm có chứa 16g CuO đun nóng thực hiện phản ứng khử, thu được 11,25g kim loại Cu.
a) Tính hiệu suất phản ứng khử trên.
b)Tìm khối lượng dd HCl dùng? (D HCl=1,2g/mL)
a, \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: \(n_{Cu\left(LT\right)}=n_{CuO}=0,2\left(mol\right)\)
\(\Rightarrow m_{Cu\left(LT\right)}=0,2.64=12,8\left(g\right)\)
\(\Rightarrow H=\dfrac{11,25}{12,8}.100\%\approx87,89\%\)
b, \(n_{H_2}=n_{CuO}=0,2\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow V_{ddHCl}=\dfrac{0,4}{2}=0,2\left(l\right)=200\left(ml\right)\)
\(\Rightarrow m_{ddHCl}=200.1,2=240\left(g\right)\)
Đúng 1
Bình luận (0)