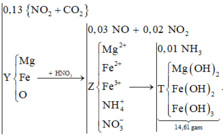
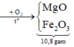
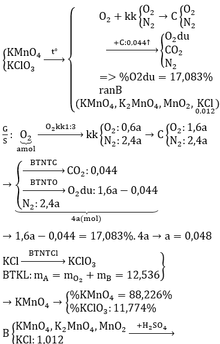
trong một bình kín chưa 11,2l khí hỗn hợp A ở đktc gồm CO2 và O2 A có tỉ khối so với H2 là 18,4 cho mẩu Zn nặng 13 g vào A và nung đến phản ứng hoàn toàn
a tính số mol mối chất khí
b tính khối lượng kễm oxit
c tính % về thể tích khí còn lại sau phản ứng