Tính số mol của 22g hỗn hợp Al và Fe

Những câu hỏi liên quan
Cho 22g hỗn hợp Al, Fe vào dung dịch có 0,6 mol HCl. Chứng minh rằng hỗn hợp không tan hết.
PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2
Fe + 2HCl -> FeCl2 + H2
Giả sử hh chỉ gồm Fe
nFe = \(\dfrac{22}{56}\approx0,4\left(mol\right)\)
Ta có tỉ lệ : \(\dfrac{n_{Fe}}{1}=0,4\) > \(\dfrac{n_{HCl}}{2}=\dfrac{0,6}{2}=0,3\)
=>Fe dư, HCl hết
hay hh ko tan hết
Đúng 0
Bình luận (0)
Tính khối lượng của Al và Fe có trong 11 gam hỗn hợp Al và Fe. Biết trong hỗn hợp đó, số mol của Al gấp 2lần số mol của Fe
Gọi số mol của Al và Fe lần lượt là x và y
Vì số mol của Al gấp 2 lần Fe nên x=2y (1)
Và khối lượng của Fe và Al là 11g nên
27x+56y=12 (2)
Giải HPT: \(\left\{{}\begin{matrix}\text{27x+56y=12 }\\\text{x=2y }\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}\text{x=0,2 mol}\\\text{y=0,1 mol}\end{matrix}\right.\)
\(\rightarrow\)mAl=27.0,2=5,4
mAl=56.0,1=5,6
tính số mol hỗn hợp x gồm 11.2 gam fe và 3,24 gam al
Ta có:
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{Al}=\dfrac{3,24}{27}=0,12\left(mol\right)\)
Nên số mol của hỗn hợp X là:
\(n_X=n_{Fe}+n_{Al}=0,2+0,12=0,32\left(mol\right)\)
Đúng 3
Bình luận (0)
Cho 22g hỗn hợp al ,fe phản ứng hoàn toàn với H2SO4 thu được 20.16 lít SO2 sản phẩm khử duy nhất ở dktc và dung dịch A a) tính khối lượng của mỗi kim loại trong hỗn hợp b) cô cạn dung dịch A thì thu được bao nhiêu gam muối khan
- Gọi số mol Al và Fe trong hốn hợp lần lượt là a, b mol
PTKL : 27a + 56b = 22
BTe : 3a + 3b = 1,8
=> a = 0,4 và b = 0,2 .
=> mAl = 10,8g và mFe = 11,2 g
b, Sau phản ứng thu được muối Al2(SO4)3 và Fe2(SO4)3 .
=> mM = 108,4g
Đúng 3
Bình luận (0)
\(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(\Rightarrow27a+56b=22\left(1\right)\)
\(n_{SO_2}=\dfrac{20.16}{22.4}=0.9\left(mol\right)\)
\(2Fe+6H_2SO_{4\left(đ\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(2Al+6H_2SO_{4\left(đ\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(n_{SO_2}=1.5a+1.5b=0.9\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.4,b=0.2\)
\(m_{Al}=0.4\cdot27=10.8\left(g\right)\)
\(m_{Fe}=11.2\left(g\right)\)
\(m_{Muối}=0.2\cdot342+0.1\cdot400=108.4\left(g\right)\)
Đúng 3
Bình luận (0)
Cho 13,7 g Fe và Al tác dụng với HCL thu được 24,64 lít đkc .Tính thành phần phần trăm số mol của Al trong hỗn hợp ban đầu?
Xem chi tiết
Gọi : \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)⇒ 56x + 27y = 13,7(1)
\(Fe + 2HCl \to FeCl_2 + H_2\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\)
Theo PTHH :
\(n_{H_2} = x + 1,5y = \dfrac{24,64}{22,4} = 1,1(2)\)
Từ (1)(2) suy ra : x = -0,16<0
(Sai đề)
Đúng 1
Bình luận (0)
em cần gấp nhờ giúp cái ạ F22: Tính số mol mỗi kim loại ? Biết :a. 9,96 gam hỗn hợp X ( Fe , Al có tỷ lệ mol 1 : 1) .b. 27,6 gam hỗn hợp Y ( Fe , Cu có tỷ lệ mol 1 : 2) .c. 29,52 gam hỗn hợp Z ( Cu, Al có tỷ lệ mol 3 : 2 ) . F23: 11 gam hỗn hợp X (Al, Fe) có tổng số mol là 0,3. Tính khối lượng mỗi kim loại ?
Đọc tiếp
em cần gấp nhờ giúp cái ạ ![]()
F22: Tính số mol mỗi kim loại ? Biết :
a. 9,96 gam hỗn hợp X ( Fe , Al có tỷ lệ mol 1 : 1) .
b. 27,6 gam hỗn hợp Y ( Fe , Cu có tỷ lệ mol 1 : 2) .
c. 29,52 gam hỗn hợp Z ( Cu, Al có tỷ lệ mol 3 : 2 ) .
F23: 11 gam hỗn hợp X (Al, Fe) có tổng số mol là 0,3. Tính khối lượng mỗi kim loại ?
F22: Tính số mol mỗi kim loại ? Biết :
a. 9,96 gam hỗn hợp X ( Fe , Al có tỷ lệ mol 1 : 1) .
Gọi x, y lần lượt là số mol Fe, Al
\(\left\{{}\begin{matrix}56x+27y=9,96\\x=y\end{matrix}\right.\)
=> x=y= 0,12(mol)
b. 27,6 gam hỗn hợp Y ( Fe , Cu có tỷ lệ mol 1 : 2) .
Gọi x, y lần lượt là số mol Fe, Cu
\(\left\{{}\begin{matrix}56x+64y=27,6\\\dfrac{x}{y}=\dfrac{1}{2}\end{matrix}\right.\)
=> x= 0,15; y=0,3
c. 29,52 gam hỗn hợp Z ( Cu, Al có tỷ lệ mol 3 : 2 ) .
Gọi x, y lần lượt là số mol Cu, Al
\(\left\{{}\begin{matrix}64x+27y=29,52\\\dfrac{x}{y}=\dfrac{3}{2}\end{matrix}\right.\)
=> x= 0,36 ; y=0,24
F23: 11 gam hỗn hợp X (Al, Fe) có tổng số mol là 0,3. Tính khối lượng mỗi kim loại ?
Gọi x, y lần lượt là số mol Al, Fe
\(\left\{{}\begin{matrix}27x+56y=11\\x+y=0,3\end{matrix}\right.\)
=> x=0,2 , y =0,1
=> \(\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
cho hỗn hợp X gồm Ag, Cu, Fe, Al. Biết tỉ lệ số mol của Fe và Al (Fe:Al 3 :8). đem nung nóng 20,1g hỗn hợp X trong không khí thu được 26,1g hỗn hợp các chất rắn Y. Giả sử tác dụng của Fe và oxi chỉ tạo ra Fe3O4. Đem hòa tan hỗn hợp Y bằng dung dịch HCl dư thấy chỉ còn lại 1 chất rắn ko tan là 8,1 g
a, Viết phương trình
b, tính phần trăm theo khối lượng các chất trong hỗn hợp X
c, tính khối lượng các oxit và muối được tạo thành sau phản ứng
Đọc tiếp
cho hỗn hợp X gồm Ag, Cu, Fe, Al. Biết tỉ lệ số mol của Fe và Al (Fe:Al= 3 :8). đem nung nóng 20,1g hỗn hợp X trong không khí thu được 26,1g hỗn hợp các chất rắn Y. Giả sử tác dụng của Fe và oxi chỉ tạo ra Fe3O4. Đem hòa tan hỗn hợp Y bằng dung dịch HCl dư thấy chỉ còn lại 1 chất rắn ko tan là 8,1 g a, Viết phương trình
b, tính phần trăm theo khối lượng các chất trong hỗn hợp X c, tính khối lượng các oxit và muối được tạo thành sau phản ứng
Hãy tính:
a) Số mol của : 28g Fe 64g Cu 5,4g Al.
b) Thể tích khí (đktc) của 0,175 mol CO2; 1,25 mol H2; 3 mol N2.
c) Số mol và thể tích của hỗn hợp khí (dktc) gồm có 0,44g CO2 0,04g H2 và 0,56g N2.
a)
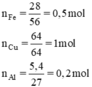
b) VCO2 = 22,4 .0,175 = 3,92l.
VH2 = 22,4 .1,25 = 28l.
VN2 = 22,4.3 = 67,2l.
c) Số mol của hỗn hợp khí bằng tổng số mol của từng khí.
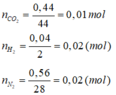
nhh = nCO2 + nH2 + nN2 = 0,01 + 0,02 + 0,02 = 0,05 mol
Vhh khí = (0,01 + 0,02 + 0,02) . 22,4 = 1,12l.
Đúng 0
Bình luận (0)
a)Tính thể tích(đktc) của: 0,75 mol khí H2S; 12,8g khí SO2; 3,2 g khí oxi.
b) Tính số mol và thể tích hỗn hợp khí ( đktc) gồm: 22g CO2; 3,55 g Cl2; 0,14g N2
a.
\(V_{H_2S}=0.75\cdot22.4=16.8\left(l\right)\)
\(V_{SO_2}=\dfrac{12.8}{64}\cdot22.4=4.48\left(l\right)\)
\(V_{O_2}=\dfrac{3.2}{32}\cdot22.4=2.24\left(l\right)\)
b.
\(n_{hh}=\dfrac{22}{44}+\dfrac{3.55}{71}+\dfrac{0.14}{28}=0.555\left(mol\right)\)
\(V_{hh}=0.555\cdot22.4=12.432\left(l\right)\)
Đúng 1
Bình luận (0)

























