Cân bằng pứ oxi hóa = phương pháp cân bằng e, xác định chất khử, chất oxi hóa
NH4N03 →→ N2 + O2 + H2O
KMnO4 + HCl →→ KCl + MnCl + H2O + Cl2
Cân bằng pứ oxi hóa = phương pháp cân bằng e, xác định chất khử, chất oxi hóa
NH4 \(\rightarrow\) N2 + O2 + H2O
KMnO4 + HCl \(\rightarrow\) KCl + MnCl + H2O
NH4NO3 → N2 + O2 + H2O
KMnO4 + HCl →KCl + MnCl + Cl2 + H2O
SAI HẾT THÌ FAI
Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
1) KClO3+HCl --> KCl +Cl2+H2O
2)K2Cr2O7 +HCl -->KCl+CrCl3 +Cl2+H2O
3) KMnO4 +HCl --> KCl+MnCl2+Cl2+H2O
4)Al+HNO3 --> Al(NO3)3+N2O+H2O
5)Fe3O4 +HNO3 -->Fe(NO3)3 +NO+H2O
6) FeS +O2 --> Fe2O3 +SO2
giúp mình với
Câu 1: Cân bằng phản ứng oxi hóa khử sau theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, sự oxi hóa, sự khử:
(1) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
(2) HNO3 + Cu→ Cu(NO3)2 + NO2 + H2O 80
(3) NH3 + O2 NO + H2O
(1) \(K\overset{+7}{Mn}O_4+H\overset{-1}{Cl}\rightarrow KCl+\overset{+2}{Mn}Cl_2+\overset{0}{Cl_2}+H_2O\)
- Chất khử: HCl
Chất oxh: KMnO4
- Sự oxh: \(2Cl^{-1}\rightarrow Cl_2^0+2e|\times5\)
Sự khử: \(Mn^{+7}+5e\rightarrow Mn^{+2}|\times2\)
\(\rightarrow2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
(2) \(H\overset{+5}{N}O_3+\overset{0}{Cu}\rightarrow\overset{+2}{Cu}\left(NO_3\right)_2+\overset{+4}{N}O_2+H_2O\)
- Chất khử: Cu
Chất oxh: HNO3
- Sự khử: \(N^{+5}+1e\rightarrow N^{+4}|\times2\)
Sự oxh: \(Cu^0\rightarrow Cu^{+2}+2e|\times1\)
\(\rightarrow4HNO_3+Cu\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\)
(3) \(\overset{-3}{N}H_3+\overset{0}{O_2}\rightarrow\overset{+2}{N}\overset{-2}{O}+H_2O\)
- Chất khử: NH3
Chất oxh: O2
- Sự khử: \(O_2^0+4e\rightarrow2O^{-2}|\times5\)
Sự oxh: \(N^{-3}\rightarrow N^{+2}+5e|\times4\)
\(\rightarrow4NH_3+5O_2\rightarrow4NO+6H_2O\)
Xác định số oxi hóa, tìm chất khử, chất oxi hóa; sự khử, sự oxi hóa và cân bằng các p/ ứng oxi hóa khử sau theo phương pháp thăng bằng electron: 1. NH3 + O2 → N2 + H2O
2. NH3 + O2 → NO + H2O
3. CH4 + O2 → CO2 + H2O
4. NH3 + CuO → Cu + N2 + H2O
5. P + KClO3 → P2O5 + KCl
6. S + HNO3 → H2SO4 + NO
7. Fe2O3 + CO → Fe + CO2
8. SO2 + Br2 + H2O → H2SO4 + HBr
9. MnO2 + HCl → MnCl2 + Cl2 + H2O
10. KClO4 + C → KCl + CO
Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
a) Al + Fe3O4 → Al2O3 + Fe
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
c) FeS2 + O2 → Fe2O3 + SO3
d) KClO3 → KCl + O2
e) Cl2 +KOH → KCl + KClO3 + H2O
Cân bằng các phương trình phản ứng oxi hóa – khử:
![]()
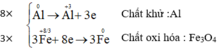
![]()
![]()

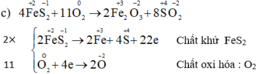

Anh chị hãy cân bằng phương trình phản ứng bằng phương pháp thăng bằng electron và chỉ rõ chất oxi hóa, chất khử, quá trình oxi hóa, quá trình khử của a)KClO3 + HCl -> KCL + Cl2 + H2O
b)KMnO4 -> K2MnO4+MnO2+O2
a) KClO3 + 6HCl --> KCl + 3Cl2 + 3H2O
Chất khử: HCl, chất oxh: KClO3
| QT khử | Cl+5 + 6e --> Cl-1 | x1 |
| QT oxh | 2Cl-1 - 2e --> Cl20 | x3 |
b) 2KMnO4 --to--> K2MnO4 + MnO2 + O2
Chất khử: KMnO4, chất oxh: KMnO4
| QT khử | 2Mn+7 + 4e --> Mn+6 + Mn+4 | x1 |
| QT oxh | 2O-2 - 4e --> O20 | x1 |
\(a.QToxh:2\overset{-1}{Cl}\rightarrow Cl_2+2e|\times5\\QTkhử:2\overset{+5}{Cl}+10e\rightarrow \overset{0}{Cl_2}|\times1\)
HCl là chất oxi hóa, KClO3 là chất khử
\(KClO_3+6HCl_{đặc}\rightarrow KCl+3Cl_2+3H_2O\)
\(b.QToxh:2\overset{-2}{O}\rightarrow\overset{0}{O_2}+4e|\times1\\ QTkhử:2\overset{+7}{Mn}+4e\rightarrow\overset{+6}{Mn}+\overset{+4}{Mn}|\times1\)
KMnO4 vừa là chất khử, vừa là chất oxi hóa
\(2KMnO_4-^{t^o}\rightarrow K_2MnO_4+MnO_2+O_2\)
Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
e) Cl2 +KOH → KCl + KClO3 + H2O
b) 2FeSO4 + 2KMnO4 + 3H2SO4 → Fe2(SO4)3 + 2MnSO4 + K2SO4 + 3H2O
e) Cl2 +2KOH → KCl + KClO3 + H2O
Xác định chất oxi hóa, chất khử, quá trình oxi hóa, quá trình khử và cân bằng phản ứng sau:
1. NH3 + Cl2 → N2 + HCl
2NH3 + 3Cl2 --> N2 + 6HCl
Chất oxh: Cl2
Chất khử: N2
| QT oxh | 2N-3 -6e --> N20 | x1 |
| QT khử | Cl20 +2e --> 2Cl-1 | x3 |
Cân bằng phản ứng oxi hóa- khử sau bằng phương pháp thăng bằng
electron. Xác định chất oxi hóa, chất khử và môi trường (nếu có):
a. Al + Fe2O3 → Al2O3 + Fe
b. Al + HNO3 → Al(NO3)3 + N2↑ + H2O
a) 2Al + Fe2O3 -to-> Al2O3 + 2Fe
Chất khử: Al
Chất oxi hóa: Fe2O3
| 2Al0-6e->Al2+3 | x1 |
| Fe2+3+6e->2Fe0 | x1 |
b) 10Al + 36HNO3 --> 10Al(NO3)3 + 3N2 + 18H2O
Chất khử: Al
Chất oxi hóa: HNO3
Môi trường: HNO3
| Al0-3e->Al+3 | x10 |
| 2N+5+10e->N20 | x3 |