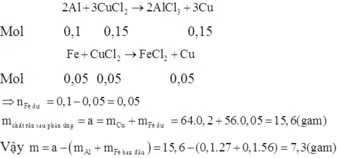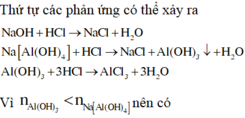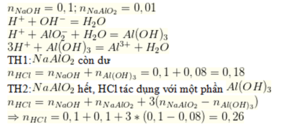cho 0,1 mol Al; 0,2 mol Fe; 0,3 mol Zn tac dụng với 0,5 mol AgNO3; 0,6 mol Cu(NO3)2. Tính số mol chất dư còn lại

Những câu hỏi liên quan
Cho 0,1 mol kim loại Na Ca Al Ag tác dụng với tối đa bao nhiêu mol O2
4Na+O2-to>2Na2O
2Ca+O2-to>2CaO
4Al+3O2-to>2Al2O3
=> cần ít nhất 2nO2 =0,2 mol
Đúng 2
Bình luận (0)
Cho hỗn hợp X gồm 0,1 mol Fe và 0,1 mol Al tác dụng với dung dịch chứa 0,2 mol CuCl2 đến khi phản ứng hoàn toàn thấy khối lượng chất rắn tăng m gam. Giá trị của m là: A. 7,3 B. 4,5 C. 12,8 D. 7,7
Đọc tiếp
Cho hỗn hợp X gồm 0,1 mol Fe và 0,1 mol Al tác dụng với dung dịch chứa 0,2 mol CuCl2 đến khi phản ứng hoàn toàn thấy khối lượng chất rắn tăng m gam. Giá trị của m là:
A. 7,3
B. 4,5
C. 12,8
D. 7,7
5,4 gam Al tương ứng với bao nhiêu mol biết rằng nguyên tử khối của Al = 27 đvC ?
A.
0,1 mol
B.
1 mol
C.
0,2 mol
D.
2 mol
Xem thêm câu trả lời
Để đốt cháy hoàn toàn hỗn hợp gồm 0,1 mol Ca, 0,2 mol Na, 0,3 mol Al, 0.1 miol Mg thì cần cho phản ứng đốt cháy là
Cho 0,1 mol Al tác dụng vừa đủ với dung dịch HCl. Tính khối lượng AlCl3 thu được sau phản ứng? (Al = 27; Cl = 35,5)
So sánh V khí hidro (đktc) trong mối trườg hợp sau:
+ 0,1 mol Zn tác dụng vs dd H2SO4 dư
+0,1 mol Al tác dụng vs dd H2SO4 dư
( cho Zn = 65;Al=27;S=32;H=1;Cl=35,5;P=31;O=16
Zn + H2SO4 \(\rightarrow\) ZnSO4 + H2 (1)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (2)
Theo PT(1) => nH2(PT1) = nZn = 0,1(mol)
=> VH2(PT1) = 0,1 . 22,4 = 2,24(l)
Theo PT(2) => nH2(PT2) = 3/2 . nAl = 3/2 . 0,1 = 0,15(mol)
=> VH2(PT2) = 0,15 .22,4 = 3,36(l)
Thấy VH2(PT1) < VH2(PT2) ( vì 2,24< 3,36)
Đúng 0
Bình luận (0)
Thêm dung dịch HCl vào dung dịch hỗn hợp gồm 0,1 mol NaOH và 0,1 mol Na[Al(OH)4] thu được 0,08 mol chất kết tủa. Số mol HCl đã thêm vào là A. 0,16 mol B. 0,18 hoặc 0,26 mol C. 0,08 hoặc 0,16 mol D. 0,26 mol
Đọc tiếp
Thêm dung dịch HCl vào dung dịch hỗn hợp gồm 0,1 mol NaOH và 0,1 mol Na[Al(OH)4] thu được 0,08 mol chất kết tủa. Số mol HCl đã thêm vào là
A. 0,16 mol
B. 0,18 hoặc 0,26 mol
C. 0,08 hoặc 0,16 mol
D. 0,26 mol
Thêm dung dịch HCl vào dung dịch hỗn hợp gồm 0,1 mol NaOH và 0,1 mol Na[Al(OH)4] thu được 0,08 mol chất kết tủa. Số mol HCl đã thêm vào là
A. 0,16 mol
B. 0,18 hoặc 0,26 mol
C. 0,08 hoặc 0,16 mol
D. 0,26 mol
Hòa tan một hỗn hợp chứa 0,1 mol Mg và 0,1 mol Al vào dung dịch hỗn hợp chứa 0,1 mol Cu(NO3)2 và 0,35 mol AgNO3. Khi phản ứng xảy ra hoàn toàn thì khối lượng (gam) chất rắn thu được là: A. 21,6 B. 37,8 C. 42,6 D. 44,2
Đọc tiếp
Hòa tan một hỗn hợp chứa 0,1 mol Mg và 0,1 mol Al vào dung dịch hỗn hợp chứa 0,1 mol Cu(NO3)2 và 0,35 mol AgNO3. Khi phản ứng xảy ra hoàn toàn thì khối lượng (gam) chất rắn thu được là:
A. 21,6
B. 37,8
C. 42,6
D. 44,2