Hìa tan hoàn toàn 6,66g tinh thể Al2(SO4)3.xH2O vào nước thành dung dịch A . Lấy 1/10 dung dịch A cho tác dụng với dung dịch BaCl2 dư thì thu được 0,699g kết tủa. Hãy xác định công thức của tinh thể muối sunfat nhôm ngậm nước ở trên.

Những câu hỏi liên quan
Hòa tan hết 6,66 g tinh thể Al2(SO4)3.nH2O vào trong nước được dung dịch A. Lấy 1/10 dung dịch A cho tác dụng với BaCl2 thu được 0,699 g kết tủa. Xác định CT của hiđrat trên
3BaCl2 + Al2(SO4)3→ 3BaSO4 + 2AlCl3
nBaSO4=\(\frac{0,699}{137+32+16.4}=0,003\) mol
theo PT => nAl2(SO4)3=0,001mol
vì lấy 1/10=> nAl2(SO4)3 ban đầu=0,01 mol
=>MAl2(SO4)3.nH2O=\(\frac{6,66}{0,01}=666\)
=> 27.2+3(32+16.4)+18n=666
<=>n=18
vậy công thức hidrat trên là Al2(SO4)3.18H2O
Đúng 0
Bình luận (0)
Hòa tan 26,64 gam chất tinh thể muối sunfat của kim loại M vào nước dung dịch X. Cho X tác dụng với dung dịch NH3 vừa đủ thu được kết tủa Y, nung Y ở nhiệt độ cao đến khối lượng không đổi được 4,08 gam oxit. Mặt khác, cho X tác dụng với dung dịch BaCl2 dư được 27,96 gam kết tủa. Công thức tnh thể trên là A.CuSO4.6H2O B. Fe2(SO4)3.12H2O C. Al2(SO4)3.24H2O D. Al2(SO4)3.18H2O
Đọc tiếp
Hòa tan 26,64 gam chất tinh thể muối sunfat của kim loại M vào nước dung dịch X. Cho X tác dụng với dung dịch NH3 vừa đủ thu được kết tủa Y, nung Y ở nhiệt độ cao đến khối lượng không đổi được 4,08 gam oxit. Mặt khác, cho X tác dụng với dung dịch BaCl2 dư được 27,96 gam kết tủa. Công thức tnh thể trên là
A.CuSO4.6H2O
B. Fe2(SO4)3.12H2O
C. Al2(SO4)3.24H2O
D. Al2(SO4)3.18H2O
1.Cho a gam hỗn hợp gồm 2 kim loại A và B( chưa rõ hóa trị) tác dụng hết với dung dịch HCl (cả A và B đều phản ứng)sau khi phản ứng kết thúc người ta chỉ thu được 67g muối và 8.96l H2 ở ĐKTC
a) Viết các PTHH
b) Tính a
2.Hòa tan 6.6g tinh thể Al2(SO4)3.nH2O vào nước thành dung dịch A. Lấy 1/10 dung dịch A cho tác dụng với dung dịch BaCl2 dư thì thu được 0.699g kết tủa. Xác định công thức của tinh thể muối sunfat của nhôm
Đọc tiếp
1.Cho a gam hỗn hợp gồm 2 kim loại A và B( chưa rõ hóa trị) tác dụng hết với dung dịch HCl (cả A và B đều phản ứng)sau khi phản ứng kết thúc người ta chỉ thu được 67g muối và 8.96l H2 ở ĐKTC
a) Viết các PTHH
b) Tính a
2.Hòa tan 6.6g tinh thể Al2(SO4)3.nH2O vào nước thành dung dịch A. Lấy 1/10 dung dịch A cho tác dụng với dung dịch BaCl2 dư thì thu được 0.699g kết tủa. Xác định công thức của tinh thể muối sunfat của nhôm
Đưa vào sổ tay
hòa tan 27,8 gam tinh thể MSO4.nH2O vào nước thu được V ml dung dịch A cho Ba(NO3)2 vào V dung dịch A thì thu được 23,3 gam kết tủa mặt khác cho NaOH dư vào Vml dung dịch A thì thu được 9 gam kết tủa xác định công thức tinh thể trênMSO4 + Ba(NO3)2 => BaSO4 + M(NO3)2
0,1 <--------------------- 0,1
nBaSO4 = 0,1mol
MSO4 + 2NaOH => Na2SO4 + M(OH)2
0,1-------------------------------------> 0,1
MM(OH)2= \(\frac{9}{0,1}\) = 90 => M=56 => Fe
=> công thức FeSO4.nH2O
n tinh thể = nFeSO4 = 0,1
=> M tinh thể = 27,8/0,1= 278
<=> 152 + 18n = 278 => n= 7
=> FeSO4.7H2O
Đúng 0
Bình luận (0)
Hòa tan 4,53 gam một muối kép X có thành phần: Al3+, NH4+, SO42- và H2O kết tinh vào nước cho đủ 100ml dung dịch Y - Lấy 20ml dung dịch Y tác dụng với dung dịch NH3 dư thu được 0,156 gam kết tủa. - Lấy 20ml dung dịch Y cho tác dụng với dung dịch Ba(OH)2 dư, đun nóng được 0,932 gam kết tủa. Công thức của X là: A. Al.NH4(SO4)2.12H2O B. Al2(SO4)3.2(NH4)2SO4.16H2O C. 2Al2(SO4)3.(NH4)2SO4.5H2O D. Al2(SO4)3.(NH4)2SO4.12H2O
Đọc tiếp
Hòa tan 4,53 gam một muối kép X có thành phần: Al3+, NH4+, SO42- và H2O kết tinh vào nước cho đủ 100ml dung dịch Y
- Lấy 20ml dung dịch Y tác dụng với dung dịch NH3 dư thu được 0,156 gam kết tủa.
- Lấy 20ml dung dịch Y cho tác dụng với dung dịch Ba(OH)2 dư, đun nóng được 0,932 gam kết tủa.
Công thức của X là:
A. Al.NH4(SO4)2.12H2O
B. Al2(SO4)3.2(NH4)2SO4.16H2O
C. 2Al2(SO4)3.(NH4)2SO4.5H2O
D. Al2(SO4)3.(NH4)2SO4.12H2O
Đáp án A
Gọi số mol Al3+, NH4+, SO42- trong 100 ml dung dịch Y lần lượt là x, y, z mol
-Phần 1:
Al3++ 3NH3+ 3H2O→ Al(OH)3+ 3NH4+
x/5 x/5 = 2.10-3 suy ra x = 0,01 mol
-Phần 2:
Ba2++ SO42-→ BaSO4
z/5 mol z/5 mol = 0,932/233 = 4.10-3 mol nên z = 0,02 mol
ĐLBT ĐT suy ra y = 0,01 mol suy ra nH2O = 0,12 mol
Suy ra CT là Al.NH4.(SO4)2.12H2O
Đúng 0
Bình luận (0)
1. Hoà tan hoàn toàn 6,66g tinh thể Al2(SO4)3 . nH2O vào nc thành dung dịch A. Lấy 1/10 dung dịch A cho tác dụng với dung dịch BaCl2 dư thì thu dc 0,699g kết tủa. Xác định công thức của tinh thể muối sunfat của nhôm.
2. Hoà tan 24,4g BaCl2.xH2O vào 175,6g nc thì thu dc dung dịch 10,4%. Tính x.
3. Cô cạn rất từ từ 200ml dung dịch CuSO4 0,2M thu dc 10g tinh thể CuSO4. pH2O. Tính P
Đọc tiếp
1. Hoà tan hoàn toàn 6,66g tinh thể Al2(SO4)3 . nH2O vào nc thành dung dịch A. Lấy 1/10 dung dịch A cho tác dụng với dung dịch BaCl2 dư thì thu dc 0,699g kết tủa. Xác định công thức của tinh thể muối sunfat của nhôm.
2. Hoà tan 24,4g BaCl2.xH2O vào 175,6g nc thì thu dc dung dịch 10,4%. Tính x.
3. Cô cạn rất từ từ 200ml dung dịch CuSO4 0,2M thu dc 10g tinh thể CuSO4. pH2O. Tính P
Bài 3:
\(n_{CuSO_4}=0,2\times0,2=0,04\left(mol\right)\)
Ta có: \(n_{CuSO_4.pH_2O}=0,04\left(mol\right)\)
\(\Rightarrow M_{CuSO_4.pH_2O}=\frac{10}{0,04}=250\left(g\right)\)
\(\Leftrightarrow160+18p=250\)
\(\Leftrightarrow18p=90\)
\(\Leftrightarrow p=5\)
Đúng 0
Bình luận (0)
Bài 2:
\(n_{BaCl_2.xH_2O}=\frac{24,4}{208+18x}\left(mol\right)\)
Ta có: \(n_{BaCl_2}=n_{BaCl_2.xH_2O}=\frac{24,4}{208+18x}\left(mol\right)\)
\(\Rightarrow m_{BaCl_2}=\frac{24,4}{208+18x}\times208=\frac{5075,2}{208+18x}\left(g\right)\)
ta có: \(m_{ddBaCl_2}mới=24,4+175,6=200\left(g\right)\)
\(C\%_{BaCl_2}mới=\frac{5075,2}{208+18x}\div200\times100\%=10,4\%\)
\(\Leftrightarrow\frac{5075,2}{41600+3600x}=0,104\)
\(\Leftrightarrow5075,2=4326,4+374,4x\)
\(\Leftrightarrow748,8=374,4x\)
\(\Leftrightarrow x=2\)
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
Hòa tan hoàn toàn 6,66g tinh thể Al2(SO3)3. n H2O vào nước đc dung dịch A Lấy 1/10 dung dịch A cho tác dụng với BaCl2 dư thì thu đc 0,699g kết tủa. Xác định CT tinh thể muối sunfat
giúp tui vs![]()
Hòa tan hoàn toàn một lượng AlCl3 và một lượng Al2(SO4)3 vào nước thu được 200 gam dung dịch X, chia dung dịch X thành hai phần: – Phần 1: cho tác dụng với BaCl2 dư thu được 13,98 gam kết tủa trắng. – Phần 2: cho tác dụng với 476 ml dung dịch Ba(OH)2 1M, sau khi phản ứng xong thu được 69,024 gam kết tủa. Biết khối lượng phần 2 gấp n lần khối lượng phần 1 (n là số nguyên dương) và lượng chất tan trong phần 2 nhiều hơn lượng chất tan trong phần 1 là 32,535 gam. Tính nồng độ phần trăm của các chất...
Đọc tiếp
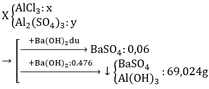
Hòa tan hoàn toàn một lượng AlCl3 và một lượng Al2(SO4)3 vào nước thu được 200 gam dung dịch X, chia dung dịch X thành hai phần:
– Phần 1: cho tác dụng với BaCl2 dư thu được 13,98 gam kết tủa trắng.
– Phần 2: cho tác dụng với 476 ml dung dịch Ba(OH)2 1M, sau khi phản ứng xong thu được 69,024 gam kết tủa. Biết khối lượng phần 2 gấp n lần khối lượng phần 1 (n là số nguyên dương) và lượng chất tan trong phần 2 nhiều hơn lượng chất tan trong phần 1 là 32,535 gam.
Tính nồng độ phần trăm của các chất có trong dung dịch X.
Cho Ba(OH)2 vào muối Al sẽ có 2TH sau:
TH1: kết tủa Al(OH)3 chưa bị hòa tan
Al3+ + 3OH– → Al(OH)3↓
→ nAl(OH)3 = nAl3+ → nAl(OH)3 = xn + 0,04n
TH2: kết tủa Al(OH)3 bị hòa tan một phần
Al3+ + 3OH– → Al(OH)3↓
(xn + 0,04n)→ 3(xn + 0,04n) (xn + 0,04n)
Al(OH)3 + OH– → AlO2– + 2H2O
0,952 – 3(xn + 0,04n) ←0,952
→ nAl(OH)3 = 4xn + 0,16n – 0,952

Đúng 0
Bình luận (0)
Hoà tan 1,952 g muối
B
a
C
l
2
.
x
H
2
O
trong nước. Thêm
H
2
S
O
4
loãng, dư vào dung dịch thu được. Kết tủa tạo thành được làm khô và cân được 1,864 g. Xác định công thức hoá học của muối.
Đọc tiếp
Hoà tan 1,952 g muối B a C l 2 . x H 2 O trong nước. Thêm H 2 S O 4 loãng, dư vào dung dịch thu được. Kết tủa tạo thành được làm khô và cân được 1,864 g. Xác định công thức hoá học của muối.
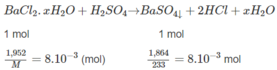
⇒ M = 244g/mol = M B a C l 2 . x H 2 O . Từ đó :
⇒ x = 2.
Đáp số : B a C l 2 . x H 2 O
Đúng 0
Bình luận (0)

















