KHỬ HOÀN TOÀN 4,06 GAM MỘT OXIT KIM LOẠI m BẰNG 3,136 LÍT CO Ở nhiệt độ cao thành kim loại khí X. tỉ khối của X so vs H2 là 18. xác định công thức của oxit kim loại

Những câu hỏi liên quan
Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng Ca(OH)2 dư, thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl dư thu được 1,176 lít khí (đkc). Xác định công thức oxit kim loại. A. CuO B. Fe2O3 C. Fe3O4 D. ZnO
Đọc tiếp
Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng Ca(OH)2 dư, thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl dư thu được 1,176 lít khí (đkc). Xác định công thức oxit kim loại.
A. CuO
B. Fe2O3
C. Fe3O4
D. ZnO
Khử hoàn toàn 4,06 gam một oxit kim loại bằng khí CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng dung dịch Ca(OH)2 (dư) tạo thành 7,00 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl (dư) thì thu được 1,176 lít khí H2 (đktc). Công thức của oxit kim loại là A. FeO. B. CrO. C. Fe2O3. D. Fe3O4
Đọc tiếp
Khử hoàn toàn 4,06 gam một oxit kim loại bằng khí CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng dung dịch Ca(OH)2 (dư) tạo thành 7,00 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl (dư) thì thu được 1,176 lít khí H2 (đktc). Công thức của oxit kim loại là
A. FeO.
B. CrO.
C. Fe2O3.
D. Fe3O4
Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
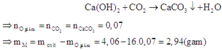
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
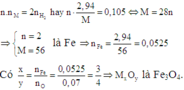
Đáp án D.
Đúng 1
Bình luận (0)
Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ sản phẩm khí sinh ra vào dung dịch Ca(OH)2 dư thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hoà tan hết vào dung dịch HCl thì thu được 1,176 lít H2 (đktc). Công thức của oxit kim loại là A. CuO. B. Al2O3. C. Fe3O4. D. ZnO.
Đọc tiếp
Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ sản phẩm khí sinh ra vào dung dịch Ca(OH)2 dư thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hoà tan hết vào dung dịch HCl thì thu được 1,176 lít H2 (đktc). Công thức của oxit kim loại là
A. CuO.
B. Al2O3.
C. Fe3O4.
D. ZnO.
Đáp án C
nCO2 = nCaCO3 = 0,07 mol
O + CO → CO2
0,07 ← 0,07
mKL = moxit – mO
= 4,06 – 0,07.16 = 2,94 (g)
Gọi hóa trị của KL khi tác dụng với HCl là n
M → 0,5n H2
0,105/n← 0,0525 (mol)
![]()
![]()
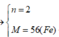
![]()
![]()
Đúng 0
Bình luận (0)
Khử hoàn toàn 4,06 gam một oxit sắt bằng khí CO dư ở nhiệt độ cao thành kim loại . Dẫn toàn bộ khí sinh ra vào bình đựng dd ca(oh)2 dư . Thấy tạo thành 7(g) kết rủa a) xác định công thức oxit sắt B) cho 4,06 g oxit sắt trên tác dụng hoàn toàn với dd H2SO4 đặc nóng
`a)`
Oxit: `Fe_xO_y`
`Fe_xO_y+yCO` $\xrightarrow{t^o}$ `xFe+yCO_2`
`CO_2+Ca(OH)_2->CaCO_3+H_2O`
Theo PT: `n_{CO_2}=n_{CaCO_3}=7/{100}=0,07(mol)`
`->n_{Fe_xO_y}={n_{CO_2}}/y={0,07}/y(mol)`
`->M_{Fe_xO_y}={4,06}/{{0,07}/y}=58y`
`->56x+16y=58y`
`->x/y={42}/{56}=3/4`
`->` Oxit: `Fe_3O_4`
`b)`
`n_{Fe_3O_4}={4,06}/{232}=0,0175(mol)`
`2Fe_3O_4+10H_2SO_4->3Fe_2(SO_4)_3+SO_2+10H_2O`
Đề thiếu.
Đúng 1
Bình luận (0)
Khử hoàn toàn một oxit của kim loại M bằng khí CO ở nhiệt độ cao, thu được 8,96 gam kim loại M và 5,376 lít khí CO2 (đktc). Oxit của kim loại là A.
F
e
3
O
4
B. CuO C. FeO D.
F
e
2
O
3
Đọc tiếp
Khử hoàn toàn một oxit của kim loại M bằng khí CO ở nhiệt độ cao, thu được 8,96 gam kim loại M và 5,376 lít khí CO2 (đktc). Oxit của kim loại là
A. F e 3 O 4
B. CuO
C. FeO
D. F e 2 O 3
Đáp án D
Ta có: n C O 2 = 0 , 24 → n O ( o x i t ) = 0 , 24 m o l
Nếu đáp án là FeO hoặc CuO thì n M = 0 , 24 → m = 37 , 333
Vậy M là Fe → m M = 0 , 16 → n M : n O = 2 : 3
Vậy oxit cần tìm là Fe2O3
Đúng 0
Bình luận (0)
Khử hoàn toàn một oxit của kim loại M bằng khí CO ở nhiệt độ cao, thu được 8,96 gam kim loại M và 5,376 lít khí CO2 (đktc). Oxit của kim loại là A.
F
e
3
O
4
B. CuO C. FeO D.
F
e
2
O
3
Đọc tiếp
Khử hoàn toàn một oxit của kim loại M bằng khí CO ở nhiệt độ cao, thu được 8,96 gam kim loại M và 5,376 lít khí CO2 (đktc). Oxit của kim loại là
A. F e 3 O 4
B. CuO
C. FeO
D. F e 2 O 3
Đáp án D
Ta có:
![]()
Nếu đáp án là FeO hoặc CuO thì
![]()
Vậy M là Fe
![]()
Vậy oxit cần tìm là Fe2O3
Đúng 0
Bình luận (0)
Khử hoàn toàn một oxit của kim loại M bằng khí CO ở nhiệt độ cao, thu được 8,96 gam kim loại M và 5,376 lít khí CO2 (đktc). Oxit của kim loại là A. FeO B. Fe2O3 C. CuO D. Fe3O4
Đọc tiếp
Khử hoàn toàn một oxit của kim loại M bằng khí CO ở nhiệt độ cao, thu được 8,96 gam kim loại M và 5,376 lít khí CO2 (đktc). Oxit của kim loại là
A. FeO
B. Fe2O3
C. CuO
D. Fe3O4
Khử hoàn toàn 2,784 gam một oxit kim loại bằng 1,344 lít CO (đktc), sau phản ứng thu được hỗn hợp khí có tỉ khối so với H2 là 20,4. Lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 806,4 ml H2(đktc). Xác định công thức của oxit kim loại đã dùng?
PTHH: AxOy + yCO --to--> xA + yCO2
Có: nCO(dư) + nCO2 = nCO(bd) = \(\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mà \(\dfrac{28.n_{CO\left(dư\right)}+44.n_{CO_2}}{n_{CO}+n_{CO_2}}=20,4.2=40,8\)
=> nCO2 = 0,048 (mol)
\(n_{A_xO_y}=\dfrac{2,784}{x.M_A+16y}\left(mol\right)\)
AxOy + yCO --to--> xA + yCO2
=> \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2,784y}{x.M_A+16y}=0,048\left(mol\right)\left(1\right)\\n_A=\dfrac{2,784x}{x.M_A+16y}\left(mol\right)\end{matrix}\right.\)
(1) => \(M_A=\dfrac{42y}{x}=>\dfrac{y}{x}=\dfrac{M_A}{42}\) (2)
PTHH: 2A + 2nHCl --> 2ACln + nH2
=> \(n_{H_2}=\dfrac{1,392xn}{x.M_A+16y}=0,036\left(mol\right)\)
=> \(1,392n=0,036.M_A+\dfrac{0,576y}{x}\) (3)
(2)(3) => MA = 28n
Xét n = 1 => L
Xét n = 2 => MA = 56 (Fe) => \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Đúng 1
Bình luận (0)
Xin cảm ơn mọi người đã đọc câu hỏi này nhưng em đã nghĩ ra đáp án cho bài tập này rồi ạ
Đúng 0
Bình luận (0)
Khử hoàn toàn 27,84g một oxit của kim loại bằng CO ở nhiệt độ cao tạo thành kim loại. Dẫn toàn bộ khí vào bình đựng Ba(OH)2 dư thu được 94,56g kết tủa. Nếu cho toàn bộ lượng kim loại vào dung dịch H2SO4l dư thu được 8,064l H2. Xác định công thức oxit
Xem chi tiết
\(n_{CO} = n_{CO_2} = n_{BaCO_3} = \dfrac{94,56}{197} = 0,48(mol)\)
Bảo toàn khối lượng :
\(m_{kim\ loại} = m_{oxit} + m_{CO} - m_{CO_2} = 27,84 + 0,48.28 -0,48.44 = 20,16(gam)\)
\(n_{H_2} = \dfrac{8,064}{22,4} = 0,36(mol)\)
2R + 2nHCl → 2RCln + nH2
\(\dfrac{0,72}{n}\).............................0,36...........(mol)
Suy ra: \(\dfrac{0,72}{n}\).R = 20,16 ⇒ R = 28n. Với n = 2 thì R = 56(Fe)
CO + Ooxit → CO2
0,48.....0,48...............(mol)
Ta có: \(\dfrac{n_{Fe}}{n_O} = \dfrac{0,36}{0,48} = \dfrac{3}{4}\). Vậy oxit sắt là Fe3O4
Đúng 0
Bình luận (0)












