Cho hợp chất hữu cơ a ở thể khí đốt cháy hoàn toàn 5,6 lít khí A ở điều kiện tiêu chuẩn thu được 22 gam CO2 và 9 gam nước. xác định công thức hóa học của phân tử là biết một lít khí A ở điều kiện tiêu chuẩn có khối lượng là 1,25 g

Những câu hỏi liên quan
Hợp chất hữu cơ A ở thể khí đốt cháy hoàn toàn 5,6 lít khí A thu được 22 gam CO2 và 9 gam H2O .tìm công thức phân tử của a biết 1 lít khí ở điều kiện tiêu chuẩn có khối lượng là 1,25 g.. lớp 9 nhé
Xem thêm câu trả lời
Đốt cháy hoàn toàn 4,8 gam một hợp chất hữu cơ A sau phản ứng thu được 6,6 gam CO2 và 5,4 gam H2O. Biết rằng khi hóa hơi ở điều kiện tiêu chuẩn 2,24 lít khí A nặng 3,2 gam. a) Xác định công thức phân tử của hợp chất hữu cơ A. b) Biết rằng A có phản ứng với Na. Tính thể tích khí hidro (đktc) thoát ra khi cho lượng chất A ở trên phản ứng hoàn toàn với Na dư. (Na = 23, O = 16, C = 16, H = 1)
a)
n CO2 = 6,6/44 = 0,15(mol) => n C = n CO2 = 0,15(mol)
n H2O = 5,4/18 = 0,3(mol) => n H = 2n H2O = 0,6(mol)
=> n O = (4,8 - 0,15.12 - 0,6)/16 = 0,15(mol)
Ta có :
n C : n H : n O = 0,15: 0,6 : 0,15 = 1 : 4 : 1
=> CTP của A là (CH4O)n
M A = (12 + 4 + 16)n = 3,2/(2,24/22,4) = 32
=> n = 1
Vậy CTPT của A là CH4O
b)
$2CH_3OH + 2Na \to 2CH_3ONa + H_2$
n CH3OH = n CO2 = 0,15(mol)
=> n H2 = 1/2 n CH3OH = 0,075(mol)
=> V H2 = 0,075.22,4 = 1,68(lít)
Đúng 2
Bình luận (0)
Đốt cháy 1,5g chất hữu cơ thu được 1,76g khí CO2; 0,9g nước và 0,448 lít khí NH3. Nếu hóa hơi 1,5g chất hữu cơ A thì thu được 0,448 lít khí. Xác định công thức phân tử của A? ( Các thể tích khí đo ở điều kiện tiêu chuẩn)
\(nCO2=nC=\dfrac{1.76}{44}=0.04mol\)
\(nH2O=\dfrac{1}{2}nH=0.05\Rightarrow nH=0.1mol\)
\(nNH3=nN=0.02mol\)
\(nO=\dfrac{mX-mC-mN-mH}{16}=\dfrac{1.5-0.04\times12-0.02\times14-0.1\times1}{16}=0.04mol\)
C:H:N:O = 2:5:1:2
=> Công thức đơn giản nhất: (C2H5NO2)n
\(MX=\dfrac{1.5}{0.02}=75\)
=> n = 1 => C2H5NO2
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 2,82 gam chất hữu cơ A cần 2,856 lít khs O2 thu được khí CO2 và hơi nước theo tỉ lệ thể tích Vco2/Vh2o = 4/3 ( các khi đo ở điều kiện tiêu chuẩn ) . Hãy xác định công thức phân tử của A . Biết tỉ khối của A với không khí nhỏ hơn 7
Ta có: \(n_{O_2}=\dfrac{2,856}{22,4}=0,1275\left(mol\right)\)
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{4}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{4}{3}\)
Gọi: nCO2 = 4x (mol) ⇒ nH2O = 3x (mol)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ 2,82 + 0,1275.32 = 4x.44 + 3x.18
⇒ x = 0,03
⇒ nCO2 = 0,03.4 = 0,12 (mol) = nC
nH2O = 0,03.3 = 0,09 (mol) ⇒ nH = 0,09.2 = 0,18 (mol)
Ta có: mC + mH = 0,12.12 + 0,18.1 = 1,62 (g) < 2,82 (g)
→ A chứa C, H và O.
⇒ mO = 2,82 - 1,62 = 1,2 (g) \(\Rightarrow n_O=\dfrac{1,2}{16}=0,075\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,12:0,18:0,075 = 8:12:5
→ CTPT của A có dạng là (C8H12O5)n (n nguyên dương)
Mà: \(M_A< 29.7=203\left(g/mol\right)\)
\(\Rightarrow\left(12.8+12.1+16.5\right)n< 203\)
⇒ n < 1,08 ⇒ n = 1
Vậy: CTPT của A là C8H12O5.
Đúng 1
Bình luận (2)
Đốt cháy hoàn toàn 1,12 lít hỗn hợp khí X gồm ankin A và hiđrocacbon B thu được 2,912 lít CO2 và 2,52 gam H2O. Xác định công thức phân tử, viết công thức cấu tạo và gọi tên A, B. Biết rằng các thể tích khí đo ở điều kiện tiêu chuẩn
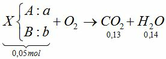
Đốt cháy ankin => nCO2 > nH2O mà theo bài ra nCO2 < nH2O
=> B là ankan nCO2 < nH2O
Nhận xét:
Đốt ankin: – nankin = nH2O – nCO2
Đốt ankan: nankan = nH2O – nCO2
=> b – a = 0,01 và b + a = 0,05
=> a = 0,02 và b = 0,03
=> số C trung bình = 2,6 và số H trung bình = 5,6
TH1: số C trong ankin < 2,6 => A là C2H2: 0,02 và B: 0,03
=> B: 44 (C3H8)
TH2: số C trong ankan < 2,6 => A : 0,02 và CH4: 0,03
=> A: 68 (C5H8) loại do hh khí
TH3: số C trong ankan < 2,6 => A: 0,02 và C2H6: 0,03
=> A: 47 (lẻ) => loại
Vậy A là C2H2 (axetilen/ etin) và B là C3H8 (propan)
Đúng 0
Bình luận (0)
Đốt cháy 6,6 gam hợp chất chất hữu cơ A thu được 10,8 gam nước 11,1555 lít khí CO2 ở điều kiện chuẩn. Hãy xác định công thức phân tử của A, biết khối lượng mol của A là 44gam/ mol
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\Rightarrow n_H=0,6.2=1,2\left(mol\right)\)
\(n_{CO_2}=\dfrac{11,1555}{24,79}=0,45\left(mol\right)=n_C\)
⇒ mC + mH = 0,45.12 + 1,2.1 = 6,6 (g) = mA
→ A chỉ gồm C và H.
Gọi: CTPT của A là CxHy.
⇒ x:y = 0,45:1,2 = 3:8
→ A có CTPT dạng (C3H8)n
\(\Rightarrow n=\dfrac{44}{12.3+1.8}=1\)
Vậy: CTPT của A là C3H8.
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 1,3 g một hợp chất hữu cơ A cho khí Oxi thì thu được 1,4 l CO2 ở điều kiện tiêu chuẩn và 1,35 gam nước biết hợp chất A có công thức phân tử trùng với công thức đơn giản nhất
\(n_{CO_2}=\dfrac{1,4}{22,4}=0,0625\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,35}{18}=0,075\left(mol\right)\)
Bảo toàn C: nC = 0,0625
Bảo toàn H: nH = 0,15
=> \(n_O=\dfrac{1,3-0,0625.12-0,15}{16}=0,025\left(mol\right)\)
Xét nC : nH : nO = 0,0625 : 0,15 : 0,025 = 5 : 12 : 2
=> CTPT: C5H12O2
Đúng 1
Bình luận (0)
Hai chất hữu cơ A và B có cùng công thức phân tử. Khi đốt cháy 2,9 gam A thu được 8,8 gam khí
CO
2
và 4,5 gam
H
2
O
. Ở điều kiện tiêu chuẩn 2,24 lít khí B có khối lượng 5,8 gam. Hãy xác định công thức phân tử của A, B và viết công thức cấu tạo của mỗi chất.
Đọc tiếp
Hai chất hữu cơ A và B có cùng công thức phân tử. Khi đốt cháy 2,9 gam A thu được 8,8 gam khí CO 2 và 4,5 gam H 2 O . Ở điều kiện tiêu chuẩn 2,24 lít khí B có khối lượng 5,8 gam. Hãy xác định công thức phân tử của A, B và viết công thức cấu tạo của mỗi chất.
Ta có M B = 5,8/22,4 x 22,4 = 58(gam/mol)
- Vì A, B có cùng công thức phân tử nên: M B = M A = 58(gam/mol)
- Trong 8,8 gam CO 2 có 8,8/44 x 12 = 2,4g cacbon
Trong 4,5 gam H 2 O có 4,5/18 x 2 = 0,5g hidro
Ta có m C + m H = 2,4 + 0,5 = 2,9g
m A = m C + m H . Vậy A và B là hai hidrocacbon có M A = 58 (gam/mol)
Vậy công thức phân tử của A,B là C 4 H 10 (xem cách giải bài số 34.5)
Công thức cấu tạo của hai chất A và B là
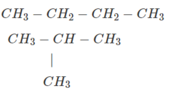
Đúng 0
Bình luận (0)
Đốt cháy 5,6 lít chất hữu cơ ở thể khí thu được 16,8 lít CO2 và 13,5 g hơi nước. 1 lít chất hữu cơ đó có khối lượng 1,875 g. Biết các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng (gam) của oxi có trong 5,6 lít X là.



















