Khử 4,64 (g) hh A gồm FeO Fe,O3, Fe;04 có số mol bằng nhau bằng CO dư thu được chất rắn B. a. khối lượng chất rắn B =2: b.Hòa tan hoàn toàn B trong dd HNO; thu được 2 khí là NO và NO2 có ti lệ số mol 1:1. Tổng thể tích của 2 khí này là bao nhiờu?

Những câu hỏi liên quan
Để tác dụng hoàn toàn với 4,64 g hỗn hợp FeO, Fe2O3, Fe3O4 cần dùng vừa đủ 160 ml dung dịch HCl 1M. Nếu khử hoàn toàn 4,64 g hỗn hợp trên bằng CO ở nhiệt độ cao thì khối lượng Fe thu được là
A. 3,36 g.
B. 4,36 g.
C. 3,63 g.
D. 4,63 g.
Chọn A
Ta có n O o x i t = 1 2 n a x i t = 1 2 . 0 , 16 . 1 = 0 , 08
m F e = m h h – m o ( o x i t ) = 4,64 – 0,08.16 = 3,36 gam.
Đúng 0
Bình luận (0)
Để khử hoàn toàn 3,04 g hh X gồm FeO, Fe3O4, Fe2O3 cần 0,05 mol H2.. Mặt khác hào tan hoàn toàn 3,04 g hh x trong dd H2SO4 đặc dư thu được thể tích SO2 (sp khử !) ở đktc là?
hỗn hợp X( quy đổi) ----> Fe( x mol) ,O( y mol)
Cho X+ H2:
Bảo toàn khối lượng: m(hh X)= m(Fe)+m(O)= 56x+16y=3,04
Bảo toàn H: n(H2O)=n(H2)=0,05 Bảo toàn O: n(O)=n(H2O)=0,05=y suy ra x=0,04
Cho X+H2SO4: ----> SO2 a mol
Fe--->Fe(3+) +3e 2O+ 4e---> 2O(2-)
0,04 3.0,04 0.05 2.0,05
S(+6)+ 2e----> S(+4)
2a a
Bảo toàn e: 3.0,04= 2.0,05+2a suy ra a=0.01 suy ra V=0,224 l
Đúng 0
Bình luận (0)
Dùng 3,136 lít khí hidro để khử hoàn toàn 8,48 g hỗn hợpA gồm CuO, FeO,Fe2O3,Fe3O4 ở nhiệt độ cao. Sau khi phản ứng kết thúc thu được hh kim loại B.
a) Tính khối lượng hh kim loại B thu được.
b)Xác định thành phần phần trăm theo khối lượng của mỗi oxit trong hh A.Biết rằng trong hh A số mol FeO2nCuO , 2nFe2O3nFe3O4
Đọc tiếp
Dùng 3,136 lít khí hidro để khử hoàn toàn 8,48 g hỗn hợpA gồm CuO, FeO,Fe2O3,Fe3O4 ở nhiệt độ cao. Sau khi phản ứng kết thúc thu được hh kim loại B.
a) Tính khối lượng hh kim loại B thu được.
b)Xác định thành phần phần trăm theo khối lượng của mỗi oxit trong hh A.Biết rằng trong hh A số mol FeO=2nCuO , 2nFe2O3=nFe3O4
Nung m gam bột Fe trong
O
2
thu được 11,36 gam hỗn hợp X gồm: Fe, FeO,
Fe
2
O
3
,
Fe
3
O
4
. Cho toàn bộ X phản ứng hết với dung dịch HN
O
3
loãng dư, thu được 1,344...
Đọc tiếp
Nung m gam bột Fe trong O 2 thu được 11,36 gam hỗn hợp X gồm: Fe, FeO, Fe 2 O 3 , Fe 3 O 4 . Cho toàn bộ X phản ứng hết với dung dịch HN O 3 loãng dư, thu được 1,344 lít khí NO (sản phẩm khử duy nhất,ở đktc).
Tìm m.
- Từ quá trình phản ứng ta thấy số oxi hoá của các chất phản ứng ở trạng thái đầu là
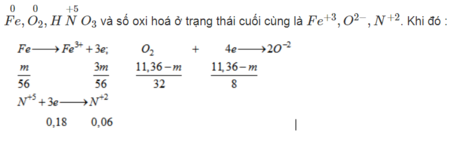
Áp dụng ĐLBT electron ta có:
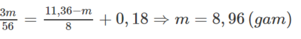
Đúng 0
Bình luận (0)
Khử hoàn toàn 46,4 gam hh gồm FeO, Fe3O4 , Fe2O3 = khí H2 ở nhiệt dộ cao thì thu đc m gam Fe và 14,4 gam nước
a, vt PTHH
b, tính m
Sơ dồ PƯ : FeO+H2-> Fe+H2O ,Fe3O4 +H2-> Fe+H2O, Fe2O3 +H2 ->Fe +H2O
PTHH: \(FeO+H_2\rightarrow Fe+H_2O\)
PTHH: \(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
PTHH: \(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
Theo PT ta có: \(n_{H2}=n_{H2O}=\dfrac{14,4}{18}=0,8\left(mol\right)\)
\(\Rightarrow m_{H2}=2.0,8=1,6\left(g\right)\)
ADĐLBTKL, ta có: \(m_{hh}+m_{H2}=m_{Fe}+m_{H2O}\)
\(\Rightarrow m_{Fe}=m_{hh}+m_{H2}-m_{H2O}=46,4+1,6-14,4=33,6\left(g\right)\)
Vậy.........
Đúng 0
Bình luận (0)
Để 10,08 gam Fe ngoài ko khí sau 1 thời gian thu đc 12g hh A gồm FeO, Fe2O3, Fe3O4, và Fe dư. Hòa tan A = dd HNO3 dư, Sau pư thu đc V lít NO (đktc) sp khử duy nhất.Tính V
*Sơ đồ
\(Fe+O2->\left\{{}\begin{matrix}FeO\\Fe2O3\\Fe3O4\\Fe\end{matrix}\right.+HNO3->Fe^{3+}+NO+H2O\)
_Theo bài:
nFe =10,08/56 = 0,18 mol
_Theo BTKL có:
mO2 = mA - mFe = 12 - 10,08 = 1,92g
=>nO2 = 1,92/32 = 0,06
_Quá trình cho và nhận e:
Feo - 3e -> Fe+3
0,18...0,54
_______________________
N+5 + 3e ->N+2
.................3x.......x
O2o + 4e -> 2O-2
0,06.........0,24
_Theo bảo toàn e:
ne cho = ne nhận
=>0,54 = 3x + 0,24
=>x = 0,3/3 = 0,1
=>nNO = x = 0,1 mol
=> V = 0,1 . 22,4 = 2,24 lít
Đúng 1
Bình luận (0)
Cho 16,8 g Fe td với oxi thì thu đc 21,6 g hh A gồm Fe, FeO, Fe2O3, Fe3O4. A td với dd HNO3 thì thu đc V lít khí NO2. Tính V
Khử m gam Fe3O4 bằng H2 thu được hh X gồm Fe và FeO, hh X tác dụng hết với 3 lít dung dịch H2SO4 0,2M (loãng). Giá trị của m là ?
Fe3O4+H2-to>Fe+2Feo+2H2o
FeO+H2SO4-<>FeSO4+H2O
Fe+H2SO4->FeSO4+H2
nH2SO4=0,4 mol
=>n hh X=0,4 mol
mà nX=n Fe3O4=0,4 mol
=>mFe3O4=0,4.232=92,8g
Đúng 0
Bình luận (0)
Khử hoàn toàn 6 g X gồm Fe, FeO, Fe2O3, Fe3O4 bằng H2 dư thu được 5,04 g Fe. Tính thể tích SO2 ở đktc thoát ra khi hòa tan X trong H2SO4 đặc, nóng, dư.















