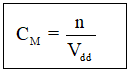nồng độ mol của 29,25g nacl trong 500ml

Những câu hỏi liên quan
Trộn lẫn 117ml dung dịch có chứa 2,84 gam Na2SO4 và 212ml dung dịch có chứa 29,25g NaCl và 171ml H2O. Nồng độ mol của ion Na+ trong dung dịch thu được là: A. 1,4M B. 1,6M C. 1,08M D. 2,0M
Đọc tiếp
Trộn lẫn 117ml dung dịch có chứa 2,84 gam Na2SO4 và 212ml dung dịch có chứa 29,25g NaCl và 171ml H2O. Nồng độ mol của ion Na+ trong dung dịch thu được là:
A. 1,4M
B. 1,6M
C. 1,08M
D. 2,0M
Đáp án C
n N a 2 S O 4 = 0,02 mol; nNaCl=0,5 mol; nNa+= 0,02.2+0,5= 0,54 mol
[Na+]= 0,54/(0,117+0,171+0,212)= 1,08M
Đúng 0
Bình luận (0)
Trong 500ml dung dịch có hòa tan 11,7g NaCl. Tính nồng độ mol của dung dịch NaCl
thêm 300ml h2o vào 200ml dung dịch nacl 1,5M để thu đượ 500ml dung dịch A. Tính số mol chất tan. Tính nồng độ mol của dung dịch A
nNaCl=0,2*1,5=0,3mol
Sau khi thêm nước thì nNaCl không đổi
Vdd mới= 0,2+0,3=0,5(l)
suy ra Cm NaCl=0,3/0,5=0,6M
Đúng 0
Bình luận (0)
Hãy tính nồng độ mol của 1 mol KC1 trong 500ml dung dịch
\(CM_{KCl}=\dfrac{n}{V}=\dfrac{1}{0,5}=2M\)
Đúng 1
Bình luận (0)
Hãy tính:
a. Nồng độ mol của 4000ml dung dịch có chứa 400g CuSO_4
b. Số mol và số gam chất tan trong 50g dd MgCl_2 4%
c. Nồng độ % của 600g dd có chứa 20g KCL
d. Nồng độ % của dd có 20g NaCl hòa tan trong 180g nước
e. Số mol và số gam chất tan trong 500ml dd KNO_3 2M
i. Tính nồng độ % của dd biết độ tan của muối ăn ở 200 là 36g
Đọc tiếp
Hãy tính:
a. Nồng độ mol của 4000ml dung dịch có chứa 400g \(CuSO_4\)
b. Số mol và số gam chất tan trong 50g dd \(MgCl_2\) 4%
c. Nồng độ % của 600g dd có chứa 20g KCL
d. Nồng độ % của dd có 20g NaCl hòa tan trong 180g nước
e. Số mol và số gam chất tan trong 500ml dd \(KNO_3\) 2M
i. Tính nồng độ % của dd biết độ tan của muối ăn ở 200 là 36g
Tính nồng độ mol của các chất tan có trong đ trong các trường hợp sau đây:
a) 500ml dd chứ 5,85g NaCl
b) 300g đ chứ 0,5 mol đồng nitrat
c) Trọn 50ml đ HCl 2M vs 100ml đ NaOH 0,5M
d) Trộn 100g đ chứa 0,2ml CuSO4 vs 200g dd chứa 0,1 mol NaOH
Tính nồng độ mol của các chất tan có trong đ trong các trường hợp sau đây:
a) 500ml dd chứ 5,85g NaCl
b) 300g đ chứ 0,5 mol đồng nitrat
c) Trọn 50ml đ HCl 2M vs 100ml đ NaOH 0,5M
d) Trộn 100g đ chứa 0,2ml CuSO4 vs 200g dd chứa 0,1 mol NaOH
Cho 0,6 mol CuSO4 trong 500ml dung dịch CuSO4 . Tính nồng độ mol của dd CuSO4
Đổi 500ml = 0,5l
\(C_{M\left(C\text{uS}O_4\right)}=\dfrac{n}{V_{\text{dd}}}=\dfrac{0,6}{0,5}=1,2M\)
Đúng 0
Bình luận (0)
Tính nồng độ % và nồng độ mol của 400g dung dich NaCl trong đó có chứa 60g NaCl (biết D=1,1g/ml)
\(C\%_{NaCl}=\dfrac{60}{400}\cdot100\%=15\%\)
Ta có: \(\left\{{}\begin{matrix}n_{NaCl}=\dfrac{60}{58,5}=\dfrac{40}{39}\left(mol\right)\\V_{NaCl}=\dfrac{400}{1,1}=\dfrac{4000}{11}\left(ml\right)=\dfrac{4}{11}\left(l\right)\end{matrix}\right.\) \(\Rightarrow C_{M_{NaCl}}=\dfrac{\dfrac{40}{39}}{\dfrac{4}{11}}\approx2,82\left(M\right)\)
Đúng 3
Bình luận (0)
Ta có: \(C\%_{NaCl}=\dfrac{60}{400}.100\%=15\%\)
\(V_{ddNaCl}=\dfrac{400}{1,1}=\dfrac{4000}{11}\left(ml\right)=\dfrac{4}{11}\left(l\right)\)
\(n_{NaCl}=\dfrac{60}{58,5}=\dfrac{40}{39}\left(mol\right)\)
\(\Rightarrow C_{M_{NaCl}}=\dfrac{\dfrac{40}{39}}{\dfrac{4}{11}}\approx2,82M\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (1)