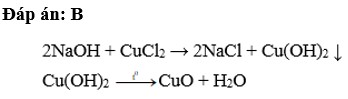Khi cho dung dịch NaOH vào dung dịch CuSO4 đến khi kết tủa không tăng thêm nữa, cho biết tên gọi và màu sắc của kết tủa thu được.

Những câu hỏi liên quan
Câu 15 : Cho 500 ml dung dịch CuSO4 0,4M thêm dung dịch NaOH vừa đủ vào thì thu được kết tủa màu xanh lam và nước lọc. Lọc kết tủa đem nung đến khối lượng không đổi thì thu được chất rắn A.
a. Viết phương trình.
b. Tính khối lượng nước lọc.
c. Tính khối lượng chất rắn A.
\(a.CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\\ Cu\left(OH\right)_2-^{t^o}\rightarrow CuO+H_2O\\b. n_{CuSO_4}=n_{Na_2SO_4}=0,2\left(mol\right)\\ m_{Na_2SO_4}=0,2.142=28,4\left(g\right)\\ c.BTNT\left(Cu\right):n_{CuO}=n_{CuSO_4}=0,2\left(mol\right)\\ \Rightarrow m_{CuO}=0,2.80=16\left(g\right)\)
Đúng 2
Bình luận (0)
Nhỏ từ từ dung dịch NaOH vào dung dịch FeCl3 đến khi kết tủa không tạo thêm nữa thì dừng lại. Lọc kết tủa rồi đem nung đến khối lượng không đổi. Thu được chất rắn là:
A.Fe(OH)3
B.Fe2O3
C.Fe
D.FeO
\(B\\ 3NaOH+FeCl_3\rightarrow Fe\left(OH\right)_3+3NaCl\\ 2Fe\left(OH\right)_3\underrightarrow{^{to}}Fe_2O_3+3H_2O\)
Đúng 0
Bình luận (0)
Cho 1,02 gam hỗn hợp A gồm Fe và Mg vào 200 ml dung dịch CuSO4. Sau khi các phản ứng hoàn toàn, lọc, thu được 1,38 gam chất rắn B và dung dịch C. Thêm dung dịch NaOH dư vào C, lấy kết tủa đem nung ngoài không khí đến khối lượng không đổi thu được 0,9 gam chất rắn D. Nồng độ mol/lít của dung dịch CuSO4 là: A. 0,075M B. 0,375M C. 0,15M D. 0,125M
Đọc tiếp
Cho 1,02 gam hỗn hợp A gồm Fe và Mg vào 200 ml dung dịch CuSO4. Sau khi các phản ứng hoàn toàn, lọc, thu được 1,38 gam chất rắn B và dung dịch C. Thêm dung dịch NaOH dư vào C, lấy kết tủa đem nung ngoài không khí đến khối lượng không đổi thu được 0,9 gam chất rắn D. Nồng độ mol/lít của dung dịch CuSO4 là:
A. 0,075M
B. 0,375M
C. 0,15M
D. 0,125M
Đáp án : A
Ta thấy chất rắn D gồm toàn oxit của Mg (và có thể của Fe) có m < mA
=> chứng tỏ A không phản ứng hết mà có kim loại dư.
Giả sử Fe chỉ phản ứng 1 phần với số mol là x; nMg = y
=> CuSO4 hết
=> moxit = mMgO + m F e 2 O 3 = 40y + 80x = 0,9g
Lại có : mB – mA = mCu – mMg – mFe pứ
=> 1,38 – 1,02 = 64.(x + y) – 24y – 56x
=> x = y = 0,0075 mol
=> n C u S O 4 = x + y = 0,015 mol
=> C M C u S O 4 = 0,075M
Đúng 0
Bình luận (0)
Cho hỗn hợp K2CO3 và NaHCO3 (tỉ lệ mol 1: 1) vào bình đựng dung dịch Ba(HCO3)2 thu được kết tủa X và dung dịch Y. Thêm từ từ dung dịch HCl 0,5M vào bình đến khi không còn khí thoát ra nữa thì hết 560 ml. Biết toàn bộ Y phản ứng với vừa đủ 200 ml dung dịch NaOH 1M. Khối lượng kết tủa X là: A. 3,94 B. 9,85 C. 7,88 D. 11,28
Đọc tiếp
Cho hỗn hợp K2CO3 và NaHCO3 (tỉ lệ mol 1: 1) vào bình đựng dung dịch Ba(HCO3)2 thu được kết tủa X và dung dịch Y. Thêm từ từ dung dịch HCl 0,5M vào bình đến khi không còn khí thoát ra nữa thì hết 560 ml. Biết toàn bộ Y phản ứng với vừa đủ 200 ml dung dịch NaOH 1M. Khối lượng kết tủa X là:
A. 3,94
B. 9,85
C. 7,88
D. 11,28
Đáp án C
Hỗn hợp K2CO3 và NaHCO3 (tỉ lệ mol 1:1) + Ba(HCO3)2 → ↓X + dd Y
Thêm 0,28 mol HCl vào bình
Y + 0,2 mol NaOH
Đặt nK2CO3 = nNaHCO3 = x mol và nBa(HCO3)2 = y mol
Dd Y + 0,2 mol NaOH → nHCO3- = 0,2 mol => x + 2y = 0,2 (1)
Bình + 0,28 mol HCl → nCO32- + 2nHCO3- = nH+ => 2x + (x+2y) = 0,28 (2)
Giải (1) (2) thu được x = 0,04 và y = 0,08 mol
=> mBaCO3 = 0,04.197 = 7,88 gam
Đúng 0
Bình luận (0)
Nhỏ từ từ dung dịch NaOH vào dung dịch
C
u
C
l
2
đển khi kết tủa không tạo thêm nữa thì dừng lại. Lọc kết tủa rồi đem nung đến khối lượng không đổi. Thu được chất rắn nào sau đây: A.
C
u
B.
C
u
O
C.
C
u
2
O
D.
C
u
(
O
H...
Đọc tiếp
Nhỏ từ từ dung dịch NaOH vào dung dịch C u C l 2 đển khi kết tủa không tạo thêm nữa thì dừng lại. Lọc kết tủa rồi đem nung đến khối lượng không đổi. Thu được chất rắn nào sau đây:
A. C u
B. C u O
C. C u 2 O
D. C u ( O H ) 2
Nhỏ dung dịch NaOH loãng vào bình đựng dung dịch chất X, thu được kết tủa xanh nhạt, khi thêm dung dịch NaOH vào bình, thấy kết tủa tan dần tạo thành kết tủa màu lục nhạt. X là :
A. CrCl3
B. AlCl3
C. CuCl2
D. ZnCl2
Chọn đáp án A
3NaOH + CrCl3 → t 3NaCl + Cr(OH)3 ¯(xanh nhạt)
Cr(OH)3 + NaOH → t NaCrO2 (lục nhạt) + 2H2
Đúng 0
Bình luận (0)
Nhỏ dung dịch NaOH loãng vào bình đựng dung dịch chất X, thu được kết tủa màu xanh nhạt, khi thêm tiếp dung dịch NaOH vào bình, thấy kết tủa tan dần tạo thành dung dịch màu lục nhạt. X là
A. CrCl 3
B. KOH
C. NaOH
D. NaCl
Nhỏ dung dịch NaOH loãng vào bình đựng dung dịch chất X, thu được kết tủa màu xanh nhạt. Khi thêm tiếp dung dịch NaOH vào bình, thấy kết tủa tan dần tạo thành dung dịch màu lục nhạt. X là A. CrCl3 B. AlCl3 C. CuCl2 D. ZnCl2
Đọc tiếp
Nhỏ dung dịch NaOH loãng vào bình đựng dung dịch chất X, thu được kết tủa màu xanh nhạt. Khi thêm tiếp dung dịch NaOH vào bình, thấy kết tủa tan dần tạo thành dung dịch màu lục nhạt. X là
A. CrCl3
B. AlCl3
C. CuCl2
D. ZnCl2
Nhỏ dung dịch NaOH loãng vào bình đựng dung dịch chất X, thu được kết tủa màu xanh nhạt. Khi thêm tiếp dung dịch NaOH vào bình, thấy kết tủa tan dần tạo thành dung dịch màu lục nhạt. X là A. CrCl3 B. AlCl3 C. CuCl2 D. ZnCl2
Đọc tiếp
Nhỏ dung dịch NaOH loãng vào bình đựng dung dịch chất X, thu được kết tủa màu xanh nhạt. Khi thêm tiếp dung dịch NaOH vào bình, thấy kết tủa tan dần tạo thành dung dịch màu lục nhạt. X là
A. CrCl3
B. AlCl3
C. CuCl2
D. ZnCl2