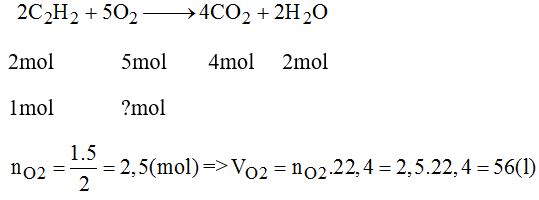Đốt cháy hoàn toàn 1,00 gam khí C2H2 thu được CO2(k) và H2O(l) giải phóng 50,01 kJ. Tính biến thiên enthalpy của phản ứng đốt cháy 1 mol khí C2H2, từ đó cho biết vì sao C2H2 được sử dụng trong đèn xì hàn cắt kim loại mà không dùng mêtan.

Những câu hỏi liên quan
Đốt cháy hoàn toàn 1 gam C2H2(g) ở điều kiện chuẩn, thu được CO2(g) và H2O(l), giải phóng 49,98 kJ. Tính biến thiên enthalpy chuẩn của phản ứng đốt cháy 1 mol C2H2.
nC2H2 = 1/26 (mol)
Đốt cháy 1/26 mol C2H2 tỏa ra 49,98 kJ
=> Đốt cháy 1 mol C2H2 tỏa ra x kJ
=> x = 1 x 49,98 : (1/26) = 1299,48 kJ
=> ${\Delta _r}H_{298}^0$ = -1299,48 kJ (vì đây là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm)
Đúng 0
Bình luận (0)
khí acetylen C2H2 cháy trong không khí theo phản ứng sauC2H2 + 02 -- CO2 + H2O a. tính thể tích khí oxi cần dùng để đốt cháy hoàn toàn 4(l) khí acetylen. Các thể tích khí đó cùng nhiệt độ và áp suấtb. cho 3,9g khí C2H2 tác dụng với 8,96(l) khí oxi ở dktc. Tính thể tích kí thu được và tỉ khối hơi của khí thu được so với khí hidro
Đọc tiếp
khí acetylen C2H2 cháy trong không khí theo phản ứng sau
C2H2 + 02 --> CO2 + H2O
a. tính thể tích khí oxi cần dùng để đốt cháy hoàn toàn 4(l) khí acetylen. Các thể tích khí đó cùng nhiệt độ và áp suất
b. cho 3,9g khí C2H2 tác dụng với 8,96(l) khí oxi ở dktc. Tính thể tích kí thu được và tỉ khối hơi của khí thu được so với khí hidro
a) PTHH: 2C2H2 + 5O2 --to--> 4CO2 + 2H2O
=> \(V_{O_2}=\dfrac{5}{2}V_{C_2H_2}=\dfrac{5}{2}.4=10\left(l\right)\)
b) \(\left\{{}\begin{matrix}n_{C_2H_2}=\dfrac{3,9}{26}=0,15\left(mol\right)\\n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\end{matrix}\right.\)
LTL: \(\dfrac{0,15}{2}< \dfrac{0,4}{5}\) => O2 dư
=> \(\left\{{}\begin{matrix}n_{CO_2}=0,15.2=0,3\left(mol\right)\\n_{O_2\left(pư\right)}=\dfrac{5}{2}.0,15=0,375\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow M_{hh}=\dfrac{0,3.44+\left(0,4-0,375\right).32}{0,3+0,4-0,375}=\dfrac{560}{13}\left(\dfrac{g}{mol}\right)\)
=> dhh/H2 = \(\dfrac{\dfrac{560}{13}}{2}=\dfrac{280}{13}\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp X gồm CH4, C2H2, C3H6 thu được CO2 (đktc) và 2,52 gam H2O. Thể tích khí O2 đã tham gia phản ứng cháy (ở đktc) là A. 3,808 lít. B. 5,376 lít. C. 4,480 lít. D. 7,840 lít
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp X gồm CH4, C2H2, C3H6 thu được CO2 (đktc) và 2,52 gam H2O. Thể tích khí O2 đã tham gia phản ứng cháy (ở đktc) là
A. 3,808 lít.
B. 5,376 lít.
C. 4,480 lít.
D. 7,840 lít
Đáp án A
nCO2= 0,1 ; nH2O = 0,14
BTNT O => nO2 = ( 0,1.2 + 0,14) : 2 = 0,17 (mol) => VO2 = 0,17.22,4 = 3,808 lít
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp X gồm CH4, C2H2, C3H6 thu được 2,24 lít CO2 (ở đktc) và 2,52 gam H2O. Thể tích khí O2 đã tham gia phản ứng cháy (ở đktc) là A. 3,808 lít. B. 5,376 lít. C. 4,480 lít. D. 7,840 lít.
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp X gồm CH4, C2H2, C3H6 thu được 2,24 lít CO2 (ở đktc) và
2,52 gam H2O. Thể tích khí O2 đã tham gia phản ứng cháy (ở đktc) là
A. 3,808 lít.
B. 5,376 lít.
C. 4,480 lít.
D. 7,840 lít.
Đốt cháy hoàn toàn hỗn hợp X gồm CH4, C2H2, C3H6 thu được 2,24 lít CO2 (ở đktc) và 2,52 gam H2O. Thể tích khí O2 đã tham gia phản ứng cháy (ở đktc) là A. 3,808 lít B. 5,376 lít C. 4,480 lít D. 7,840 lít
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp X gồm CH4, C2H2, C3H6 thu được 2,24 lít CO2 (ở đktc) và 2,52 gam H2O. Thể tích khí O2 đã tham gia phản ứng cháy (ở đktc) là
A. 3,808 lít
B. 5,376 lít
C. 4,480 lít
D. 7,840 lít
Một hỗn hợp X gồm C2H4, C3H6, CH4 và C2H2 trong đó số mol CH4 bằng 2 lần số mol C2H2. Đốt cháy hoàn toàn 0,1 mol hỗn hợp X thu được 9,02 gam CO2 và 3,87 gam H2O. Cho 0,1 mol hỗn hợp X phản ứng tối đa với a gam Br2 trong dung dịch. Giá trị của a là A. 14,4. B. 16,0. C. 17,6. D. 12,8.
Đọc tiếp
Một hỗn hợp X gồm C2H4, C3H6, CH4 và C2H2 trong đó số mol CH4 bằng 2 lần số mol C2H2. Đốt cháy hoàn toàn 0,1 mol hỗn hợp X thu được 9,02 gam CO2 và 3,87 gam H2O. Cho 0,1 mol hỗn hợp X phản ứng tối đa với a gam Br2 trong dung dịch. Giá trị của a là
A. 14,4.
B. 16,0.
C. 17,6.
D. 12,8.
Người ta dùng đèn xì oxi - axetilen để hàn cắt kim loại. Phản ứng cháy của axentilen C2H2 trong oxi tại thành khí cacbonic và hơi nước. Hãy tính thể tích oxi (đktc) cần thiết để đốt cháy hoàn toàn 44,8 lít C2H2 (đktc)
\(n_{C_2H_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\)
PT: \(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{5}{2}n_{C_2H_2}=5\left(mol\right)\)
\(\Rightarrow V_{O_2}=5.22,4=112\left(l\right)\)
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn m gam hỗn hợp gồm C2H2, CH4,C2H6, C4H10. sau phản ứng thu được 8,96 lít khí CO2 và 10,8 gam H2O.
a. tính m?
b. tính v không khí cần dùng để đốt cháy hết hỗn hợp trên? Biết Oxi chiếm 20% thể tích không khí
help me !!!!![]()
a, Ta có: \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\Rightarrow n_H=0,6.2=1,2\left(mol\right)\)
m = mC + mH = 0,4.12 + 1,2.1 = 6 (g)
b, Theo ĐLBT KL, có: m + mO2 = mCO2 + mH2O
⇒ mO2 = 22,4 (g) \(\Rightarrow n_{O_2}=\dfrac{22,4}{32}=0,7\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,7.22,4=15,68\left(g\right)\)
\(\Rightarrow V_{kk}=\dfrac{15,68}{20\%}=78,4\left(g\right)\)
Đúng 1
Bình luận (0)
Hỗn hợp khí X hồm C2H4, C2H2, C3H8, C4H10 và H2. Dẫn 6,32 gam X qua bình đựng dung dịch brom thì có 0,12 mol Br2 phản ứng. Đốt cháy hoàn toàn 2,24 lít X thu được 4,928 lít CO2 và m gam H2O. Tìm m? A. 5,04g B. 4,68g C. 5,21g D. 4,50g
Đọc tiếp
Hỗn hợp khí X hồm C2H4, C2H2, C3H8, C4H10 và H2. Dẫn 6,32 gam X qua bình đựng dung dịch brom thì có 0,12 mol Br2 phản ứng. Đốt cháy hoàn toàn 2,24 lít X thu được 4,928 lít CO2 và m gam H2O. Tìm m?
A. 5,04g
B. 4,68g
C. 5,21g
D. 4,50g