Viết pthh -cho từ từ đến dư dung dịch h2so4 đặc vào dung dịch pb(no3)2 - cho từ từ 1-2ml h2so4 đặc vào cốc chứa một ít đường saccarozo

Những câu hỏi liên quan
Nêu hiện tượng và viết PTHH:
a) Cho từ từ dung dịch H2SO4(đặc) vào cốc chứa một ít đường saccarozơ (C12H22O11)
b) Cho một ít dung dịch H2SO4(loãng) vào cốc chứa Fe(OH)3
c) Cho một ít bột CuO vào cốc chứa dung dịch HCl
d) Cho một ít bột Cu vào cốc chứa dung dịch H2SO4(đặc)
a) Lúc đầu: C12H22O11 + H2SO4 → 12C(đen) + H2SO4.11H2O
Sau đó: C12H22O11 + 24H2SO4 → 12CO2↑ + 24SO2↑ + 35H2O
Khi nhỏ axit H2SO4 đặc vào saccarozo, ta thấy đường nhanh chóng hóa đen, sau đó khối rắn tăng thể tích rất nhanh và thoát khí mùi hắc (SO2). Quan sát phương trình ta thấy chỉ 1 mol đường nhưng tạo ra những (12 + 24 = 35) mol khí, vì vậy thể tích khối rắn tăng lên nhanh.
b) 3H2SO4 + 2Fe(OH)3 ⟶ Fe2(SO4)3 + 6H2O
Hiện tượng : Chất rắn màu nâu đỏ Sắt III hidroxit (Fe(OH)3) tan dần trong dung dịch H2SO4, tạo ra dung dịch màu vàng nâu
c) CuO + 2HCl ⟶ 2H2O + CuCl2
Hiện tượng : Chất rắn màu đen đồng II oxit (CuO) tan dần trong dd, tạo thành dd màu xanh lam là CuCl2.
d)Cu + 2H2SO4 ⟶ 2H2O + SO2 + CuSO4
Hiện tượng: Chất rắn màu đỏ Đồng (Cu) tan dần trong dung dịch và sủi bọt khí do khí mùi hắc Lưu huỳnh dioxit (SO2) sinh ra.
Đúng 0
Bình luận (0)
Cho H2SO4 đặc vào cốc chứa một ít đường saccarozo, thu hỗn hợp khí sau phản ứng rồi sục vào dung dịch Ca(OH)2 dư. Nêu hiện tượng xảy ra trong các thí nghiệm và viết phương trình hóa học của các phản ứng xảy ra
Lúc đầu: C12H22O11 + H2SO4 → 12C(đen) + H2SO4.11H2O
Sau đó: C12H22O11 + 24H2SO4 → 12CO2↑ + 24SO2↑ + 35H2O
Khi nhỏ axit H2SO4 đặc vào saccarozo, ta thấy đường nhanh chóng hóa đen, sau đó khối rắn tăng thể tích rất nhanh và thoát khí mùi hắc (SO2). Quan sát phương trình ta thấy chỉ 1 mol đường nhưng tạo ra những (12 + 24 = 35) mol khí, vì vậy thể tích khối rắn tăng lên nhanh.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
SO2 + Ca(OH)2 → CaSO3↓ + H2O
Khí (CO2 + SO2) sục vào dung dịch Ca(OH)2 dư ta thấy xuất hiện kết tủa trắng, kết tủa tăng dần đến tối đa và không thay đổi.
Đúng 1
Bình luận (0)
Câu 8: nêu hiện tượng và viết pthh khi cho:
a) Từ từ đến dư CO2 vào dung dịch nước vôi trong
b) Bột đồng vào dung dịch H2SO4 đặc
b1:Nêu hiện tượng quan sát được và viết phương trình hóa học xảy ra ghi rõ điều kiện phản ứng (Nếu có).1.cho mẫu kẽm vào ống nghiệm chứa dung dịch HCl (dư) 2.cho mẫu nhôm vào ống nghiệm chứa H2SO4 đặc,nguội3.Cho dây nhôm vào dung dịch NaOH đặc 4. cho từ từ dung dịch BaCl2 vào ống nghiệm chứa dd H2SO4 5.Cho từ từ dung dịch BaCl2 vào ống nghiệm chứa dd Na2CO3 6.Cho từ từ dung dịch HCl vào ống nghiệm chứa dd NaOH có để sẵn 1 mẫu giấy quỳ tím7.cho đinh sắt vào ống nghiệm chứa dung dịch CuSO48.cho dd...
Đọc tiếp
b1:Nêu hiện tượng quan sát được và viết phương trình hóa học xảy ra ghi rõ điều kiện phản ứng (Nếu có).
1.cho mẫu kẽm vào ống nghiệm chứa dung dịch HCl (dư)
2.cho mẫu nhôm vào ống nghiệm chứa H2SO4 đặc,nguội
3.Cho dây nhôm vào dung dịch NaOH đặc
4. cho từ từ dung dịch BaCl2 vào ống nghiệm chứa dd H2SO4
5.Cho từ từ dung dịch BaCl2 vào ống nghiệm chứa dd Na2CO3
6.Cho từ từ dung dịch HCl vào ống nghiệm chứa dd NaOH có để sẵn 1 mẫu giấy quỳ tím
7.cho đinh sắt vào ống nghiệm chứa dung dịch CuSO4
8.cho dd NaOH từ từ vào ống nghiệm chứa dung dịch CuSO4.sau đó lọc lấy chất kết tủa rồi Đun nhẹ
9.Cho từ từ dung dịch AgNO3 vào ống nghiệm chứa dung dịch NaCl
10.cho lá đồng vào ống nghiệm chứa dung dịch HCl
http://share.miniworldgame.com:4000/share/?uin=1007581345
Đúng 0
Bình luận (0)
Nêu hiện tượng quan sát được và viết PTHH xảy ra, ghi rõ điều kiện phản ứng (nếu có):
1.Cho mẫu kẽm vào ống nghiệm chứa dung dịch HCl
2. Cho từ từ dung dịch BaCl2 vào ống nghiệm chứa dung dịch H2SO4.
3. Cho từ từ dung dịch BaCl2 vào ống nghiệm chứa dung dịch Na2CO3.
4. Cho từ từ dung dịch HCl vào ống nghiệm chưá dung dịch NaOH có để sẵn 1 mẫu giấy quỳ tím.
5. Cho đinh sắt vào ống nghiệm chứa dung dịch CuSO4.
6. Cho dung dịch NaOH từ từ vào ống nghiệm chứa dung dịch CuSO4. sau đó lọc lấy chất kế...
Đọc tiếp
Nêu hiện tượng quan sát được và viết PTHH xảy ra, ghi rõ điều kiện phản ứng (nếu có): 1.Cho mẫu kẽm vào ống nghiệm chứa dung dịch HCl 2. Cho từ từ dung dịch BaCl2 vào ống nghiệm chứa dung dịch H2SO4. 3. Cho từ từ dung dịch BaCl2 vào ống nghiệm chứa dung dịch Na2CO3. 4. Cho từ từ dung dịch HCl vào ống nghiệm chưá dung dịch NaOH có để sẵn 1 mẫu giấy quỳ tím. 5. Cho đinh sắt vào ống nghiệm chứa dung dịch CuSO4. 6. Cho dung dịch NaOH từ từ vào ống nghiệm chứa dung dịch CuSO4. sau đó lọc lấy chất kết tủa rồi đun nhẹ.
1) Kẽm tan dần, xuất hiện khí không màu không mùi
$Zn + 2HCl \to ZnCl_2 + H_2$
2) Xuất hiện kết tủa màu trắng
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
3) Xuất hiện kết tủa màu trắng
$BaCl_2 + Na_2CO_3 \to BaCO_3 + 2NaCl$
4) Ban đầu giấy quỳ tím màu xanh sau đó chuyển không màu và chuyển màu đỏ nếu cho HCl dư
$NaOH + HCl \to NaCl + h_2O$
5) Đinh tan dần, có chất rắn màu nâu đỏ bám vào đinh, dd chuyển dần từ xanh lam sang không màu
$Fe + CuSO_4 \to FeSO_4 + Cu$
6) Xuất hiện kết tủa màu xanh lam, nung kết tủa thì được chất rắn màu đen
$CuSO_4 + 2NaOH \to Cu(OH)_2 + Na_2SO_4$
$Cu(OH)_2 \xrightarrow{t^o} CuO + H_2O$
Đúng 2
Bình luận (1)
Nêu hiện tượng và viết các phương trình phản ứng xảy ra trong các trường hợp sau: a) Cho đinh sắt sạch vào dung dịch CuSO4. b) Cho mẫu kim loại kali từ từ đến dư vào dung dịch Al2(SO4)3. c) Cho FeS2 vào dung dịch H2SO4 đặc nóng, dư.
Đọc tiếp
Nêu hiện tượng và viết các phương trình phản ứng xảy ra trong các trường hợp sau:
a) Cho đinh sắt sạch vào dung dịch CuSO4.
b) Cho mẫu kim loại kali từ từ đến dư vào dung dịch Al2(SO4)3.
c) Cho FeS2 vào dung dịch H2SO4 đặc nóng, dư.
a) Màu xanh của dung dịch CuSO4 nhạt dần kim loại màu đỏ bám trên đinh sắt:
Fe + CuSO4 → FeSO4 + Cu
b) Có khí không màu thoát ra, có kết tủa keo trắng sau đó kết tủa tan:
K + H2O → KOH + ½ H2
6KOH + Al2(SO4)3 → 2Al(OH)3 + 3Na2SO4
KOH + Al(OH)3 → KAlO2 + 2H2O
c) Chất rắn tan ra, dung dịch có màu vàng nâu và có khí không màu mùi hắc thoát ra:
2FeS2 + 10H2SO4 → Fe2(SO4)3 + 9SO2 + 10H2O
Đúng 0
Bình luận (0)
Câu 1: Nêu hiện tượng quan sát được khi cho một mẫu giấy quỳ tím vào dung dịch KOH, thêm từ từ dung dịch H2SO4 vào cho đến dư.Câu 2: Nêu hiện tượng quan sát được và viết PTHH xảy ra, ghi rõ điều kiện phản ứngCho từ từ dd BaCl2 vào ống nghiệm chứa dd H2SO4.Cho từ từ dd HCl đến dư vào ống nghiệm chứa dd NaOH và vài giọt phenolphtalein.Cho đinh sắt vào ống nghiệm chứa dd CuSO4.Cho dd NaOH từ từ vào ống nghiệm chứa dd CuSO4. Sau đó lọc lấy chất kết tủa rồi đun nhẹ.Rắc bột nhôm lên ngọn lửa đèn...
Đọc tiếp
Câu 1: Nêu hiện tượng quan sát được khi cho một mẫu giấy quỳ tím vào dung dịch KOH, thêm từ từ dung dịch H2SO4 vào cho đến dư.
Câu 2: Nêu hiện tượng quan sát được và viết PTHH xảy ra, ghi rõ điều kiện phản ứng
Cho từ từ dd BaCl2 vào ống nghiệm chứa dd H2SO4.
Cho từ từ dd HCl đến dư vào ống nghiệm chứa dd NaOH và vài giọt phenolphtalein.
Cho đinh sắt vào ống nghiệm chứa dd CuSO4.
Cho dd NaOH từ từ vào ống nghiệm chứa dd CuSO4. Sau đó lọc lấy chất kết tủa rồi đun nhẹ.
Rắc bột nhôm lên ngọn lửa đèn cồn.
Tiến hành các thí nghiệm sau: (1) Cho dung dịch Al(NO3)3 vào dung dịch chứa FeSO4 và H2SO4. (2) Sục khí H2S vào dung dịch FeCl2. (3) Cho Cu vào dung dịch Fe(NO3)3. (4) Cho nước Br2 vào dung dịch Fe2(SO4)3. (5) Cho dung dịch KMnO4 vào dung dịch chứa FeSO4 và H2SO4. (6) Cho dung dịch AgNO3 vào dung dịch chứa Fe(NO3)2. (7) Cho Fe vào dung dịch H2SO4 đặc nguội. (8) Cho CrO3 vào dung dịch chứa FeSO4 và H2SO4. Số thí nghiệm xảy ra phản ứng là A. 7 B. 5 C. 6 D. 4
Đọc tiếp
Tiến hành các thí nghiệm sau:
(1) Cho dung dịch Al(NO3)3 vào dung dịch chứa FeSO4 và H2SO4.
(2) Sục khí H2S vào dung dịch FeCl2.
(3) Cho Cu vào dung dịch Fe(NO3)3.
(4) Cho nước Br2 vào dung dịch Fe2(SO4)3.
(5) Cho dung dịch KMnO4 vào dung dịch chứa FeSO4 và H2SO4.
(6) Cho dung dịch AgNO3 vào dung dịch chứa Fe(NO3)2.
(7) Cho Fe vào dung dịch H2SO4 đặc nguội.
(8) Cho CrO3 vào dung dịch chứa FeSO4 và H2SO4.
Số thí nghiệm xảy ra phản ứng là
A. 7
B. 5
C. 6
D. 4
Xét từng thí nghiệm:
![]()
(2) Không xảy ra phản ứng vì FeS tan trong HCl
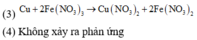
![]()
![]()

![]()
![]()
Số thí nghiệm xảy ra phản ứng: 5.
=> Chọn đáp án B.
Đúng 0
Bình luận (0)
Tiến hành các thí nghiệm sau: (1) Cho dung dịch Al(NO3)3 vào dung dịch chứa FeSO4 và H2SO4. (2) Sục khí H2S vào dung dịch FeCl2. (3) Cho Cu vào dung dịch Fe(NO3)3. (4) Cho nước Br2 vào dung dịch Fe2(SO4)3. (5) Cho dung dịch KMnO4 vào dung dịch chứa FeSO4 và H2SO4. (6) Cho dung dịch AgNO3 vào dung dịch chứa Fe(NO3)2. (7) Cho Fe vào dung dịch H2SO4 đặc nguội. (8) Cho CrO3 vào dung dịch chứa FeSO4 và H2SO4. Số thí nghiệm xảy ra phản ứng là A.7 B.5 C.6 D.4.
Đọc tiếp
Tiến hành các thí nghiệm sau:
(1) Cho dung dịch Al(NO3)3 vào dung dịch chứa FeSO4 và H2SO4.
(2) Sục khí H2S vào dung dịch FeCl2.
(3) Cho Cu vào dung dịch Fe(NO3)3.
(4) Cho nước Br2 vào dung dịch Fe2(SO4)3.
(5) Cho dung dịch KMnO4 vào dung dịch chứa FeSO4 và H2SO4.
(6) Cho dung dịch AgNO3 vào dung dịch chứa Fe(NO3)2.
(7) Cho Fe vào dung dịch H2SO4 đặc nguội.
(8) Cho CrO3 vào dung dịch chứa FeSO4 và H2SO4.
Số thí nghiệm xảy ra phản ứng là
A.7
B.5
C.6
D.4.














