Viết các phương trình phản ứng xảy ra giữa các cặp chất sau:
PhotPho+Oxi
Sắt+Oxi
Hiđrô+Sắt(III)ô-xit
Sắt photpho lưu huỳnh oxi hiđrô các phương trình phản ứng xảy ra sau khi cho 2 chất tác dụng với nhau
3Fe + 2O2 ---to→ Fe3O4
4P + 5O2 ---to→ 2P2O5
S + O2 ---to→ SO2
2H2 + O2 ---to→ 2H2O
Thực hiện phản ứng giữa các cặp chất sau:
1. F e 2 O 3 + H N O 3 →
2. F e C l 3 + F e →
3. F e 2 S O 4 3 + C u →
4. A l + F e 2 O 3 →
Các phản ứng xảy ra mà trong đó hợp chất sắt (III) thể hiện tính oxi hóa là
A. 1, 2, 4.
B. 2, 3, 4.
C. 1, 2, 3.
D. 1, 3, 4.
Cho 24g hỗn hợp gồm sắt (III) ôxít và đồng (II) oxit dùng hiđrô hứa sau phản ứng thu được 17,6 gam hỗn hợp hai kim loại ở nhiệt độ cao A viết các phương trình phản ứng xảy ra b.tính thể tích hiđrô cần dùng ở điều kiện tiêu chuẩn c.tính khối lượng mỗi ôxít đã phản ứng D.tính phần trăm theo khối lượng mỗi ôxít
a, PT: \(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
b, Theo PT: \(n_{H_2}=n_{H_2O}=a\left(mol\right)\)
Theo ĐLBT KL, có: m oxit + mH2 = mKL + mH2O
⇒ 24 + 2a = 17,6 + 18a ⇒ a = 0,4 (mol)
\(\Rightarrow V_{H_2}=0,4.22,4=8,96\left(l\right)\)
c, Gọi: \(\left\{{}\begin{matrix}n_{Fe_2O_3}=x\left(mol\right)\\n_{CuO}=y\left(mol\right)\end{matrix}\right.\) ⇒ 160x + 80y = 24 (1)
Theo PT: \(\left\{{}\begin{matrix}n_{Fe}=n_{Fe_2O_3}=2x\left(mol\right)\\n_{Cu}=n_{CuO}=y\left(mol\right)\end{matrix}\right.\) ⇒ 56.2x + 64y = 17,6 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,1.160=16\left(g\right)\\m_{CuO}=0,1.80=8\left(g\right)\end{matrix}\right.\)
d, \(\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\dfrac{16}{24}.100\%\approx66,67\%\\\%m_{CuO}\approx33,33\%\end{matrix}\right.\)
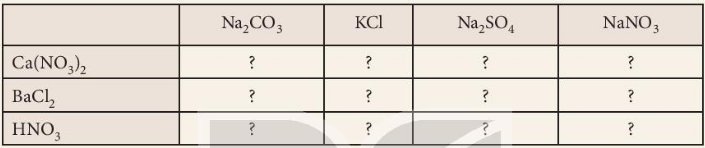
Trong dung dịch, giữa các cặp chất nào sau đây có xảy ra phản ứng? Viết phương trình hoá học của các phản ứng đó.
| Na2CO3 | KCl | Na2SO4 | NaNO3 | |
| Ca(NO3)2 | Có phản ứng (1) | Không phản ứng | Có phản ứng (2) | Không phản ứng |
| BaCl2 | Có phản ứng (3) | Không phản ứng | Có phản ứng (4) | Không phản ứng |
| HNO3 | Có phản ứng (5) | Không phản ứng | Không phản ứng | Không phản ứng |
Các PTHH:
\(\left(1\right)Ca\left(NO_3\right)_2+Na_2CO_3\rightarrow2NaNO_3+CaCO_3\downarrow\\ \left(2\right)Na_2SO_4+Ca\left(NO_3\right)_2\rightarrow CaSO_4+2NaNO_3\\ \left(3\right)Na_2CO_3+BaCl_2\rightarrow BaCO_3+2NaCl\\ \left(4\right)Na_2SO_4+BaCl_2\rightarrow BaSO_4+2NaCl\\ \left(5\right)2HNO_3+Na_2CO_3\rightarrow2NaNO_3+CO_2+H_2O\)
Viết phương trình phân tử và phương trình ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch giữa các cặp chất sau: MgCl2 + KNO3
Viết phương trình phân tử và phương trình ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch giữa các cặp chất sau: HClO + KOH
HClO +KOH → KClO + H2O
HClO + OH- → H2O + ClO-
Viết phương trình phân tử và phương trình ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch giữa các cặp chất sau: NH4Cl + AgNO3
NH4Cl + AgNO3 → NH4NO3 + AgCl ↓
Ag+ + Cl- → AgCl ↓
Viết phương trình phân tử và phương trình ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch giữa các cặp chất sau: NaF + HCl
Viết phương trình phân tử và phương trình ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch giữa các cặp chất sau: FeS (r) + 2HCl
FeS (r) +2HCl → FeCl2 + H2S ↑
FeS (r) + 2H+ → Fe2+ + H2S ↑