crackinh propan thu được 8,8 gam hh khí A gồm H2, CH4, C2H6, C3H6 và C3H8 dư. Hiệu xuất p/ứ đạt 90%. Dẫn hh khí A qua dd Brom vừa đủ thì có bao nhiêu gam Brom p/ứ
Crackinh 8,8 gam propan thu được hh A gồm H2, CH4, C2H4, C3H6 và một phần propan chưa bị crackinh. Biết % propan phản ứng là 90%. Khối lượng phân tử trung bình của A là:
A. 39,6
B. 23,16
C. 2,315
D. 3,96
Crackinh propan thu được 67,2 lít (đktc) hỗn hợp X gồm H2, C3H6, CH4, C2H4, C3H8. Dẫn toàn bộ X vào bình đựng dung dịch Br2 dư thì thấy có 160 gam brom phản ứng (biết rằng chỉ có C2H4, C3H6 phản ứng với Br2 và đều theo tỉ lệ số mol 1:1). Vậy % propan đã phản ứng là:
A. 20 %
B. 25%
C. 50 %
D. 75 %
Crackinh 4,48 lít butan (đktc), thu được hỗn hợp X gồm 6 chất H2, CH4, C2H6, C2H4, C3H6, C4H8. Dẫn hết hỗn hợp X vào bình dung dịch brom dư thì thấy khối lượng bình brom tăng 8,4 gam và bay ra khỏi bình brom là hỗn hợp khí Y. Thể tích oxi (đktc) cần đốt hết hỗn hợp Y là :
A. 6,72 lít
B. 4,48 lít
C. 5,6 lít
D. 8,96 lít.
Hổn hợp X gồm propan, etilen, propin. Dẫn 2,24 lít hổn hợp X qua dd brom dư thấy có 20,8g brom phản ứng . Đốt cháy hoàn toàn khí thoát ra thu được 1,44 gam H2O. a. Viết các pthh xảy ra và tính phần trăm thể tích mỗi khí có trong hh X B. Dẫn 9,3 gam hh X qua dd AgNO3/ NH3 dư thu được bao nhiêu gam kết tủa
Dẫn V lít khí propan qua ống sử đựng xúc tác ở nhiệt độ thích hợp thu được 19,6 lít hỗn hợp khí X chỉ gồm CH4, C2H4, C3H6, H2 và C3H8 dư. Dẫn hỗn hợp X từ từ qua dung dịch nước brom dư, đến phản ứng hoàn toàn thấy tiêu tốn hết 60 gam Br2. Giá trị của V là (các khí đều đo ở đktc)
A. 8,4.
B. 9,8.
C. 11,2.
D. 16,8.
Crackinh 0,4 mol C4H10 thu đc hh X gồm 5 hidrocacbon. Dẫn X qua dd nước brom dư thấy bình đựng nước brom tăng 8,4 gam và có khí Y thoát ra. Đốt cháy hoàn toàn Y cần V lít khí O2 (ở đktc). Tính giá trị của V ?
\(C_4H_{10}\underrightarrow{cracking}X\left\{{}\begin{matrix}C_3H_6+CH_4\\C_2H_4+C_2H_6\\C_4H_{10\left(dư\right)}\end{matrix}\right.\underrightarrow{ddBr_2}Y\left\{{}\begin{matrix}CH_4\\C_2H_6\\C_4H_{10\left(dư\right)}\end{matrix}\right.\)
m bình tăng = manken = 8,4 (g)
Coi hỗn hợp anken là CH2.
Ta có: \(n_{CH_2}=\dfrac{8,4}{14}=0,6\left(mol\right)\)
PT: \(2CH_2+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{3}{2}n_{CH_2}=0,9\left(mol\right)\)
\(2C_4H_{10}+13O_2\underrightarrow{t^o}8CO_2+10H_2O\)
Theo PT: \(n_{O_2}=\dfrac{13}{2}n_{C_4H_{10}}=2,6\left(mol\right)\)
Có: nO2 (đốt cháy C4H10) = nO2 (đốt cháy anken) + nO2 (đốt cháy ankan Y)
⇒ nO2 (đốt cháy Y) = 2,6 - 0,9 = 1,7 (mol)
\(\Rightarrow V_{O_2}=1,7.22,4=38,08\left(l\right)\)
Cho hh X gồm CH4, C2H4 và C2H2. Lấy 8,6 gam X t/d hết với dd brom (dư) thì khối lượng brom pư là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hh khí X t/d với lượng dư dd AgNO3 trong NH3, thu được 36 gam kết tủa. Phần trăm thể tích của CH4 có trong X là
A. 20%
B. 50%
C. 25%
D. 40%
Đáp án B
Gọi x, y, z 1à số mol của CH4, C2H4 và C2H2 trong 8,6g hh X
=> 16x + 28y + 26z = 8,6 (1)
- Khi cho X td với dung dịch Br2 dư:
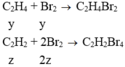
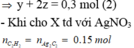

a)
\(C_2H_4 + Br_2 \to C_2H_4Br_2 n_{C_2H_4} = n_{Br_2} = \dfrac{8}{160} = 0,05(mol)\\ \Rightarrow \%V_{C_2H_4} = \dfrac{0,05.22,4}{2,24} .100\%= 50\%\\ \%V_{C_2H_4} = 100\%-50\% = 50\%\)
b)
\(C_2H_4 + H_2 \xrightarrow{t^o,Ni} C_2H_6\\ n_{H_2\ pư} = n_{C_2H_6} = \dfrac{0,896}{22,4} = 0,04(mol)\\ \Rightarrow m_{H_2\ pư} = 0,04.2 = 0,08(gam)\)
một hỗn hợp khí A gồm 0.5 mol H2 va 0.3 mol ankin X. Nung A một thời gian với xúc tác Ni thu được hh B có tỉ số với H2 bằng 16.25. Dẫn hh B qua dd brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là 32 gam. X là?
Bảo toàn π: n(π) = nH2phản ứng + nBr2 → nH2 = 0,4 (mol)
n(B) = n(A) - nH2phản ứng = 0,4 (mol)
→ mB = 16,25 * 0,4* 2 = 13 (g) = mA (BTKL)
→ mX = 12 (g) → MX = 40 → C3H4