Nguyên tố chlorine có Z = 17. Hãy cho biết số lớp electron, số electron thuộc lớp ngoài cùng, số electron độc thân của nguyên tử chlorine

Những câu hỏi liên quan
Quan sát hình 3.5 và bảng tuần hoàn, hãy cho biết số electron lớp ngoài cùng của nguyên tử Li (lithium) và Cl (chlorine). Hai nguyên tố đó nằm ở nhóm nào trong bảng tuần hoàn?
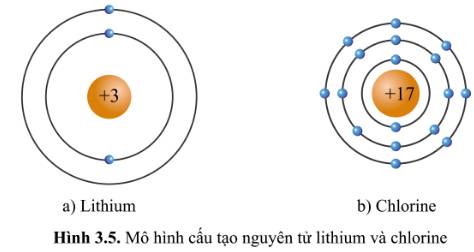
- Xét mô hình cấu tạo của nguyên tử lithium: có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp vỏ ngoài cùng => Thuộc nhóm IA
- Xét mô hình cấu tạo của nguyên tử chlorine: có 7 hình tròn xanh ở vòng tròn ngoài cùng => Có 7 electron ở lớp vỏ ngoài cùng => Thuộc nhóm VIIA
Đúng 0
Bình luận (0)
Ở trạng thái cơ bản, nguyên tử của nguyên tố X có lớp electron ngoài cùng là lớp L chứa 2 electron độc thân và không còn chứ orbitan trống. Trong nguyên tử nguyên tố Y có tổng số electron thuộc các phân lớp p là 11a) Viết cấu hình electron và xác ịnh vị trí của X, Y trong bảng tuần hoànb) Viết công thức hóa học của tất cả các hợp chất tạo bởi 3 nguyên tố X, Y và hydrogen, So sáng tính axit của các hợp chất này, giải thích tại sao?
Đọc tiếp
Ở trạng thái cơ bản, nguyên tử của nguyên tố X có lớp electron ngoài cùng là lớp L chứa 2 electron độc thân và không còn chứ orbitan trống. Trong nguyên tử nguyên tố Y có tổng số electron thuộc các phân lớp p là 11
a) Viết cấu hình electron và xác ịnh vị trí của X, Y trong bảng tuần hoàn
b) Viết công thức hóa học của tất cả các hợp chất tạo bởi 3 nguyên tố X, Y và hydrogen, So sáng tính axit của các hợp chất này, giải thích tại sao?
a. X: \(1s^{^2}2s^{^2}2p^{^4}\)
Vị trí: ô 8, chu kì 2, nhóm VIA (nguyên tố oxygen, O)
Y: \(1s^{^2}2s^{^2}2p^{^6}3s^{^2}3p^{^5}\)
Vị trí: ô 17, chu kì 3, nhóm VIIA (nguyên tố chlorine, Cl)
b. \(HClO,HClO_2,HClO_3,HClO_4\)
Tính acid tăng dần từ trái sang phải trong dãy trên vì trong phân tử acid cấu tạo từ các nguyên tố giống nhau thì phân tử nào chứa nhiều nguyên tử O hơn thì có tính acid mạnh hơn
Đúng 2
Bình luận (1)
vẽ sơ đồ cấu tạo nguyên tử nguyên tố O(Z=8),Mg(Z=17),Ca(Z=20).Cho biết số lớp electron và số electron lớp ngoài cùng mỗi loại nguyên tử
Nguyên tố X có cấu hình electron nguyên tử
1
s
2
2
s
2
2
p
6
3
s
2
3
p
2
Hãy cho biết số lớp electron và số electron...
Đọc tiếp
Nguyên tố X có cấu hình electron nguyên tử 1 s 2 2 s 2 2 p 6 3 s 2 3 p 2
Hãy cho biết số lớp electron và số electron ở lớp ngoài cùng.
Nguyên tử có 3 lớp, lớp ngoài cùng có 4 electron.
Đúng 0
Bình luận (0)
Hãy viết cấu hình electron của các nguyên tử có Z = 3 đến Z = 10 và nhận xét về số electron thuộc lớp ngoài cùng của nguyên tử các nguyên tố trong dãy đó.
Từ Z = 3 đến Z = 10 ta có các nguyên tử :
Li: 1 s 2 2 s 1 ; Be: 1 s 2 2 s 2 ; B: 1 s 2 2 s 2 2 p 1 ; C: 1 s 2 2 s 2 2 p 2
N: 1 s 2 2 s 2 2 p 3 ; O: 1 s 2 2 s 2 2 p 4 ; F: 1 s 2 2 s 2 2 p 5 ; Ne: 1 s 2 2 s 2 2 p 6
Nhận xét : Số electron thuộc lớp ngoài cùng của các nguyên tử đó tăng dần từ 1 (Li) đến 8 (Ne).
Đúng 0
Bình luận (0)
Nguyên tử của nguyên tố Z có 4 lớp electron, lớp ngoài cùng có 6 electron. Số hiệu nguyên tử của Z là
A. 24
B. 34
C. 36
D. 16
Nguyên tử của nguyên tố Z có 4 lớp electron, lớp ngoài cùng có 6 electron. Số hiệu nguyên tử của Z là:
A. 24
B. 34
C. 36
D. 16
Đáp án B
Cấu hình electron của Z là: 1s22s22p63s23p63d104s24p4
Số hiệu nguyên tử của Z là 34
Đúng 0
Bình luận (0)
Nguyên tử nguyên tố X có Z = 17. Số electron thuộc lớp ngoài cùng của X là giá trị nào dưới đây?
A. 1.
B. 2.
C. 7.
D.3.
Đáp án C.
Cấu hình electron của X: 1s22s22p63s23p5
Đúng 0
Bình luận (0)
cho biết tên , kí hiệu , số hiệu nguyên tử của : a) 2 nguyên tố mà nguyên tử có số electron lớp ngoài cùng là tối đa ; b) 2 nguyên tố mà nguyên tử có 1 electron ở lớp ngoài cùng ; c) 2 nguyên tố mà nguyên tử có 7 electron ở lớp ngoài cùng
HD:
a) Lấy 2 nguyên tố khí hiếm, ví dụ: 24He (1s2) và 1020Ne (1s22s22p6).
b) Lấy 2 nguyên tố thuộc nhóm IA, ví dụ: 11H (1s1) và 37Li (1s22s1).
c) Lấy 2 nguyên tố thuộc nhóm VIIA, ví dụ: 919F (1s22s22p5) và 1735Cl (1s22s22p63s23p5).
Đúng 0
Bình luận (0)
HD:
a) Lấy 2 nguyên tố khí hiếm, ví dụ: 24He (1s2) và 1020Ne (1s22s22p6).
b) Lấy 2 nguyên tố thuộc nhóm IA, ví dụ: 11H (1s1) và 37Li (1s22s1).
c) Lấy 2 nguyên tố thuộc nhóm VIIA, ví dụ: 919F (1s22s22p5) và 1735Cl (1s22s22p63s23p5).
Đúng 0
Bình luận (0)
Xem thêm câu trả lời















