Tính khối lượng của 0,2479 lít khí N2O

Những câu hỏi liên quan
Tính khối lượng Nitơ có trong:
a) 8,8 gam N2O. b) 6.1023 phân tử NH4NO3. c) 6,72 lít khí NO ( đktc).
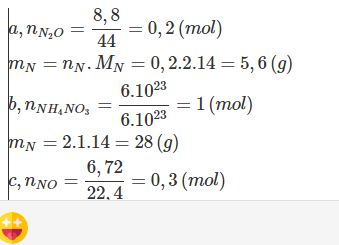
=> mN=nN.14=0,3.14=4,2(g)
Nãy lỗi mạng quá
Đúng 0
Bình luận (0)
\(a.n_{N_2O}=\dfrac{8,8}{44}=0,2\left(mol\right)\\ \Rightarrow n_N=2n_{N_2O}=0,4\left(mol\right)\\ \Rightarrow m_N=0,4.14=5,6\left(g\right)\\ b.n_N=2n_{NH_4NO_3}=\dfrac{2.6.10^{23}}{6.10^{23}}=2\left(mol\right)\\ \Rightarrow m_N=2.14=28\left(g\right)\\ c.n_N=n_{NO}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ \Rightarrow m_N=0,3.14=4,2\left(g\right)\)
Đúng 0
Bình luận (0)
Hoà tan a gam Al trong dung dịch HNO3 loãng thu được 0,896 lít hỗn hợp khí X gồm N2O và NO (đktc). Tỷ khối hơi của X so với H2 bằng 18,5.
a. Tính % khối lượng các khí trong hỗn hợp ?
\(\left\{{}\begin{matrix}n_{N_2O}+n_{NO}=0,04\\44n_{N_2O}+30n_{NO}=18,5.2.0,04=1,48\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{N_2O}=0,02\left(mol\right)\\n_{NO}=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{N_2O}=\dfrac{0,02.44}{1,48}.100\%=59,46\%\\\%m_{NO}=\dfrac{0,02.30}{1,48}.100\%=40,54\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho hỗn hợp rắn X chứa Fe3O4, FeCO3, Al (trong đó số mol của Fe3O4 là 1/3 mol )tác dụng với 0,2479 lít(đktc) khí O2 đun nóng, kết thúc phản ứng chỉ thu được hỗn hợp rắn Y và 0,2479 lít khí CO2 .Cho Y phản ứng với HCl vừa đủ thu được 1,344 lít hỗn hợp khí Z và dung dịch T. Cho AgNO3 dư vào dung dịch T, phản ứng xảy ra hoàn toàn thấy có 101,59 gam kết tủa. Biết các khí đo ở đktc. Tính khối lượng của X
Đọc tiếp
Cho hỗn hợp rắn X chứa Fe3O4, FeCO3, Al (trong đó số mol của Fe3O4 là 1/3 mol )tác dụng với 0,2479 lít(đktc) khí O2 đun nóng, kết thúc phản ứng chỉ thu được hỗn hợp rắn Y và 0,2479 lít khí CO2 .Cho Y phản ứng với HCl vừa đủ thu được 1,344 lít hỗn hợp khí Z và dung dịch T. Cho AgNO3 dư vào dung dịch T, phản ứng xảy ra hoàn toàn thấy có 101,59 gam kết tủa. Biết các khí đo ở đktc. Tính khối lượng của X
Hòa tan hoàn toàn 4,48 gam bột sắt vào lượng dư axit HNO3 thu được V lít khí (đktc) hỗn hợp khí gồm N2O và N2, không có sản phẩm khử khác. Tỉ khối của A so với H2 là 18,45. Viết ptpư, tính V
Gọi số mol N2O, N2 là a, b (mol)
Có: \(\overline{M}_A=\dfrac{44a+28b}{a+b}=18,45.2=36,9\left(g/mol\right)\)
=> 7,1a = 8,9b (1)
PTHH: 8Fe + 30HNO3 --> 8Fe(NO3)3 + 3N2O + 15H2O
\(\dfrac{8}{3}a\)<-------------------------------a
10Fe + 36HNO3 --> 10Fe(NO3)3 + 3N2 + 18H2O
\(\dfrac{10}{3}b\)<------------------------------b
=> \(\dfrac{8}{3}a+\dfrac{10}{3}b=\dfrac{4,48}{22,4}=0,2\) (2)
(1)(2) => \(\left\{{}\begin{matrix}a=\dfrac{89}{2370}\left(mol\right)\\b=\dfrac{71}{2370}\left(mol\right)\end{matrix}\right.\) => \(V=\left(\dfrac{89}{2370}+\dfrac{71}{2370}\right).22,4=\dfrac{1792}{1185}\left(l\right)\)
Đúng 2
Bình luận (0)
Hãy tính:
(a) Số mol nguyên tử Fe, O trong 4,64 gam Fe3O4.
(b) Số lượng nguyên tử N, O trong 3,36 lít khí N2O (đktc).
(c) Khối lượng nguyên tố H, S, O trong 4,9 gam H2SO4.
a) \(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=3n_{Fe_3O_4}=0,06\left(mol\right)\\n_O=4n_{Fe_3O_4}=0,08\left(mol\right)\end{matrix}\right.\)
b) \(n_{N_2O}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_N=2n_{N_2O}=0,3\left(mol\right)\\n_O=n_{N_2O}=0,15\left(mol\right)\end{matrix}\right.\)
c) Ta có: \(n_{H_2SO_4}=\dfrac{4,9}{98}=0,05\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_H=2n_{H_2SO_4}=0,1\left(mol\right)\\n_S=n_{H_2SO_4}=0,05\left(mol\right)\\n_O=4n_{H_2SO_4}=0,2\left(mol\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 20 gam dung dịch H2SO4 4,9% tác dụng hết với dung dịch K2SO3.a) Tính thể tích khí CO2 thu được (điều kiện chuẩn). Đ/S: 0,2479 lítb) Dẫn toàn bộ khí CO2 thu được qua dung dịch Ca(OH)2 dư thu được CaCO3 và H2O. Tính khối lượng kết tủa thu được. Đ/S: 1 gam(Cho H1; S32; O16; Ca40; C12)*Đã cho sẵn đáp án, hoàn thành quá trình làm bài rồi so sánh kết quả.
Đọc tiếp
Cho 20 gam dung dịch H2SO4 4,9% tác dụng hết với dung dịch K2SO3.
a) Tính thể tích khí CO2 thu được (điều kiện chuẩn). Đ/S: 0,2479 lít
b) Dẫn toàn bộ khí CO2 thu được qua dung dịch Ca(OH)2 dư thu được CaCO3 và H2O. Tính khối lượng kết tủa thu được. Đ/S: 1 gam
(Cho H=1; S=32; O=16; Ca=40; C=12)
*Đã cho sẵn đáp án, hoàn thành quá trình làm bài rồi so sánh kết quả.
Hỗn hợp X gồm 3 khí: N2O, CO2, C3H8 có % khối lượng bằng nhau. Dẫn 3,36 lít X qua dung dịch Ba(OH)2 dư thấy có V lít khí thoát ra (các thể tích đo ở đktc). Giá trị của V là
A. 2,24 lít. B. 3,36 lít. C. 1,12 lít. D. (3,36 – V) lít.
Gọi số mol của N2O, CO2, C3H8 là a, b, c
=> \(\left\{{}\begin{matrix}a+b+c=\dfrac{3,36}{22,4}=0,15\\44a=44b=44c\end{matrix}\right.\)
=> a = b = c = 0,05 (mol)
Khí thoát ra gồm N2O, C3H8
=> V = (0,05 + 0,05).22,4 = 2,24(l)
=> A
Đúng 1
Bình luận (0)
Gọi số mol của N2O, CO2, C3H8 là a, b, c
=>
Đúng 0
Bình luận (0)
Hỗn hợp A gồm CO2 ,N2O và H2 biết 1,12 lít hỗn hợp A có khối lượng là 1,78g ,lấy lượng H2 trong A trộn với 0,672 lít khí x thu được hỗn hợp B có khối lượng là 0,14g .Tìm x
\(n_{CO_2}=a\left(mol\right),n_{N_2O}=b\left(mol\right),n_{H_2}=c\left(Mol\right)\)
\(n_A=a+b+c=0.05\left(mol\right)\)
\(\Leftrightarrow44a+44b+44c=2.2\left(1\right)\)
\(m_A=44a+44b+2c=1.78\left(g\right)\left(2\right)\)
\(\Rightarrow c=0.01\)
\(m_B=0.01\cdot2+0.03\cdot X=0.14\left(g\right)\)
\(\Rightarrow X=4\)
\(X:He\)
Đúng 1
Bình luận (0)
Hỗn hợp khí N2 và N2O có tỉ khối so với O2 là 1. Tính Thể tích khí N2O cần thêm vào 8,96 lít hỗn hợp trên (đktc) để có tỉ khối so với O2 tăng lên bằng 1,075




















