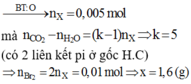đốt cháy 2,4 gam kim loại M hóa trị n cần 1,12 lít O2 điều kiện tiêu chuẩn xd kloai M

Những câu hỏi liên quan
đốt cháy kim loại M hóa trị 1 cần 0,672 lít O2 điều kiện tiêu chuẩn thu được 3,72 gam oxit xác định kim loại M
\(4M+O_2\rightarrow\left(t^o\right)2M_2O\\ n_{O_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\ n_{oxit}=2.0,03=0,06\left(mol\right)\\ M_{oxit}=2M_M+16=\dfrac{3,72}{0,06}=62\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow M_M=\dfrac{62-16}{2}=23\left(\dfrac{g}{mol}\right)\left(M:Natri\left(Na=23\right)\right)\)
Đúng 1
Bình luận (1)
: đốt cháy hoàn toàn 7,8g hỗn hợp A gồm 2 kim loại Magie và Nhôm cần dùng 4,48 lít khí Oxi ở điều kiện tiêu chuẩn thấy tạo ra m gam 2 oxit.
a) viết phương trình hóa học
b)tính khối lượng và % khối lượng mỗi kim loại trong hỗn hợp A
c) tính m
a) 2Mg + O2 --to--> 2MgO
4Al + 3O2 --to--> 2Al2O3
b) Gọi số mol Mg, Al là a, b
=> 24a + 27b = 7,8
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2Mg + O2 --to--> 2MgO
______a--->0,5a-------->a
4Al + 3O2 --to--> 2Al2O3
b-->0,75b------->0,5b
=> 0,5a + 0,75b = 0,2
=> a = 0,1 ; b = 0,2
=> mMg = 0,1.24 = 2,4 (g); mAl = 0,2.27 = 5,4 (g)
=> \(\left\{{}\begin{matrix}\%Mg=\dfrac{2,4}{7,8}.100\%=30,769\%\\\%Al=\dfrac{5,4}{7,8}.100\%=69,231\%\end{matrix}\right.\)
c) \(\left\{{}\begin{matrix}n_{MgO}=0,1\left(mol\right)\\n_{Al_2O_3}=0,1\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{MgO}=0,1.40=4\left(g\right)\\m_{Al_2O_3}=0,1.102=10,2\left(g\right)\end{matrix}\right.\)
=> m = 4 + 10,2 = 14,2 (g)
Đúng 0
Bình luận (0)
Câu 36. Khi phân hủy có xúc tác 14,7 gam KClO3, thể tích khí oxi thu được làA. 4,032 lít. B. 8,064 lít. C. 7,092 lít. D. 12, 096 lít.Câu 37. Đốt cháy hoàn toàn 4,6 gam một kim loại M hóa trị I cần sử dụng hết 1,12 lít khí O2 ở đktc. Kim loại M là A. Na. B. K. C. Ca. D. Ba.Cây 38. Cho 8,5 gam oxit kim loại hóa trị II tác dụng vừa đủ với 2,24 khí hidro ở đktc. CTHH của oxit kim loại là A. CuO B. ZnO C. FeO D. MgOCâu 39. Trong các phát biểu sau, phát biểu nào là sai?A. Oxi tan nhiều trong nước. B....
Đọc tiếp
Câu 36. Khi phân hủy có xúc tác 14,7 gam KClO3, thể tích khí oxi thu được là
A. 4,032 lít. B. 8,064 lít. C. 7,092 lít. D. 12, 096 lít.
Câu 37. Đốt cháy hoàn toàn 4,6 gam một kim loại M hóa trị I cần sử dụng hết 1,12 lít khí O2 ở đktc. Kim loại M là
A. Na. B. K. C. Ca. D. Ba.
Cây 38. Cho 8,5 gam oxit kim loại hóa trị II tác dụng vừa đủ với 2,24 khí hidro ở đktc. CTHH của oxit kim loại là
A. CuO B. ZnO C. FeO D. MgO
Câu 39. Trong các phát biểu sau, phát biểu nào là sai?
A. Oxi tan nhiều trong nước. B. Oxi nặng hơn không khí.
C. Oxi chiếm 1/5 thể tích không khí. D. Oxi là chất khí không màu, không mùi, không vị.
Câu 40. Khi đưa que đóm tàn đỏ vào miện ống nghiệm chứ oxi có hiện tượng gì xảy ra?
A. Tàn đóm bùng cháy. B. Tàn đóm tắt dần.
C. Tàn đóm tắt ngay. D. Không có hiện tượng gì.
đốt cháy hoàn toàn 7,6 g một chất x cần dùng 8,96 lít o2 điều kiện tiêu chuẩn thu được m CO2 - n H2O = 6 gam công thức phân tử của x
Xem chi tiết
Ta có: \(n_{O_2}=0,4\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{CO_2}=x\left(mol\right)\\n_{H_2O}=y\left(mol\right)\end{matrix}\right.\)
Theo đầu bài, có: 44x - 18y = 6 (1)
Theo ĐLBT KL, có: mX + mO2 = mCO2 + mH2O
⇒ 44x + 18y = 7,6 + 0,4.32 = 20,4 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CO_2}=0,3\left(mol\right)\\n_{H_2O}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_C=0,3\left(mol\right)\\n_H=0,8\left(mol\right)\end{matrix}\right.\)
Vì đốt cháy X thu được CO2 và H2O nên X chắc chắn có C và H, có thể có O.
Có: mC + mH = 0,3.12 + 0,8.1 = 4,4 (g) < mX.
⇒ X chứa nguyên tố O.
⇒ mO = 7,6 - 4,4 = 3,2 (g) ⇒ nO = 0,2 (mol)
Giả sử: CTPT của X là CxHyOz (x, y, z nguyên dương).
⇒ x : y : z = 0,3 : 0,8 : 0,2 = 3 : 8 :2
⇒ CTĐGN của X là C3H8O2.
Không biết đề bài còn thiếu phần nào không bạn nhỉ?
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn một hỗn hợp A (glucôzơ, anđehit fomic, axit axetic) cần 2.24 lít O2 (điều kiện tiêu chuẩn). Dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2, thấy khối lượng bình tăng m gam. Giá trị của m là A. 6.2 B. 4.4 C. 3.1 D. 12.4
Đọc tiếp
Đốt cháy hoàn toàn một hỗn hợp A (glucôzơ, anđehit fomic, axit axetic) cần 2.24 lít O2 (điều kiện tiêu chuẩn). Dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2, thấy khối lượng bình tăng m gam. Giá trị của m là
A. 6.2
B. 4.4
C. 3.1
D. 12.4
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2, thu được 6,384 lít CO2 và 4,77 gam H2O. Mặt khác, m gam X phản ứng vừa đủ với x gam Br2 (trong dung môi CCl4). Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Giá trị của x là A. 4,0. B. 3,2. C. 4,8. D. 1,6.
Đọc tiếp
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2, thu được 6,384 lít CO2 và 4,77 gam H2O. Mặt khác, m gam X phản ứng vừa đủ với x gam Br2 (trong dung môi CCl4). Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Giá trị của x là
A. 4,0.
B. 3,2.
C. 4,8.
D. 1,6.
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2, thu được 6,384 lít CO2 và 4,77 gam H2O. Mặt khác, m gam X phản ứng vừa đủ với x gam Br2 (trong dung môi CCl4). Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Giá trị của x là A. 4,0. B. 3,2. C. 4,8. D. 1,6.
Đọc tiếp
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2, thu được 6,384 lít CO2 và 4,77 gam H2O. Mặt khác, m gam X phản ứng vừa đủ với x gam Br2 (trong dung môi CCl4). Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Giá trị của x là
A. 4,0.
B. 3,2.
C. 4,8.
D. 1,6.
Chọn D.
→
B
T
O
n
X
=
0
,
005
m
o
l
mà ![]() (có 2 liên kết pi ở gốc H.C)
(có 2 liên kết pi ở gốc H.C)
n B r 2 = 2 n X = 0 , 01 m o l ⇒ x = 1 , 6 g a m
Đúng 0
Bình luận (0)
Bài 3. Đốt cháy hết 18 gam một kim loại M (có hóa trị II không đổi) cần dùng vừa đủ 8,4 lít khí O2 (đktc). Xác định kim loại M
\(2M+O_2\to 2MO\\ n_{O_2}=\frac{8,4}{22,4}=0,375mol\\ n_M=2n_{O_2}=2.0,375=0,75mol\\ m_M=\frac{18}{0,75}=24 (g/mol)\\ \Rightarrow M: Mg( Magie)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 2 amin no đơn chức đồng đẳng kế tiếp cần 2,24 lít O2 thu được 1,12 lít CO2 (các khí đều đo ở điều kiện tiêu chuẩn). Công thức của 2 amin là: A. C3H7NH2, C4H9NH2 B. C2H5NH2, C3H7NH2 C. C4H9NH2, C5H11NH2 D. CH3NH2, C2H5NH2
Đọc tiếp
Đốt cháy hoàn toàn 2 amin no đơn chức đồng đẳng kế tiếp cần 2,24 lít O2 thu được 1,12 lít CO2 (các khí đều đo ở điều kiện tiêu chuẩn). Công thức của 2 amin là:
A. C3H7NH2, C4H9NH2
B. C2H5NH2, C3H7NH2
C. C4H9NH2, C5H11NH2
D. CH3NH2, C2H5NH2