Đốt cháy hoàn toàn 4,2g Hidrocacbon A thu được 6,72 lít khí CO2 (đktc) và hơi nước. Biết A có tỉ khối Hidro là 21. Xác định công thức phân tử của Hidrocacbon.
Giúp em với ạ :<
Em cảm ơn nhiều :3
Đốt cháy hoàn toàn 5,7 gam chất hữu cơ X thu được 6,72 lít khí CO2 (đktc) và 4,5 gam H2O. a. Xác định công thức đơn giản nhất của X. b. Xác định công thức phân tử của X, biết tỉ khối hơi của X so với H2 là 57.
nCO2= 0,3(mol) -> nC=0,3(mol)
nH2O =0,25(mol) -> nH=0,5(mol)
mC+mH=0,3.12+0,5.1=4,1(g) < 5,7(g)
=>mO=5,7-4,1=1,6(g) -> nO=0,1(mol)
Gọi CTTQ X: CxHyOz (x,y,z: nguyên, dương)
Ta có: x:y:z= 0,3:0,5:1= 3:5:1
=> CT ĐG nhất X: C3H5O.
b) M(X)=57.2=114(g/mol)
Mà: M(X)=M(C3H5O)a= 57a
<=>114=57a
<=>a=2
=>CTPT X : C6H10O2
Đốt cháy hoàn toàn a lit khí hidrocacbon C x H y , thu được 6,72 lit khí C O 2 và 7,2g H 2 O . Tìm công thức phân tử hidrocacbon, biết hidrocacbon này có tỉ khối so với heli bằg 11, các khí được đo ở đktc.
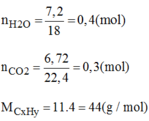
Phương trình hóa học của phản ứng:
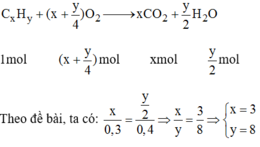
Công thức phân tử của H.C có dạng C 3 H 8 n
→ (12.3 + 1.8).n= 44 → n=1
Vậy công thức phân tử là C 3 H 8
Đốt cháy hoàn toàn 2,24lít Hyđrô cácbon thể khí thu được 6,72 lít khí CO2 và 5,4 lít hơi nước. Xác định công thức phân tử của hợp chất này , biết rằng các thể khí đều ở đktc
\(n_C=n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_H=2n_{H_2O}=2.\dfrac{5,4}{18}=0,6\left(g\right)\\ n_{C_xH_y}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ CTPT:C_xH_y\\ x:y=0,3:0,6=1:2\\ \Rightarrow\left(CH_2\right)_n=\dfrac{0,3.12+0,6}{0,1}=42\left(\dfrac{g}{mol}\right)\\ \Rightarrow n=3\\ CTPT:C_3H_6\)
Đốt cháy hoàn toàn 0,74 gam hợp chất hữu cơ Y (chứa C, H, O), thu được 6,72 lít khí CO2 ở đktc và 0,54 gam H2O. Tỉ khối hơi của X so với H2 là 37. Xác định công thức phân tử của Y?
Bn check lại đề chứ mình nghĩ VCO2 = 0,672
\(n_{CO_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
\(n_{H_2O}=\dfrac{0,54}{18}=0,03\left(mol\right)\)
Bảo toàn C: nC(Y) = 0,03 (mol)
Bảo toàn H: nH(Y) = 2.0,03 = 0,06 (mol)
=> \(n_O=\dfrac{0,74-0,03.12-0,06}{16}=0,02\left(mol\right)\)
nC : nH : nO = 0,03 : 0,06 : 0,02 = 3:6:2
=> CTHH: (C3H6O2)n
Mà M = 2.37 = 74
=> n = 1
=> CTHH: C3H6O2
Đốt cháy hoàn toàn 2g chất hữu cơ A chứa C, H, O thu được 4,4 g CO2 và 1,792 l hơi ( đktc ). Biết tỉ khối hơi của A so với hidro là 100. Xác định công thức phân tử của A
Ta có: \(d_{A/H_2}=100\)
\(\Rightarrow M_A=100.2=200\left(g/mol\right)\)
\(\Rightarrow n_A=\dfrac{2}{200}=0,01\left(mol\right)\)
\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\Rightarrow n_C=0,1\left(mol\right)\)
⇒ Số nguyên tử C trong A là: \(\dfrac{0,1}{0,01}=10\)
\(n_{H_2O}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\Rightarrow n_H=0,08.2=0,16\left(mol\right)\)
⇒ Số nguyên tử H trong A là: \(\dfrac{0,16}{0,01}=16\)
Giả sử n là số nguyên tử O có trong A.
Ta có: 10.12 + 16 + n.16 = 200
⇒ n = 4
Vậy: CTPT của A là C10H16O4.
Bạn tham khảo nhé!
Bảo toàn nguyên tố với C,H :
\(n_C = n_{CO_2} = \dfrac{4,4}{44}= 0,1(mol)\\ n_H = 2n_{H_2O} = 2.\dfrac{1,792}{22,4} = 0,16(mol)\)
Mà :
\(m_O = m_A - m_C - m_H = 2 - 0,1.12 - 0,16 = 0,64(gam)\\ \Rightarrow n_O = \dfrac{0,64}{16} = 0,04(mol)\)
Ta có :
\(n_C: n_H : n_O = 0,1 :0,16 : 0,04 = 5 : 8 : 2\)
Vậy CTPT của A là : \((C_5H_8O_2)_n\)
Mà :
\(M_A = (12.5+8+16.2)n = M_{H_2}.100 = 200(đvC)\\ \Rightarrow n = 2\)
Vậy CTPT của A : \(C_{10}H_{16}O_4\)
đốt cháy hoàn toàn 1,12g một chất hữ cơ A cần 2,688 lít khí O2 (đktc). Toàn bộ sản phẩm cháy gồm CO2 và hơi nước được hấp thụ hết vào bình đựng nước vôi trong dư thu được 8g kết tủa
1/ xác định công thức phân tử của chất A, biết tỉ khối hơi của A so với hidro là 28
2/ viết công thức cấu tạo các chất ứng với coog thức phân tử A
Đốt cháy hoàn toàn 1,88 gam chất hữu cơ A (chứa C, H, O) cần 1,904 lít O2 (đktc) thu được CO2 và hơi nước theo tỉ lệ thể tích 4:3. Hãy xác định công thức phân tử của A. Biết tỉ khối của A so với không khí nhỏ hơn 7.
A. C8H12O5.
B. C4H8O2.
C. C8H42O3.
D. C6H12O6.
Thông thường khi đề bài cho số mol O2 cần để đốt cháy thì chắc chắn ta sẽ phải sử dụng hoặc định luật bảo khối lượng, hoặc bảo toàn nguyên tố Oxi.
Quay trở lại bài toán này, ta thấy đề cho cần dùng 1,904 lít O2, không cho khối lượng CO2 và H2O mà chỉ cho tỉ lệ thể tích (tỉ lệ số mol), do đó nhận ra được nếu ta sử dụng phương pháp bảo toàn khối lượng ta sẽ tính được số mol CO2 và số mol H2O, từ đó tính được số mol O trong A. Tiếp theo đó ta sẽ xác định công thức đơn giản nhất để tìm ra công thức phân tử.
Có: n O 2 = 1 , 904 22 , 4 = 0 , 085 ( m o l ) ⇒ m O 2 = 0 , 085 . 32 = 2 , 72 ( g a m )
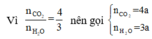
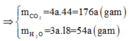
Sơ đồ phản ứng: A + O2 ⇒ CO2 + H2O
Áp dụng định luật bảo toàn khối lượng ta có: m A + m O 2 = m C O 2 + m H 2 O
Hay 1,88 + 2,72 = 176a + 54a ⟺ a = 0,02
⇒ 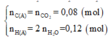
![]()
![]()
Vì C : H : O = nC : nH : nO =0,08 : 0,12 : 0,05 = 8 : 12 : 5
Nên công thức đơn giản nhất của A là C8H12O5.
Khi đó công thức phân tử của A có dạng (C8H12O5)n
Mà MA < 7Mkhôngkhí nên 188n < 7.29 ⇒ n < 1,08 ⇒ n = l
Do đó công thức phân tử của A là C8H12O5.
Đáp án A.
Đốt cháy 4,2g một hợp chất A thu được 6,72 lít CO2 (đktc) và 5,4g H2O. Biết tỉ khối của A đối với oxi là 1,3125. Tìm công thức phân tử A
C3H6
Giải thích các bước giải:
A + O2 ---> CO2 + H2O
nCO2=6,72 /22,4=0,3 mol
nH2O=5,4/18=0,3 mol
-> A chứa 0,3 mol C và 0,6 mol H
-> C : H=0,3:0,6=1:2 -> A có dạng (CH2)n
Ta có: dA/O2=1,3125 -> mA=32.1,3125=42 -> 14n=42 -> n=3
-> A là C3H6
Câu 1: Đốt cháy hoàn toàn 1 hiđrocacbon, sau phản ứng thu được 6,72 lít CO2 và 5,4 g H2O. Tỉ khối hơi của hiđrocacbon so với oxi bằng 1,3125. Xác định công thức phân tử của hiđrocacbon.
Câu 2: Đốt cháy 4,5 gam chất hữu cơ thu được 6,6 gam khí CO2 và 2,7 gam H2O. Biết khối lượng mol của chất hữu cơ là 60 gam. Xác định công thức phân tử của chất hữu cơ.
Câu 1:
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
Gọi CTPT cần tìm là CxHy.
⇒ x:y = 0,3:0,6 = 1:2
→ CTPT cần tìm có dạng (CH2)n
Mà: M = 1,3125.32 = 42 (g/mol)
\(\Rightarrow n=\dfrac{42}{12+1.2}=3\)
Vậy: CTPT đó là C3H6.
Câu 2:
\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\Rightarrow n_H=0,15.2=0,3\left(mol\right)\)
Có: mC + mH = 0,15.12 + 0,3.1 = 2,1 (g) < 4,5 (g)
→ Chất cần tìm gồm: C, H và O.
⇒ mO = 4,5 - 2,1 = 2,4 (g) \(\Rightarrow n_O=\dfrac{2,4}{16}=0,15\left(mol\right)\)
Gọi: CTPT cần tìm là CxHyOz.
⇒ x:y:z = 0,15:0,3:0,15 = 1:2:1
→ CTPT cần tìm có dạng (CH2O)n
\(\Rightarrow n=\dfrac{60}{12+1.2+16}=2\)
Vậy: CTPT đó là C2H4O2