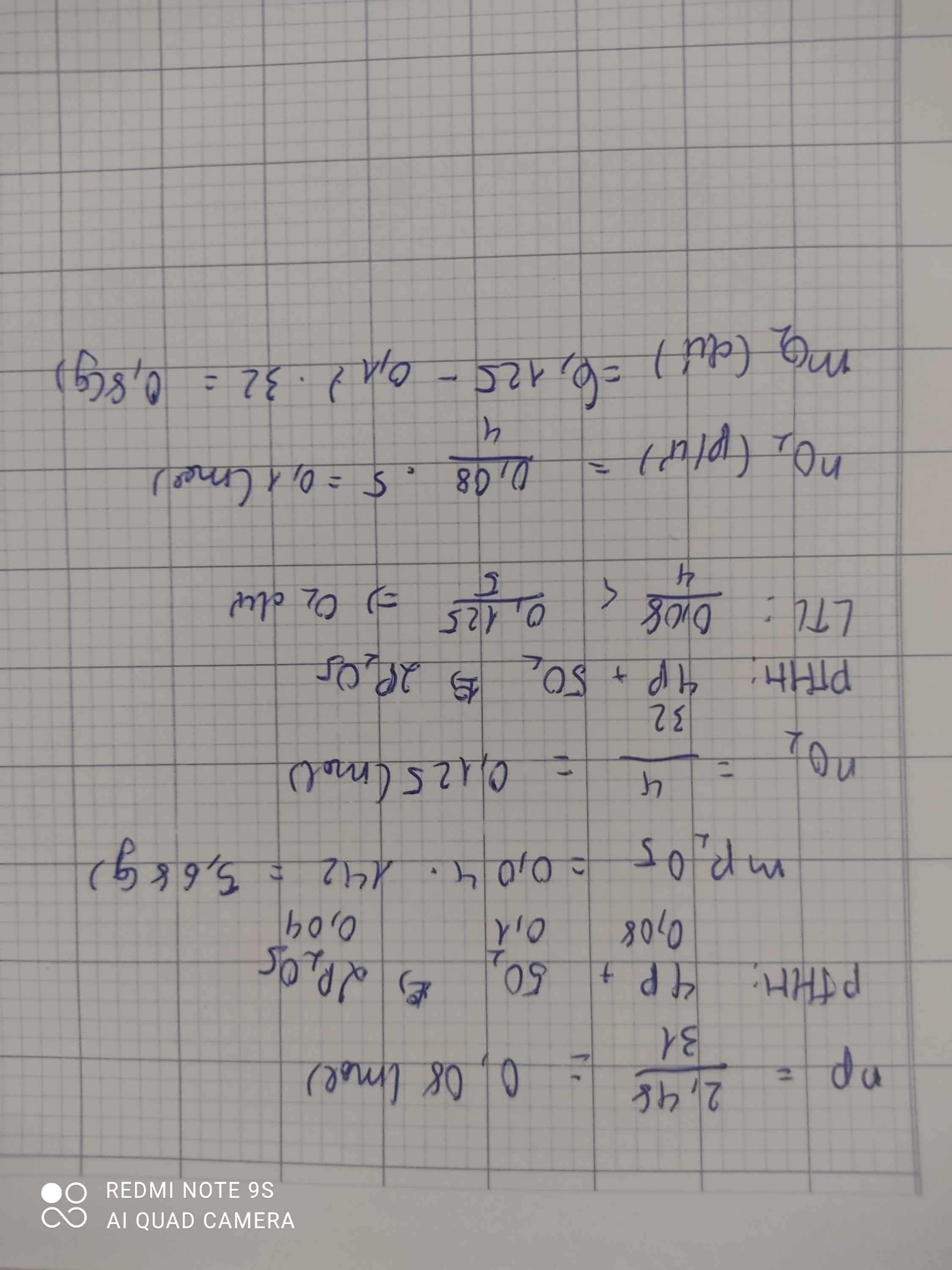1.Đốt cháy 6,2g photpho trong bình chứa 6,4g oxi. Sau phản ứng hoàn toàn,chất nào còn dư? (P=31,O=16) * Oxi Hai chất đều dư Hai chất phản ứng vừa đủ Photpho
2.Số gam KMnO4 cần dùng để đièu chế được 2,24 lít khí oxi (đktc) là: (K=39,Mn=55,O=16) * 31,6 gam 20,7 gam 40,8 gam 14,3 gam