Cho hỗn hợp X gồm CO2 và N2 (ở đktc) có tỉ khối so với oxi là 1,225.
a/ Tính % theo thể tích của N2 trong hỗn hợp.
b/ Dẫn V lít X vào dung dịch Ca(OH)2 dư, thấy tạo thành 20 gam kết tủa CaCO3. Tìm V.
Cho 10 lít (đktc) hỗn hợp khí gồm N2 và CO2 tác dụng với 2 lít dung dịch Ca(OH)2 0,02 mol/l thu được 1 gam kết tủa. Thành phần % theo thể tích N2 trong hỗn hợp ban đầu là:
A. 2,24% hoặc 84,32%
B. 2,24% hoặc 15,68%
C. 15,68% hoặc 97,76%
D. 84,32% hoặc 97,76%
Đáp án D
Ta có nCa(OH)2= 2.0,02= 0,04 mol; nCaCO3= 1/100= 0,01 mol
Ta có nCa(OH)2 > nCaCO3 nên có 2 trường hợp:
- TH1: Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
Theo PT (1): nCaCO3= nCO2= 0,01 mol →VCO2=0,01.22,4=0,224 lít
→%VCO2= 2,24%→ %VN2= 100%- 2,24%=97,76%
- TH2: Ca(OH)2 phản ứng hết:
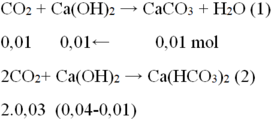
Ta có: nCO2= 0,01+ 2.0,03= 0,07 mol →VCO2= 0,07.22,4=1,568 lít
→%VCO2= 15,68%→ %VN2= 100%- 15,68%=84,32%
Dẫn 1 lít hỗn hợp khí X gồm N2 và CO2 (đktc) đi chậm qua 2 lít dung dịch Ca(OH)2 0,01 M thu được 1g kết tủa. Tính thể tích của N2 và CO2 trong X
nCa(OH)2 = 2.0,01 = 0,02 (mol)
\(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
TH1: Nếu kết tủa không bị hòa tan
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,01<----0,01
=> \(\left\{{}\begin{matrix}V_{CO_2}=0,01.22,4=0,224\left(l\right)\\V_{N_2}=1-0,224=0,776\left(l\right)\end{matrix}\right.\)
TH2: Nếu kết tủa bị hòa tan 1 phần
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,02---->0,02------>0,02
CaCO3 + CO2 + H2O --> Ca(HCO3)2
0,01--->0,01
=> VCO2 = (0,02 + 0,01).22,4 = 0,672 (l)
=> VN2 = 1 - 0,672 = 0,328 (l)
Hỗn hợp X gồm SO2 và O2 có tỉ khối so với N2 bằng 2. Lấy 4,48 lít hỗn hợp X ở đktc cho đi qua bình đựng V2O5 nung nóng thu được hỗn hợp Y. Cho toàn bộ hỗn hợp Y thu được lội qua dung dịch Ba(OH)2 dư thấy có 33,51 gam kết tủa. Hiệu suất phản ứng oxi hóa SO2 thành SO3 là:
A. 60%.
B. 75%.
C. 95%.
D. 40%
Đáp án A
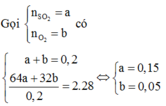
Có: ![]()
Mol trước phản ứng 0,15 0,05
Mol phản ứng 2x x 2x
Mol cân bằng (0,15 – 2x) (0,05 – x) 2x
Do đó
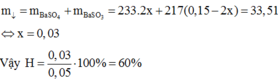
Hỗn hợp X gồm SO2 và O2 có tỉ khối so với N2 bằng 2. Lấy 4,48 lít hỗn hợp X ở đktc cho đi qua bình đựng V2O5 nung nóng thu được hỗn hợp Y. Cho toàn bộ hỗn hợp Y thu được lội qua dung dịch Ba(OH)2 dư thấy có 33,51 gam kết tủa. Hiệu suất phản ứng oxi hóa SO2 thành SO3 là:
A. 60%.
B. 75%.
C. 95%.
D. 40%
Đáp án A
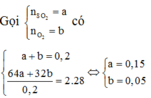
Có: ![]()
Mol trước phản ứng 0,15 0,05
Mol phản ứng 2x x 2x
Mol cân bằng (0,15 – 2x) (0,05 – x) 2x
Do đó
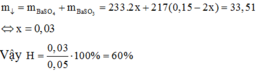
Cho 5,6 lít hỗn hợp X gồm N2 và CO2 (đktc) đi chậm qua 5 lít dung dịch Ca(OH)2 0,02M để phản ứng xảy ra hoàn toàn thu được 5 gam kết tủa. Tính tỉ khối hơi của hỗn hợp X so với H2.
n(Ca(OH)2) = 0,1 mol; n(CaCO3) = 0,05.
TH1: CO2 thiếu
CO2 + Ca(OH)2 → CaCO3 + H2O.
→ n(CaCO3) = n(CO2) = 0,05.=> n(N2) = 0,25 – 0,05 = 0,2.
Nên dX/H2 =\(\dfrac{0,05.44+0,2.28}{0,25.2}\) = 15,6. Không có đáp án nào.
TH2: CO2 phản ứng hết,
CO2 + Ca(OH)2 → CaCO3 + H2O.
0,05 0,05 0,05
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,1 ← (0,1 – 0,05)
=> n(CO2) = 0,15 => n(N2) = 0,25 – 0,15 = 0,1.
Nên dX/H2 =\(\dfrac{0,15.44+0,1.28}{0,25.2}\) = 18,8. Thỏa mãn.
Cho a gam hỗn hợp A gồm Mg, Al vào b gam dung dịch HNO3 24% đủ thu được 8,96 lít hỗn hợp khí X gồm NO, N2O, N2 (đktc) và dung dịch B. Thêm một lượng O2 vừa đủ vào X, sau phản ứng được hỗn hợp Y. Dẫn Y từ từ qua dung dịch NaOH dư thu được 4,48 lít hỗn hợp khí Z (đktc) có tỷ khối hơi so với H2 là 20. Nếu cho dung dịch NH3 dư vào B thì thu được được 62,2 gam kết tủa. Phần trăm thể tích của NO trong X là:
A. 50%.
B. 40%
C. 30%
D. 20%
Khi cho 3,36 lít (đo ở đktc) hỗn hợp khí X gồm N2, CO và CO2 đi qua CuO dư đốt nóng, rồi sục vào dung dịch nước vôi trong dư, thì thu được 10 gam kết tủa và 4,8 gam đồng. Thành phần % về thể tích của N2 trong hỗn hợp X là giá trị nào dưới đây?
A. 16,67%
B. 33,33%
C. 50,00%
D. 66,67%
Đáp án B
Đặt n N 2 = x mol; nCO = y mol; n C O 2 = z mol
→ x+y+z=3,36/22,4= 0,15 mol
C O + C u O → t 0 C u + C O 2 ( 1 ) y y y m o l
ta có: y = nCu = 4,8/64= 0,075 mol; n C O 2 = y + z mol
CO2+ Ca(OH)2 → CaCO3+ H2O
Ta có: n C a C O 3 = n C O 2 = y+z = 10/100 = 0,1 mol →z = 0,025 mol
→x = 0,05 mol→% V N 2 = % n N 2 = 33,33%
Cho hỗn hợp khí X gồm CO2 và N2 (ở đktc) có tỉ khối đối với khí oxi là 1,225.
1. Tính thành phần % theo thể tích của mỗi khí trong hỗn hợp X.
2. Tính khối lương của 1 lít hỗn hợp khí X ở đktc.
1)
Coi \(n_X = 1(mol)\)
Gọi : \(n_{CO_2} = a(mol) ; n_{N_2} = b(mol)\)
Ta có :
\(n_X = a + b = 1(mol)\\ m_X = 44a + 28b = 1.1,225.32(gam)\\ \Rightarrow a = 0,7 ; b = 0,3\)
Vậy :
\(\%V_{CO_2} = \dfrac{0,7}{1}.100\% = 70\%\\ \%V_{N_2} = 100\% - 70\% = 30\%\)
2)
\(n_X = \dfrac{1}{22,4}(mol)\\ \Rightarrow m_X = n.M = \dfrac{1}{22,4}.1,225.32 = 1,75(gam)\)
Cho 11,2 lít (đktc) hỗn hợp khí X gồm N2, CO và CO2 qua dung dịch Ca(OH)2 dư thu được 15 gam kết tủa, sau đó đi qua ống sứ chứa CuO dư nung nóng thấy khối lượng chất rắn trong ống sứ giảm đi 1,6 gam. Nếu cho 5,6 lít hỗn hợp khí trên đi qua ống sứ chứa CuO dư nung nóng rồi dẫn sản phẩm khí đi qua dung dịch Ca(OH)2 thì lượng kết tủa thu được là
A. 12,5 gam
B. 25,0 gam
C. 15,0 gam
D. 7,50 gam
Đáp án A.
→ n X = 0 , 5 ; n C O 2 = 0 , 15 ; n C O = 0 , 1 → n N 2 = 0 , 25
→
n
X
=
0
,
25
→
n
C
a
C
O
3
=
n
C
O
+
n
C
O
2
=
0
,
125
→
m
=
12
,
5