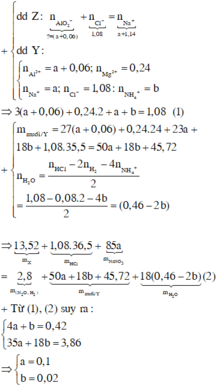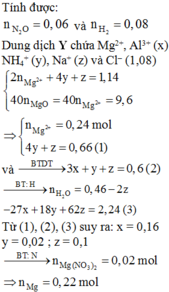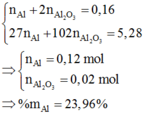hòa tan 29,4g hỗn hợp gồm Cu,Al,Mg vào 200ml HCl thu được 11.2L khí(dkc) 19,2g chất không tan
a)tính % khối lượng trong hỗn hợp đầu
b)cho dung dịch muối thu được tác dụng AgNO3.Tính khối lượng kết tu

Những câu hỏi liên quan
Câu 1: Hòa tan hoàn toàn 12,725g hỗn hợp Mg, Al, Zn bằng dung dịch HCl thu được dung dịch A và 11,2 l H2 ở đktc. Tính khối lượng muối có trong dung dịch A.
Câu 2: Cho 11,8g hỗn hợp Cu, Al tác dụng với khí õi thu được 18,2g hỗn hợp oxit. Tính % khối lượng của Cu trong hỗn hợp ban đầu.
Câu 2 :
\(n_{Cu}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m=64a+27b=11.8\left(g\right)\left(1\right)\)
\(BTKL:m_{O_2}=18.2-11.8=6.4\left(g\right)\)
\(n_{O_2}=\dfrac{6.4}{32}=0.2\left(mol\right)\)
\(2Cu+O_2\underrightarrow{^{^{t^0}}}2CuO\)
\(4Al+3O_2\underrightarrow{^{^{t^0}}}2Al_2O_3\)
\(n_{O_2}=0.5a+0.75b=0.2\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(\%Cu=\dfrac{0.1\cdot64}{11.8}\cdot100\%=54.23\%\)
Đúng 1
Bình luận (0)
Câu 1 :
\(n_{HCl}=2n_{H_2}=2\cdot\dfrac{11.2}{22.4}=1\left(mol\right)\)
\(BTKL:\)
\(m_{Muối}=12.725+1\cdot36.5-0.5\cdot2=48.225\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch chứa hai chất tan NaNO3 và 1,08 mol HCl. Sau khi kết thúc phản ứng, thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2, có tỉ khối so với He bằng 5. Dung dịch Y tác dụng tối đa với dung dịch chứa 1,14 mol NaOH, lấy kết tủa nung ngoài không khí tới khối lượng không đổi thu được 9,6 gam chất rắn. Khối lượng của Al có trong hỗn hợp X là A. 5,40 gam. B. 2,70 gam. C. 4,05 gam. D. 3,24 ga...
Đọc tiếp
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch chứa hai chất tan NaNO3 và 1,08 mol HCl. Sau khi kết thúc phản ứng, thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2, có tỉ khối so với He bằng 5. Dung dịch Y tác dụng tối đa với dung dịch chứa 1,14 mol NaOH, lấy kết tủa nung ngoài không khí tới khối lượng không đổi thu được 9,6 gam chất rắn. Khối lượng của Al có trong hỗn hợp X là
A. 5,40 gam.
B. 2,70 gam.
C. 4,05 gam.
D. 3,24 gam
Đáp án D
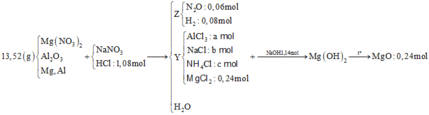
∑ nZ = 3,136 : 22,4 = 0,14 (mol)
Dùng quy tắc đường chéo tính được nN2O: nH2 = 3: 4
=> nN2O = 0,06 (mol); nH2 = 0,08 (mol)
∑ nHCl = 3a + b + c + 0,24.2 = 0,18 (1)
∑ nNaOH = 4a + c + 0,24.2 = 1,14 (2)
Bảo toàn nguyên tố H
nHCl = 4nNH4Cl + 2nH2 + 2nH2O
=> nH2O = 0,46 – 2c
Bảo toàn khối lượng:
mX + mNaNO3 + mHCl = mY + mZ + mH2O
=> 13,52 + 1,08.36,5 + 85b = 133,5a + 58,5b + 53,5c + 95.0,24 + 0,14.20 + 18( 0,46 – 2c) (3)
Từ (1), (2) và (3)
=> a = 0,16 ; b = 0,1 và c = 0,02 (mol)
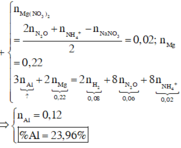
Ta có: nH+ = 10nN2O + 10nNH4 + 2nH2 + 2nO (Oxit)
=> nO(Oxit) = 0,06 (mol0 => nAl2O3 = 0,02 (mol)
=> nAl = 0,12 (mol)
=> %Al = 0,12.27 = 3,24 (g)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp X gồm Na, Mg, Al vào nước thu được 8,96 lít H2 (ở đktc) và dung dịch Z còn lại 5,1 gam chất rắn không tan Y. Cho Y tác dụng với dung dịc HCl thu được 0,25 mol khí H2. Tính khối lượng của Al trong hỗn hợp X?
Giả sử số mol của Mg, Al trong Y lần lượt là a, b (mol)
=> 24a + 27b = 5,1
PTHH: Mg + 2HCl --> MgCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
=> a + 1,5b = 0,25
=> a = 0,1 ; b = 0,1
Gọi số mol Na là k (mol)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
k-------------------->k---->0,5k
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
k<-----k------------------------------>1,5k
=> 0,5k + 1,5k = 0,4
=> k = 0,2 (mol)
=> nAl(X) = 0,2 + 0,1 = 0,3 (mol)
=> mAl(X) = 0,3.27 = 8,1 (g)
Đúng 4
Bình luận (0)
C1: Cho 10.8 g hỗn hợp gồm Mg và Fe tác dụng với 102.2 g dung dịch HCl 20% thu được dung dịch A và 5.6 l khí- tính % khối lượng của mỗi kim loại trong hỗn hợp- tính % nồng độ các chất trong dung dịch A- cho dung dịch A tác dụng với lượng dư dung dịch AgNO3. tính khối lượng kết tủa.C2: cho 1.74 g hỗn hợp A gồm nhôm và magie tác dụn vừa đủ 100ml dung dịch HCl có D 1.05 g/ml, thu được 1.792l H2 và dung dịch X.- tính % khối lượng của nhôm- cho dung dịch X tác dụng vừa đủ 50 g dung dịch AgNO3 thu đư...
Đọc tiếp
C1: Cho 10.8 g hỗn hợp gồm Mg và Fe tác dụng với 102.2 g dung dịch HCl 20% thu được dung dịch A và 5.6 l khí
- tính % khối lượng của mỗi kim loại trong hỗn hợp
- tính % nồng độ các chất trong dung dịch A
- cho dung dịch A tác dụng với lượng dư dung dịch AgNO3. tính khối lượng kết tủa.
C2: cho 1.74 g hỗn hợp A gồm nhôm và magie tác dụn vừa đủ 100ml dung dịch HCl có D = 1.05 g/ml, thu được 1.792l H2 và dung dịch X.
- tính % khối lượng của nhôm
- cho dung dịch X tác dụng vừa đủ 50 g dung dịch AgNO3 thu được dung dịch Y. Tính C% dung dịch Y
C3: hòa tan hoàn toàn 10.3 gam hỗn hợp Mg và MgCO3 trong 100g dung dịch HCl 18.25% thu được dung dịch X và 4.48l hỗn hợp khí Y
- tính % khối lượng mỗi chất trong hỗn hợp ban đầu
- tính nồng độ % của các chất trong dung dịch X
- cho toàn bộ lượng khí H2 trong Y tác dụng với 1.68 l khí Cl2 (hiệu suất phản ứng 80%) rồi hấp thụ toàn bộ sản phẩm thu được vào dung dịch AgNO3 dư thì thu được bao nhiêu gam kết tủa?
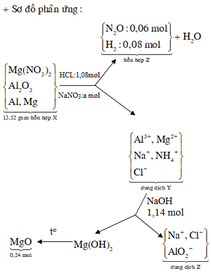
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch chứa hai chất tan NaNO3 và 1,08 mol HCl. Sau khi kết thức phản ứng, thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2, có tỉ khối so với He bằng 5. Dung dịch Y tác dụng tối đa với dung dịch chứa 1,14 mol NaOH, lấy kết tủa nung ngoài không khí tới khối lượng không đổi thu được 9,6 gam rắn. Phần trăm khối lượng của Al có trong hỗn hợp X là : A. 31,95%. B. 19,97%. C. 23,96%. D. 27,96%...
Đọc tiếp
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch chứa hai chất tan NaNO3 và 1,08 mol HCl. Sau khi kết thức phản ứng, thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2, có tỉ khối so với He bằng 5. Dung dịch Y tác dụng tối đa với dung dịch chứa 1,14 mol NaOH, lấy kết tủa nung ngoài không khí tới khối lượng không đổi thu được 9,6 gam rắn. Phần trăm khối lượng của Al có trong hỗn hợp X là :
A. 31,95%.
B. 19,97%.
C. 23,96%.
D. 27,96%.
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch chứa hai chất tan NaNO3 và 1,08 mol HCl. Sau khi kết thức phản ứng, thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2, có tỉ khối so với He bằng 5. Dung dịch Y tác dụng tối đa với dung dịch chứa 1,14 mol NaOH, lấy kết tủa nung ngoài không khí tới khối lượng không đổi thu được 9,6 gam rắn. Phần trăm khối lượng của Al có trong hỗn hợp X là : A. 31,95%. B. 19,97%. C. 23,96%. D. 27,96%...
Đọc tiếp
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch chứa hai chất tan NaNO3 và 1,08 mol HCl. Sau khi kết thức phản ứng, thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2, có tỉ khối so với He bằng 5. Dung dịch Y tác dụng tối đa với dung dịch chứa 1,14 mol NaOH, lấy kết tủa nung ngoài không khí tới khối lượng không đổi thu được 9,6 gam rắn. Phần trăm khối lượng của Al có trong hỗn hợp X là :
A. 31,95%.
B. 19,97%.
C. 23,96%.
D. 27,96%.
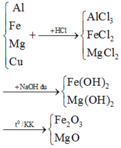
Cho hỗn hợp bột gồm Al, Fe, Mg và Cu tác dụng với lượng dư dung dịch HCl. Lọc bỏ phần chất rắn không tan thu được dung dịch X. Cho X tác dụng với lượng dư dung dịch NaOH thu được kết tủa Y. Nung Y trong không khí đến khối lượng không đổi, thu được chất rắn Z. Chất rắn Z gồm: A. Fe2O3; MgO; CuO. B. MgO; FeO. C. Fe2O3; MgO. D. Al2O3; Fe2O3; MgO.
Đọc tiếp
Cho hỗn hợp bột gồm Al, Fe, Mg và Cu tác dụng với lượng dư dung dịch HCl. Lọc bỏ phần chất rắn không tan thu được dung dịch X. Cho X tác dụng với lượng dư dung dịch NaOH thu được kết tủa Y. Nung Y trong không khí đến khối lượng không đổi, thu được chất rắn Z. Chất rắn Z gồm:
A. Fe2O3; MgO; CuO.
B. MgO; FeO.
C. Fe2O3; MgO.
D. Al2O3; Fe2O3; MgO.
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch NaNO3 và 1,08 mol HCl (đun nóng). Sau khi kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2. Tỉ khối của Z so với He bằng 5. Cho Y tác dụng với dung dịch NaOH dư, thấy có 1,14 mol NaOH phản ứng, thu được kết tủa T. Nung T trong không khí tới khối lượng không đổi, thu được 9,6 gam rắn. Phần trăm khối lượng của Al có trong hỗn hợp X là A. 23,96%. B. 27,96% C. 19,97%...
Đọc tiếp
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch NaNO3 và 1,08 mol HCl (đun nóng). Sau khi kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2. Tỉ khối của Z so với He bằng 5. Cho Y tác dụng với dung dịch NaOH dư, thấy có 1,14 mol NaOH phản ứng, thu được kết tủa T. Nung T trong không khí tới khối lượng không đổi, thu được 9,6 gam rắn. Phần trăm khối lượng của Al có trong hỗn hợp X là
A. 23,96%.
B. 27,96%
C. 19,97%
D. 31,95%
Hòa tan 14,7g hỗn hợp X gồm Al, Cu, Mg trong 200ml dung dịch HCl aM, thu được 5,6 lít khí (đktc), 9,6g chất rắn Y không tan và dung dịch Aa. Tính khối lượng mỗi kim loại trong Xb. Tính nồng độ mol dung dịch HCl đã dùng. Biết HCl dùng dư 20% so với lượng cần thiếtc. Tính nồng độ mol các chất trong dung dịch Ad. Tính thể tích khí Cl2 (đktc) cần để phản ứng hết với chất rắn Y
Đọc tiếp
Hòa tan 14,7g hỗn hợp X gồm Al, Cu, Mg trong 200ml dung dịch HCl aM, thu được 5,6 lít khí (đktc), 9,6g chất rắn Y không tan và dung dịch A
a. Tính khối lượng mỗi kim loại trong X
b. Tính nồng độ mol dung dịch HCl đã dùng. Biết HCl dùng dư 20% so với lượng cần thiết
c. Tính nồng độ mol các chất trong dung dịch A
d. Tính thể tích khí Cl2 (đktc) cần để phản ứng hết với chất rắn Y
a) \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
mCu = mY = 9,6 (g)
Gọi số mol Al, Mg là a, b
=> 27a + 24b = 14,7 - 9,6 = 5,1 (g)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a-->3a-------->a------>1,5a
Mg + 2HCl --> MgCl2 + H2
b--->2b------->b----->b
=> 1,5a + b = 0,25
=> a = 0,1; b = 0,1
=> \(\left\{{}\begin{matrix}m_{Al}=0,1.27=2,7\left(g\right)\\m_{Mg}=0,1.24=2,4\left(g\right)\\m_{Cu}=9,6\left(g\right)\end{matrix}\right.\)
b) nHCl(PTHH) = 3a + 2b = 0,5 (mol)
=> nHCl(thực tế) = \(\dfrac{0,5.120}{100}=0,6\left(mol\right)\)
=> \(C_{M\left(HCl\right)}=\dfrac{0,6}{0,2}=3M\)
c) \(\left\{{}\begin{matrix}C_{M\left(AlCl_3\right)}=\dfrac{0,1}{0,2}=0,5M\\C_{M\left(MgCl_2\right)}=\dfrac{0,1}{0,2}=0,5M\\C_{M\left(HCldư\right)}=\dfrac{0,6-0,5}{0,2}=0,5M\end{matrix}\right.\)
d) \(n_{Cu}=\dfrac{9,6}{64}=0,15\left(mol\right)\)
PTHH: \(Cu+Cl_2\underrightarrow{t^o}CuCl_2\)
0,15-->0,15
=> \(V_{Cl_2}=0,15.22,4=3,36\left(l\right)\)
Đúng 2
Bình luận (0)